-
Постов
1016 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Roman7474
-
-
-
Конечно,он с восторгом превращается в оксиды,гидроксиды)))
Интересно если его расплавить (t плав. 1100 С) и провести электролиз что будет на электродах?
-
-
Получится ли сульфат алюминия,при сплавлении гидросульфата аммония с оксидом алюминия? Или жженные аммоний-алюминиевые квасцы? Или нефига не получится?
Сульфат алюминия и так прекрасно обезвоживается при 300 С. Зачем его получать спеканием?
-
Сульфат плюс сульфат мэй би.
Сульфат железа плюс сульфат аммония? Сульфат железа 3 ?
-
-
попробуйте при невысокой температуре восстановить до магнетита,водородом. Оксид алюминия-то так и останется,а потом уже магнитиком.
Нет это я пробовал,он почему-то спекается с Al2O3 даже при 400 C.Получается магнитный песок черного цвета с размером частиц около 1 мм.
-
-
Смесь оксидов примерно 50 на 50. Порошок красный,размер частиц как у пищевой соды примерно.Я его с электролитом кипятил Fe2O3 переходит в раствор и он светлеет.В осадке Al2O3. На мешке написано именно эти 2 оксида в составе.Для чего применяли не знаю.А как щелочным методом?А щелочной подходит? Что это, смесь или что?
-
Магнитиком
Ага если бы еще Fe2O3 магнитился.
попробуйте взболтать с водой и дать отстояться, в некоторых случаях удается
И что Fe2O3 наверху должен быть?
-
Кислотный способ не подходит.Может как-то механически можно?
-
Ага, щаз! Медь так и посыпалась...
А куда она денется?
-
Посоветуйте способ разделения хлорида меди и хлорида никеля.
CuCl2 + Ni = NiCl2 + Cu↓
-
От концентрации,и температуры должно зависить направление смещения равновесия.
C Fe(OH)2 должно пойти.
-
В растворе-нет,при сплавлении-наверняка.
По-крайней мере при сплавлении,вполне вероятно. Но может и с оксидом алюминия по-идее.
С гидроксидами в растворе должны реагировать по идее... Например NH4HSO4 + Fe(OH)3 пойдет при подогреве в растворе?
-
-
Такая реакция идет в очень разбавленных растворах, поэтому препаративно она не интересна.
Лучше калите железный купорос и получайте SO3, из которого можно сделать и серку и олеум и хлорсульфонку
Из железного купороса не только SO3 пойдет,но еще и SO2.
NaHSO4 + Fe(OH)3 + H2O будет ли взаимодействовать при нагревании?
-
Сульфат железа разлагается при нагревании

Можно ли потом отфильтровать осадок FeSO4(OH) ? И до какого pH будет идти разложение? Я так понимаю серная кислота выделяется до определенного количества ее в растворе и потом реакция останавливается?
-
Книга "Реакции твердых тел" так описывает разложение нитрита бария
2Ba(NO2)2 = Ba(NO3)2 + BaO + NO + 1/2N2
Вероятно, с нитратом кальция ожидать образование нитрита еще менее вероятно
Т.е. реакция сразу идет до CaO + NO + N2.
Это просто проверить.Нагреть и посмотреть пойдет ли NO2.
Можно ли получить нитрат кальция при нагревании по реакции? Ca(OH)2 + 2NH4NO3 = Ca(NO3)2 + 2NH4OH
NH4OH затем можно выпарить я так понимаю?
-
пойдет NO,Который вырвавшись на воздух,и немного остыв превратится в NO2
Ну тык NO пойдет,а стальной сосуд то окислятся будет и продырявится.
-
Взаимодействует. Получается оксид железа, оксид азота(II) и азот.
Т.е. нагреть Ca(NO2)2 в стальном сосуде для выделения NO2 не получится?
-
-
Разложением?
NH4Cl -> HCl + NH3
При нагревании он разлагается на NH3 и HCl, но при остывании снова соединяется.Выделить по отдельности NH3 и HCl не получается.
-
Правильно так:
Ca(NO3)2 = 2CaO + 4NO2 + O2
Это что получается можно получить азотную кислоту растворяя NO2 в воде?


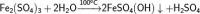
Al2O3+Fe2O3 как разделить?
в Неорганическая химия
Опубликовано
Если Al2O3 такого же размера частицы,почему Fe2O3 должен наверх всплывать с пеной?