-
Постов
1016 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Roman7474
-
-
Смогу ли я получить сульфат аммония приливая серной кислоты к мочевине? Будет выделятся CO2 ?
CO(NH2)2 + H2SO4 (40%) + H2O = ?
-
Какая растворимость, такая и реакция.Взяли бы болтушку, было бы значительно лучше.
А подогрев что-нибудь даст?
-
Да, он плохо реагирует с FeCl3. В этом смысле имел виду.во как, что приливаем, то и выпадает?
-
Fe(NO3)3 + Ca(OH)2 хорошо ли идет реакция? Или Ca(OH)2 сбивается в комки? Например у меня так было с FeCl3 + Ca(OH)2.Приливал раствор Ca(OH)2 к FeCl3 получался осадок Ca(OH)2
-
Дело в том, что Fe2O3 реагирует только с достаточно концентрированными кислотами и после растворения много неизрасходованной кислоты.Если будешь сушить, то кислота улетает.Для сухих оксидов азота подошла бы, для "мокрых", как в нашем случае, лучше эмалированная посуда. У нитрата железа вроде невысокая температура разложения, эмаль должна выдержать.
Здесь придется полностью выкипятить раствор чтобы не потерять кислоту.
А может просто с гидросульфатом аммония спечь, Al2O3 реагирует хуже, затем растворить, отделить осадок Al2O3 и раствор осадить аммиаком? Полученный сульфат аммония снова разлагать до гидросульфата и аммиака?
-
Потери только при обезвоживании кристаллогидрата, эту воду с примесью кислоты можно отгонять в тот же приемник, что и ноксы при дальнейшем разложении. Всяко проще, чем с SO3 возиться- там тоже потери на SO2 будут.
Для этого нужна кислотоупорная, большая посуда. Сталь же не подойдет?
-
-
-
-
Да, на счет нашествия это вы верно сказали.
-
-
Если высушить Fe(OH)SO4 как разлагается при нагревании?Что-то типа
4FeSO4 + 2H2O + O2 = 4Fe(OH)SO4
и так далее вплоть до Fe2O3*nH2O
-
Без кислоты так и должно быть
А что это был за осадок?
-
Спасибо, aversun. Я пробовал без серной кислоты.Пропускал воздух и подогревал.Выпал какой-то осадок.Надо искать прежде всего в голове. Уравнение простейшее
4FeSO4 + 2H2SO4 + O2 = 2Fe2(SO4)3 + 2H2O
-
Напишите пожалуйста уравнение реакции.Что -то нигде не нашел.Там SO2 будет?В соответствии с уравнением реакции + небольшой избыток
А как еще?
Можно.
-
Добавьте кислоты и окисляйте сульфат железа (II) до сульфат железа (III) хоть воздухом, хоть перекисью. Затем прокалите сульфат железа (III). Можно наоборот часть сульфат железа (II) окисляйть до сульфат железа (III), а другую часть прокалить на воздухе.
А серной кислоты много добавлять? Как кислородом окислить?В растворе?Подогревать надо?
-
А у вас,что прям ярко-желтый? Всам-деле?
Светло-желтый
-
-
Какой был,какой стал? Гидратация?
Был зеленоватого цвета, стал желтого.И осадок желтый.
-
-
Как из FeSO4 получить Fe2(SO4)3 и Fe2O3?
-
а что вам нужно-то из смеси выделить,ну или что нужнее?
Окись железа.
-
Так естественно пар будет уносить HCl. Его потом нужно в холодильнике конденсировать, а лишний HCl растворять в воде.
-
Оксихлоридов здесь вроде нет.Нет, уж скорее пойдет для безводной соли так
4FeSO4 + O2 = Fe2O2SO4 + Fe2(SO4)3
А еще скорее через более сложные оксихлориды, последние являются нормальными промежуточными продуктами при разложении сульфатов железа.


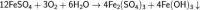
Оксиды железа
в Неорганическая химия
Опубликовано
Т.е. реакция хуже пойдет?