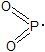-
Постов
10617 -
Зарегистрирован
-
Посещение
-
Победитель дней
47
Тип контента
Профили
Форумы
События
Весь контент M_GM
-
Концентрация HCl даёт вам концентрацию ионов Н(+) Пишем уравнение реакции и выражаем К(равн) ее через Ka и Ks Используя К(равн) и [Н(+)] находим концентрацию [Ca(2+)], которая и будет определять растворимость соли в моль/л
-
В растворе нет Н2СО3, поэтому там нечему диссоциировать по первой ступени Диссоциация это разложение, распад, а ты какую реакцию пишешь? И диссоциирует не раствор, а растворенное вещество И если речь идет об ионах, не забывай указывать их заряды, хотя бы в скобках.
-
Т.е. КОН и НСl не обмениваются ионами?
-
А КОН + HCl - это РИО или нейтрализации?
-
Стандартный электродный потенциал дается для стандартного состояния, т.е. для 1M серной кислоты
- 4 ответа
-
- 1
-

-
Начните с электронной формулы цинка, и его иона в этом комплексе вспомните также тип связи, связывающей ион цинка и молекулы воды тогда можно будет понять какие орбитали использует ион цинка для связей ... Начинайте! (Помогают тому, кто сам что-то делает )
-
Начните с уравнений реакций, которые будут протекать при горении факела Далее надо рассчитать тепловой эффект каждой реакции, а для этого нужны табличные данные; энтальпии образования пропана, бутана, продуктов их сгорания А далее возникает задача определить состав смеси, по объемной доле и общей массе Начинайте! (Помогают тому, кто сам что-то делает )
-
Поглощают влагу из окружающего воздуха, образуя при этом капли концентрированного раствора, которые постепенно расплываются по поверхности.
-
У вас указано время полураспада t0,5 = 10,0 мин. т.е. за 10 мин распадается (вступает в реакцию) половина имеющегося вещества, его концентрация уменьшается вдвое. За 70 минут такое уменьшение произойдет 7 раз, и концентрация уменьшится в 2*2*2*2*2*2*2=27 = 128 раз Кинетическое уравнение я не использовал, для такого расчёта, считаю, в этом нет необходимости
-
Помоему, просто С70=С0/27; = 1/128 = 0,0078 M
-
Как то непонятно. Речь идет о массовой доле элемента кислорода, или о массовой доле простого вещества кислорода? Если в замкнутой системе идет реакция между веществами, то и общая масса остается неизменной, и масса каждого элемента. А значит постоянна и массовая доля элемента, и никакого отношения к выходу реакции она не имеет. Кстати для смеси СО - 0,55 О2 - 0,45 мольных долей массовая доля элемента кислорода изначально равна 77,85% Так и стоит написать в ответе.
-
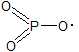
Ну оторвать, не оторвать, а взять в совместное пользование могут и берут: Каждый атом кислорода берет у атома фосфора в совместное пользование по два электрона и сам предоставляет в совместное пользование два электрона За счет этих 4-х электронов каждый атом кислорода образует двойную связь с атомом фосфора: Но вот незадача! У атома фосфора остался еще один неспаренный электрон! И его тоже желательно пристроить на какое-то общее электронное облако с другим атомом! И желающий находится - это еще один атом кислорода, у которого очень кстати тоже есть неспаренные электроны. В результате атом фосфора получает в совместное пользование еще одну электронную пару, образует еще одну связь: Но вот незадача! У атома кислорода то было два неспаренных электрона! И теперь он думает, куда бы ему пристроить оставшийся, и чтоб было это энергетически выгодно! И свет не без добрых частиц, готовых протянуть руку помощи с неспаренным электроном! Подвёртывается другой атом фосфора с таким электроном и в результате получается: , где все электроны спарены, и всё энергетически выгодно! Тут и сказочке конец, кто прочёл - тот молодец!
-
Мой ответ: 1,84 г
-
А как она потом детям будет помогать ДЗ по химии делать? Или хотите, чтобы они маму ни во что не ставили?
-
И то верно, зачем голову то нагружать? берем готовую формулу, подставляем какие-никакие циферки, переписываем на листочек закорючечки, которые выдает калькулятор и радуемся жизни.
-
Скорость прямой реакции определяется характеристиками исходных веществ, во всяком случае в том приближении, которое используется в учебных задачах.
-
Считайте, сколько моль хлорида натрия в вашей порции растертых таблеток и пишите уравнение реакции с нитратом серебра
-
Да будет вам придираться! Есть некие усредненные данные, которые используются для рассчетов. Есть некий средний человек, который потребляет некое среднее количество белков жиров и углеводов, в среднем спит и бодрствует столько то часов в сутки, и имеет средний доход и среднюю продолжительность жизни ... лет. На этом держится вся статистика. Ах, да! Это же буржюазная лже-наука.
-
Потому и надо узнать сколько метаналя прореагировало с оксидом серебра, чтобы потом по разнице найти сколько его прореагировало с водородом
-
Если вы в раствор NH4NO3 прильёте соляную кислоту, ничего подобного происходить не будет. И вообще никакой реакции не пойдет. Если вы твердый NH4NO3 начнёте прокаливать в атмосфере газообразного хлороводорода, то и здесь продуктами реакции скорее всего будет N2O + H2O, и хлороводород останется не причём, разве что поглотится образованной водой. Впрочем нагревание смеси N2O + HCl возможно приведет к указанным продуктам.
-
Второе уравнение правильное, если х и у количества вещества в исходной смеси А вот первое откуда такое взялось? У вас что, в 6.28 г смеси содержится суммарно 1,6 моль кислот? И хотелось бы начать с уравнения реакции с оксидом серебра Еще раз: у вас было 2,4 г метаналя. Он прореагировал частично с водородом Потом туда бухнули аммиачный раствор оксида серебра и выпал осадок. Сколько метаналя прореагировало с водородом? Это первый кусок задачи.
-
Показывайте, как у вас так - будет видно, где ошибка
-
Вот что-то очень сомневаюсь, что здесь пойдет какая-либо реакция, тем более с количественным выходом Но составитель задачи видимо предполагал, что пойдет А избыток метаналя полностью окислится оксидом серебра до СО2 и воды Отсюда де можно сделать вывод, сколько водорода выделили кислоты, и составить систему уравнений для нахождения их количеств. На бумаге все решаемо