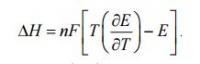Поиск
Показаны результаты для тегов 'Электрохимия'.
Найдено 71 результат
-
Коллеги, прошу совета по корректной интерпретации Mott–Schottky (MS) анализа для полупроводниковых материалов. Работаем с тонкими и толстоплёночными покрытиями (g-C₃N₄, TiO₂, гибридные системы) на FTO, измерения проводятся методом электрохимической импедансной спектроскопии с построением MS-графиков (1/C² vs E) в диапазоне частот ~2–10 кГц, с электродом сравнения Ag/AgCl. Возникают следующие вопросы: Как корректно выбирать «истинный» линейный участок MS-графика? Часто наблюдаются несколько квазилинейных областей при разных потенциалах. Правильно ли использовать только участок при достаточно большом обратном смещении, и какие визуальные/физические критерии указывают на область, соответствующую ёмкости области пространственного заряда, а не влиянию поверхностных состояний или слоя Гельмгольца? Какую роль играет частота измерений? Насколько корректно считать MS-анализ высокочастотным методом и при каких частотах вклад ёмкости Гельмгольца и поверхностных состояний можно пренебречь? Как интерпретировать частотную зависимость плоского потенциала? Подготовка и нанесение образцов для MS-анализа. Какие подходы считаются наиболее корректными для формирования воспроизводимых фотоэлектродов (drop-casting, doctor-blade, electrophoretic deposition)? Как критично влияют толщина плёнки, пористость, связующее (например, Nafion) и качество контакта с FTO на форму MS-графика и определение flat-band потенциала? Существуют ли практические критерии, позволяющие понять, что измеряется ёмкость полупроводника, а не межзерновые или контактные эффекты? Связь MS с другими методами: Как корректно сопоставлять результаты MS (flat-band, тип проводимости) с энергетическими уровнями, определяемыми методом XPS? Какие допущения обычно принимаются при таком сравнении?
- 3 ответа
-
- электрохимия
- измельчение
-
(и ещё 3 )
C тегом:
-
Здравствуйте! Долгое время пытаюсь найти константы устойчивости комплексных соединений рутения. Поделитесь опытом, если кто-то знает. Желательно, конечно, константы устойчивости всех возможных комплексов рутения. Но первостепенно, важен оксалат рутения (III). Заранее спасибо за интерес к данной теме и ответы!)
- 3 ответа
-
- химия
- электрохимия
- (и ещё 3 )
-
Здравствуйте, работаем уже много лет на трилонатном электролите кадмирования состав кадмий сернокислый 50-60 г/л трилон Б 85-100 г/л аммоний сернокислый 100-150г/л гидроксид натрия до 20 г/л закрепитель У-2 1,5-2 г/л рН 3.6-3.8 плотность тока 1-2 а/дм2 температура - 18-25 С в последнее время начались проблемы с кадмием, он плохо покрывает и блестящие осадки стали матовыми. также аноды в процессе электролиза пассивируются сильно. Анализы состава ванны в норме, не можем понять в чем проблема и как ее исправить, помогите, пожалуйста!
-
Чему равно количество использованного электричества (в числах "F"), если при электролизе водного раствора сульфата кобальта (CoSo4) с инертными электродами на катоде выделилось 118 г вещества. Какое это вещество? Что и в каком количестве выделилось на аноде?
-
- электролиз
- электрохимия
-
(и ещё 1 )
C тегом:
-
При прохождении тока последовательно через электролизёры, содержащие цианиды серебра и золота, в первом электролизёре на катоде выделилось 0,1079 г Ag, во втором – 0,0657 г Au. Вычислите: а) эквивалент золота; б) его валентность в соединении, подвергнутом электролизу.
-
- кулонометрия задачи
- кулонометрия
- (и ещё 4 )
-
рН-метр исследовательского класса практически даром - ниже себестоимости. мы купили его за 4000 евро в прошлом году Mettler Toledo. Новый в запечатанной коробке. рН-метр S80 SevenMulti - двух-модульный для проведения ион-селективных/рН/ОВП измерений. можем отдать в добрые руки за символические деньги для прибора этого класса. Описание: http://www.argentum107.ru/?m=prosp&an=AUB6 Сейчас снят с производства. Его замена S500 - от 500т.р.
- 1 ответ
-
- рн-метр
- кондуктометр
- (и ещё 8 )
-
Здравствуйте, очень нужна помощь. Дан электролиз раствора NaNO2, на выходе были получены NaNO3, NH3 и H2. Кто нибудь может помочь записать эту реакцию, заранее спасибо)
- 10 ответов
-
- электрохимия
- электролиз
-
(и ещё 1 )
C тегом:
-
Здравствуйте! У меня дана схема гальванического элемента: Ag/AgCl/LiCl//Fe(SO4)3,Fe(SO4)2/Pt и зависимость E=f(T) E=0.455+1.02*10^-3. Вот формула из которой выводят температурный коэффициент. Но дело в том, что значение энтальпии тоже нужно найти. Не могу понять откуда выразить этот коэффициент. А еще не счет реакций в этом элементе: Ag-e=Ag+, Fe3+ +3e=Fe, Fe2+ +2e=Fe ? Верно или нет?
-
1. Для получения 1 м3 хлора (н.у.) при электролизе водного раствора хлороводородной кислоты с угольными электродами было пропущено 8,75*10^6 Кл электричества. Вычислите выход по току (отношение массы или объема выделившегося вещества к теоретически возможным). Составьте уравнения электродных процессов. 2. Через два соединенных последовательно электролизера, содержащих, соответственно, водные растворы Na2SO4 и AgNO3, пропускали ток силой 10,0 А в течение 1 ч 40 мин. На какую величину увеличилась масса одного из электродов? Составьте уравнения всех катодных и анодных процессов, если электроды угольные. Помогите решить, или хотя бы задачи подобного рода помогите найти, не могу найти, а как решить не понимаю 2 задачи, одну понял как решать
-
Приведите схему электролиза раствора электролита для получения Н2 и О2. Какое количество электричества необходимо пропустить, чтобы получить 112 л Н2 (н.у.), если Вт=70%? Какой объем О2 выделится (н.у.)? Какое вещество подвергается разложению в электролите и какова его масса? Запишите уравнения анодно-катодных процессов и суммарное уравнение электролиза. Знаю как найти объем О2 и необходимое количество электричества, но возник вопрос: как понять какое вещество подвергается разложению и как рассчитать его массу? (Если через закон Фарадея, то какое количество электронов будет в этом случае?) Заранее спасибо за помощь.
-
Электрохимия. Свойства металлов. Помогите решить, пожалуйста:С
Fresmy опубликовал тема в Решение заданий
Составить схему коррозионного элемента с нарушенным покрытием во влажном воздухе. Основа - Ge ( ЕОGe2+ / Ge =+ 0,01 В ) Покрытие - As ( ЕОAs3+ / As = + 0,30 В ); он используется для облегчения пайки полупроводников. Указать толщину и тип покрытия. Хелп :С Хотя-бы навести на решение...-
- электрохимия
- металлы
-
(и ещё 1 )
C тегом:
-
Прошу помощи в решении задач по электрохими! 5. Растворимость сероводорода в воде при 293 К и давлении 101,3 кПа равна 2,58 м3 на 1 м3 Н2О. Рассчитайте массовую долю H2S в таком растворе. Определите, при каком давлении растворимость сероводорода в воде уменьшится в пять раз. 7. Теплота гидратации безводного цинка сульфата равна 95,27 кДж/моль. Определите изменение температуры при растворении 1 моля ZnSO4 в 400 моль воды, если энтальпия растворения 1 моля кристаллогидрата ZnSO4·7H2O в 400 моль воды равна -17,70 кДж/моль. Теплоемкость раствора цинка сульфата равна 4,19 Дж/г·К. 8. Рассчитайте понижение давления насыщенного пара над раствором, содержащим 36 г сахарозы С12Н22О11 в 540 г воды при 315 К, если давление насыщенного пара над водой при этой температуре равно 82 кПа. Определите осмотическое давление такого раствора, зная его плотность ρ = 1,01 г/мл. 9. Определите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,390С. 10. Докажите, какое вещество – камфару С10Н16О или нафталин С10Н8 – растворили в бензоле, если внесение 39 г этого вещества в 1000 г бензола привело к понижению Ткрист на 1,3 К. 11. В растворе бензойной кислоты НС7Н5О2 концентрация ионов водорода Сμ(Н+) = 3·10-3 моль/л. Определите молярную концентрацию этого раствора, если константа диссоциации кислоты kd = 6,14·10-5. 12. Вычислите активную концентрацию 0,005 М раствора алюминия сульфата, если коэффициенты активности Al3+ и SO42- соответственно равны 0,285 и 0,495, а плотность раствора ρ = 1,019 г/мл. 13. Вычислите ионную силу раствора, содержащего 1,59 г меди (2) сульфата CuSO4 и 0,44 г калия сульфата K2SO4 в 250 г воды. 14. Рассчитайте, в каком объеме насыщенного раствора ограниченно растворимой соли серебра ортофосфата содержится 0,15 г ионов серебра. 15. Определите, выпадет ли осадок магния оксалата MgC2O4, если к 0,1 л 0,01 М раствора Mg(NO3)2 прибавлено 0,4 л 0,001 н. раствора Na2C2O4. 16. Вычислите рН 0,01 М раствора аммония гидроксида и определите, как изменится величина водородного показателя, если раствор разбавить в 5 раз. 17. Рассчитайте рН раствора, содержащего в 500 мл воды смесь равных объемов 0,0005 М раствора НСl и 0,001 М раствора CaСl2. 18. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) серебра нитратом и калия хроматом; б) кадмия сульфатом и натрия сульфидом; в) соляной кислотой и цинка нитритом. 19. Составьте ионно-молекулярные уравнения гидролиза солей Na3PO4, CuSO4, Cr2S3 по всем возможным ступеням. Укажите реакцию среды полученных растворов. Напишите выражения и рассчитайте значения констант гидролиза этих соединений. Сделайте выводы по полученным величинам. 20. Вычислите рН и буферную ёмкость по отношению к HCl раствора, полученного при смешивании 1,2 л 1,2 М раствора уксусной кислоты и 0,6 л 0,6 М раствора натрия ацетата.
-
Оксидирование или анодирование нержавеющей стали
Dimka_nevedimka опубликовал тема в Неорганическая химия
Добрый день! Хотелось бы поинтересоваться был ли у кого опыт цветного оксидирования сталей. С черным металлом не возникает проблем, а вот с нержой не как не могу добиться подходящего результата. Сталь японский аналог 304, интересует только химическое или электрохимическое. Кто поделится опытом в данном вопросе, буду очень благодарен.- 1 ответ
-
- нержа
- оксидирование
-
(и ещё 2 )
C тегом:
-
Составьте схему процессов, происходящих при электролизе водного раствора KNO3 на медных электродах. Какая масса газа выделится на катоде при пропускании через раствор тока силой 12 А в течение 30 мин?
-
Рассчитайте ЭДС гальванического элемента, состоящего из стандартного водородного электрода и свинцового электрода, погружённого в раствор ацетата свинца с активностью а(Pb2+) = 1(моль/л) ,при Т = 298К. Составьте схему элемента. Напишите уравнения процессов, протекающих на электродах.
-
- эдс
- гальванический элемент
-
(и ещё 1 )
C тегом:
-
Открыта вакансия для исследователя в совместной лаборатории Института проблем химической физики Российской академии наук и Сколковского института науки и технологий Предполагаемое направление исследования: - Разработка литиевых и натриевых источников тока на основе органических электродных материалов. - Детальное электрохимическое исследование новых органических электродных материалов (преимущественно – катодных), конструирование лабораторных макетов литиевых (натриевых) источников тока на их основе и проведение стандартного набора испытаний. - Поиск и реализация новых подходов к конструированию гибких аккумуляторных батарей, обладающих большой емкостью и высокими скоростями заряда-разряда, что на сегодняшний день является одним из самых перспективных направлений исследований в области органической электроники. Условия работы: - Работа будет вестись в рамках уже поддержанного проекта Российского научного фонда в 2016-2018 г. с возможностью продления. - Исследования будут проводиться в Лаборатории функциональных материалов для электроники и медицины ИПХФ РАН (г. Черноголовка, Московская обл.)и в Центре электрохимического хранения энергии Сколковского института науки и технологий (Сколтех, Московская обл., г. Сколково) под непосредственным руководством в.н.с. П. А. Трошина (Pavel A.Troshin). - Лаборатории ИПХФ РАН и Сколтеха располагают комплексом современного оборудования для проведения исследований в области органической электроники. Имеющаяся приборная инфраструктура уникальна для нашей страны и в полной мере достаточна для решения задач проекта. - При успешном ходе работы исследователь может рассчитывать на компенсацию в размере ~ 46 000 руб. в месяц. Возможны другие выплаты (например, аспирантской стипендии, если человек поступает в аспирантуру). - Дружный, молодой и быстро развивающийся коллектив (средний возраст сотрудников лаборатории ~ 25 лет); Ожидаемые результаты (научные «бонусы», который получит исследователь за 3 года в ходе выполнения обозначенного проекта): - Публикации в ведущих международных научных журналах. - Патенты и ноу-хау. - Сотрудничество с российскими и зарубежными компаниями. - Представление результатов на престижных международных конференциях. - Для аспирантов – подготовка и защита кандидатской диссертации на самом высоком уровне. - Для кандидатов наук – создание весомого задела для будущей докторской диссертации. Требования к претендентам: - Заинтересованность в научно-исследовательской работе, готовность учиться и развиваться – обязательно; - Готовность уделять работе значительное количество времени – обязательно; - Приемлемый уровень знаний в области электрохимии и физической химии – обязательно; - Диплом специалиста или магистра со средним баллом выше 4.5 – весьма желательно; - Опыт работы с литиевыми источниками тока – весьма желательно; - Наличие публикаций – желательно; - Знание английского языка – желательно. Жилищные условия: Предоставляется общежитие в г. Черноголовка.При успешном развитии работ и при своевременном получении (наличии) степени кандидата наук есть возможность в течение нескольких лет получить служебную квартиру в рамках действующих жилищных программ РАН и ФАНО. Форма заявки: 1.Стандартное резюме (Curriculum Vitae) + список публикаций 2.Короткое обоснование, отвечающее на вопрос о том, почему претендент считает свою кандидатуру в полной мере соответствующей предлагаемой вакансии. Заявки и вопросы могут быть направлены по электронной почте gadomsky@rambler.ru с копией на адреса troshin2003@inbox.ru и P.Troshin@skoltech.ru
- 3 ответа
-
- электрохимия
- органические катоды
- (и ещё 2 )
-
Доброго дня химикам! У меня в процессе изучения курса электрохимии в медицинском университете возникли вопросы, ответить на которые самостоятельно я так и не смог — и потому надеюсь на помощьь компетентных пользователей этого форума. :-) 1. Известно что ионитовое стекло стеклянного электрода не пропускает ионы водорода насквозь, а лишь обменивает поверхностные катионы на ионы водорода раствора. Тогда каким образом в гальванической цепи, в которой одна фаза является не пропускающим заряды изолятором (стекло), вообще возникает ЭДС? Она же разомкнута. 2. Стеклянный электрод обменивает часть своих катионов на ионы водорода из раствора. Как при этом возникает разность потенциалов между поверхностями ионитового стекла, если в изначально лишенном потенциала стекле положительные частицы с одним плюсом обменивались на другие с тем же самым единственным плюсом? Буду особенно благодарен за ответ на пальцах в стиле "вот этот заряд пошел сюда, этот туда, в итоге стрелка прибора отклонилась".
- 6 ответов
-
- ионит
- стеклянный электрод
-
(и ещё 2 )
C тегом:
-
Составить гальванический элемент, используя в качестве анода магниевый электрод. Вычислить ЭДС в стандартных условиях, и ее величину при уменьшении концентрации ионов Men+ у катода до 0.01 моль/л.
- 1 ответ
-
- электрохимия
- эдс
-
(и ещё 1 )
C тегом:
-
электронные уравнения процессов, происходящих на электродах
Wreigy опубликовал тема в Решение заданий
уважаемые гуру. прошу помочь с тремя задачами из эликтролиза. или показать решение подобных. 1. Составьте электронные уравнения процессов, происходящих на электродах, при электролизе водных растворов электролитов с нерастворимым анодом. Напишите уравнения электролиза в молекулярном виде: ZnI2; Mg(NO3)2 2. Определите, какой металл является анодом, а какой - катодом в паре Al-Ni. Что происходит на пластинках при атмосферной коррозии и коррозии в кислой среде? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии? 3. Магниевый электрод в растворе своей соли имеет потенциал -2,410 В. Электродный потенциал платинового электрода в растворе своей соли будет на 0,020 В меньше его стандартного электродного потенциала. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, составленного из магниевого и платинового электродов, опущенных в растворы своих солей.