-
Постов
1952 -
Зарегистрирован
-
Победитель дней
2
Тип контента
Профили
Форумы
События
Сообщения, опубликованные terri
-
-
Доброго времени суток!
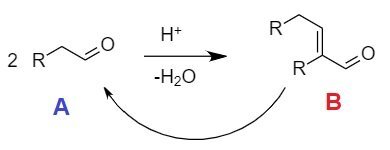
В реакции получаю альдегид (А). Он вроде и получается, но как-то активно начинает сам с собой реагировать,
образуя продукт конденсации (В).
Помогите, пожалуйста, советом, как можно из В снова получить А, если это, конечно, возможно.
спасибо !
-
 Всякое мохбыть имеет право быть проверенным. Спасибо!
Всякое мохбыть имеет право быть проверенным. Спасибо!
А вот с ледяной не поняла. Она сделает устойчивым бензиловый альдегид?
-
В 26.04.2022 в 20:07, yatcheh сказал:
Пербензойной кислотой бензиловый спирт не окисляется. Даже бензгидрол не окисляется. А вот альдегиды - на ура.
Походу, перкислотами спирты вообще окисляются намного медленнее альдегидов, поэтому сомнительно, что удастся остановить процесс на стадии альдегида.
А я не хочу пербензойной, у меня надуксусная, которая окисляет изопропанол. А какие спирты окисляются легче - вторичные или первичные?
Да, согласна-согласна, что альдегид быстрее окислится в кислоту, чем спирт в альдегид. Может, тогда альдегид связывать в серную соль?
Или может быть, что окисление альдегида в кислоту будет затруднительно в неводной среде?
-
Нет, куча способов не нужна, нужно проверить окислительные свойства надуксусной кислоты.
Изопропанол окислился при нормальной температуре, но там нет побочки.
С бензиловым спиртом, может, поможет температуру еще и понизить,
чтобы до бензойной кислоты дело не дошло?
-
Доброго времени суток!
Практика показала, что с помощью надуксусной кислоты можно довольно удачно окислить изопропанол на ацетон.
Как вы думаете, можно ли таким способом окислить бензиловый спирт на альдегид без того,
чтобы реакция окисления пошла на бензойную кислоту?
Интересно ваше мнение. Спасибо!
-
2 часа назад, stearan сказал:
получается, Ваша достигнутая конверсия (и, соответственно, константа) заметно превосходит оных 0.37

Вот это да!?
Это я так здорово промахнулась со своими 0.03?!?
-
Доброго времени суток!
Работаю с гидроперитом в изопропаноле при 37°C и меня начинают мучать сомнения,
что не вся перекись водорода из гидроперита идет на окисление субстрата, а по дороге к этому окислению
перекись просто разваливается на воду и кислород, видимо, молекулярный, который уже ничего не окисляет.
Возможно такое? И как это проверить?
Оставить, к примеру, гидроперит в среде изопропанола буз субстрата и проверить содержание воды через какое-то время?
Спасибо!
-
1 час назад, stearan сказал:
к 1) возможно константа 0.37 была определена для реакции уксусной кислоты с каким-нибудь реально-безопасным для работы раствором перекиси водорода, напр. 50% (или и того менее), тогда цифры из-за содержания воды будут другими.
У меня были такие исходные данные: 60 мл ледяной уксусной кислоты и 97 мл 35% перекиси водорода.
Вроде 1 моль уксусной и 1 моль перекиси в одном неизменном объеме, концентрации ведь в формуле в (моль/л).
Вот у меня получилось 0,03. Не правильно? ?
-
4 часа назад, popoveo сказал:
1. Верно.
2. Да, в щелочном растворе произойдет нейтрализация кислот, но ацетат-анион никуда не денется и будет окисляться до пероксоацетат-аниона, который в присутствии OH- более устойчив.
Т.е. будут соли надуксусной кислоты, которые сами по себе распадаются гораздо медленнее кислоты.
1. Вот смотрите, подставляю свои значения из опыта: смешала по 1 молю уксусной кислоты и перекиси водорода.
Конверсия уксусной на надуксусную была 15%. И вот мой расчет константы равновесия:
К=(0,15)(0,15)/[0,85)(0,85)]=0,03
Вот вместо Ваших 0,37 у меня на порядок меньше получилось. Не могу понять, почему.
У Вас достоверный источник по 0,37?
2. Если я Вас правильно понимаю, устойчивость надуксусной кислоты тесно связана с рН раствора, где она находится?
И чем рН выше, тем она устойчивее? ... причем при достаточно высоких значениях рН речь уже об устойчивости пероксоацетата.
-
15 часов назад, Arkadiy сказал:
реакция экзотермическая, лейте медленно
C ацетангидридом понятно, что его буду медленно приливать к гидропериту.
А как с фталиевым ангидридом? Смешать два кристаллических вещества и согреть?
3 часа назад, popoveo сказал:При 4 °C период полураспада надуксусной кислоты составляет несколько месяцев, при 40 °C он сокращается до одной недели.
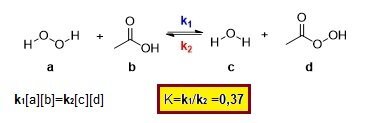
Константа равновесия реакции H2O2 + CH3COOH <=> H2O + CH3C(O)OOH равна 0.37.
Равновесие сильно сместится вправо в щелочном растворе.
Добавьте сюда разложение при н.у. и картина станет совсем ясна.
Вот смотрите рисунок. Пока верно?
В щелочном растворе ведь произойдет нейтрализация кислот (уксусной и надуксосной).
Вы имеете ввиду частичную нейтрализацию?
-
10 часов назад, popoveo сказал:
Я же написал, что в случае щелочной среды
1. Нет, она в принципе неустойчива при н.у.
2. Равновесие будет смещено в сторону ее разложения.
1. Вот как в принципе? Если смешать при н.у. уксусную и перекись водорода, то через сутки надуксусной в смеси будет около 10%. Возможно, она устойчива в присутствии уксусной?
С другой стороны, надуксусная живет и здравствует при 37 градусах, когда ее образует энзим, но тут содержание надуксусной не больше 3%. Возможно, она в таком разбавлении устойчива?
2. Вот с этим равновесием не знаю. Если ацетангидрид прореагирует с гидроперитом и возникнет надуксусная и уксусная, может надуксусная в присутствии уксусной, мочевины, действительно, достигнет какого-то максимума, а что будет над, то разложится. Но, видимо, это можно определить только экспериментально.
-
19 часов назад, Arkadiy сказал:
Естественно. Если слишком нагреете, то реакция пойдет бурно и все это может вскипеть и плюнуть!
Хочу при 37 градусах попробовать.
Еще не плюнет?

-
30 минут назад, Arkadiy сказал:
Может и так.
Ангидриды весьма активны их активность к аминам и спиртам выше, чем к воде
Это активность будет повышаться с температурой?
-
47 минут назад, Arkadiy сказал:
Все зависит от соотношения, но вы получите смесь спирта, этилацетата, уксусной и надуксусной кислот ...
Реакции могут идти все, а не те, которые вам нравятся.
Спирт зачем? Сначала получите надкислоту, а потом лейте спирт
Идея! Спасибо!
т.е. смешать ацетангидрид и гидроперит, а только потом ... может, вообще спирт не лить, а сразу субстрат?
-
В 17.04.2022 в 17:33, popoveo сказал:
Потому что неустойчива.
Именно в изопропаноле неустойчивая?
23 часа назад, Arkadiy сказал:ангидрид со спиртом в первую очередь даст эфир, в случае фталевого ангидрида -кислый
Одним словом, надуксусная не будет образовываться ?
-
-
В 14.04.2022 в 19:06, BritishPetroleum сказал:
Синтез диэтилмалоната включает в себя щелочной гидролиз соли нитрила малоновой кислоты...
Я тоже за этерификацию, но не с HCl, а с pTSA с избытком спирта. А этанол - да, подсушить азеотропической дистилляцией с чемнить, что под рукой.
-
В 15.04.2022 в 07:21, popoveo сказал:
Есть только предположение, что надуксусная кислота будет разваливаться, а вот пероксоароматическая будет жить.
А можно уточняющий вопрос?

Почему надуксусная будет разваливаться?
-
Доброго времени суток!
Есть система изопропанола и гидроперита, в которую добавляется ангидрид с целью получить надкислоту.
В первую систему добавляют ацетангидрид, а во вторую - фталиевый ангидрид.
И вот интересно узнать, где этот процес образования надкислоты пойдет (и пойдет ли?) быстрее. Спасибо!
-
15 часов назад, stearan сказал:
это наверно всем известно, но на всякий случай...
А конкретной методики у Вас нет случайно?
-
Посмотрите в Вики для каждого из соединеий, в чем они растворяются/не растворяются.
Может быть такая ситуация, что что-то растворяется в воде, что-то нет.
Всю найденную информацию пишите сюда, будем разбираться вместе.

Вам же важно научиться, верно?!
-
21 час назад, yatcheh сказал:
А этот узкий интервал рН устанавливается экспериментально? ?
Бисульфитное соединение - это типа соли сульфоновой кислоты?
22 часа назад, BritishPetroleum сказал:Бисульфитное соединение будет где у углерода все связи насыщены, конденсироваться он не может уже
Да, было бы чудесно, если бы это работало.

Но есть такой ньюанс, что альдегид получается при температуре около 100-105°C.
Бисульфитное соединение выдержит такую температуру?
-
1 час назад, yatcheh сказал:
Ингибиторы - сомнительно. Не представляю себе механизм такого ингибирования. Замедлить реакцию можно, повышая pH среды до нейтрального. Но это же другое. А исключить нежелательную реакцию можно, защищая группу. Подумать только - как...
Продукт - альдегид, он в кислой среде образуется.
Вот, может, идея - не придавать сразу всю кислоту, а только половину необходимого количества.
Спасибо! Навели на эту идею.
 11 минут назад, BritishPetroleum сказал:
11 минут назад, BritishPetroleum сказал:Мб ещё бисульфит натрия? Он притянет к себе альдегиды, в кислой среде и не будет конденсации никакой
Притянет, в смысле что-то ввиде аддукта будет образовываться?
Надо подумать.
Система, где идет реакция, - двухфазная, а альдегид не растворим в воде.
-
Доброго времени суток!
Не подскажите, как можно предотвратить такую конденсацию альегидов в кислой среде,
существуют ли какие-нибудь специфические ингибиторы? Спасибо!


Бензиловый спирт в альдегид
в Органическая химия
Опубликовано
Понятно! ... т.е. окисление надо вести в избытке ледяной уксусной.
А как потом снова к альдегиду вернуться после окисления?