
Angry_Biotechnologist
-
Постов
285 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Angry_Biotechnologist
-
-
11 часов назад, Arkadiy сказал:
БедныЙ! Как тебя угораздило!
НИЧЕГО НЕ будет! , прокашлялись и забыли про химию - это не ваше
Спасибо за ответ.
Химию не брошу
 уже было что дышал хлором и водородом, но не было настолько сильной реакции организма. Плюс читая все инструкции по безопасности и вреде диоксида, признаюсь чесно - немного перепугался. Вот и спрашиваю тут, у более опытных людей, если написаное имеет смысл в моем случае.
уже было что дышал хлором и водородом, но не было настолько сильной реакции организма. Плюс читая все инструкции по безопасности и вреде диоксида, признаюсь чесно - немного перепугался. Вот и спрашиваю тут, у более опытных людей, если написаное имеет смысл в моем случае.
-
Спасибо за ответ!
Тоесть прокашлялся и забыл?
Я думал муколтические попить чтобы вывести мокроту с легких - есть ли смысл?
-
Добрый день,
2 дня назад, по собственной тупости, случайно вдохнул диоксид азота. Секунд 10-20 сильно прокашлялся. Вчера бул приступ кашля на 1-2 мин. Сегодня уже лучше, но ощущение как будто лёгкую простуду схватил. Скорее всего пойду к доктору.
Воопрос: у кого был подобный опыт? Как лечили? Долго ли?
Заранее спасибо
-
03.05.2020 в 02:33, M_GM сказал:
По закону Бугера-Ламберта-Бера: А= ЕСl
Если у аденина С= х, а у гуанина С= у,, то
А245= 8050хl + 10900yl = 0.488 и
А262= 13300хl + 7580yl = 0.493
Два уравнения с двумя неизвестными,
но вот как-то не хватает еще величины l, длины кюветы в которой проводились измерения адсорбцииМожет порыться еще в условии задачи?
Спасибо Вам большое за ответ, длина кюветы 1см.
Если у Вас есть минута взглянуть на вот эту публикацию, страница 765, авторы дают формулы для концентрации аденина и гуанина, которые они каким-то образом выводят из тех формул что Вы написали. Я не могу понять почему они делят на 84е6

Еще раз очень признателен

-
Доброго времени суток :)
Возникла проблема с решением вот такой вот задачки:
Сколько моль/л аденина и гуанина в смеси этих 2х нуклеотидов, учитывая что абсорбция А245=0.488 и А262=0.493
Коэффициент молярной экстинкции аденина Е245=8050М/см Е262=13300М/см
Коэффициент молярной экстинкции гуанина Е245=10900М/см Е262=7580М/см
Я только то и понимаю что абсорбция у аденина лучше в 262нм, а гуанина в 245нм
Очень признателен за какую-угодно помощь!
Спасибо за внимание
-
1 час назад, Аль де Баран сказал:
По стандартной методике заместо фенолфталеина в эту реакцию берут нитрат ртути или, на худой конец, серебра.
Подскажите пожалуйста название реакции, во имя науки и просвещения

-
Добрый день!
При смешивании спирта 96%с маленьким количеством фенолфталеина и HNO3(ч) произошло следуюшее:
1) Активное выделение диокиси азота (коричневые пары с хлористым запахом), соответсвенно бурление самого розтвора.
2) Розтвор изменил цвет сначала на желтоватый потом на зеленаво-синий и вконце перешел на зеленый
3) После охлаждения в воде, образовался осадок (белый), который постепенно осел. цвет все ещё был зеленкавый (вместе с осадком все это имело вид эдакого лимонада =D, уж извините за аналогии).
4) После осаждения осадка я слил всю жидкость и налил сверху свежей воды дистилированой. Через полчаса вода стала золотисто-желтой, осадок не растворился.
5) Я слил желтый "обмывок" и попробовал растворить осадок в спирте - растворимость крайне хорошая. В дословно 2мл спирта растворилось все практически мгновенно (я только помешать успел где-то секунд 20).
Я попробовал повторить реакцию. Но результат нулевой. Подозреваю что какая-то посуда була грязной.
Подскажите что могло произойти?
Заранее спасибо!
-
1 час назад, ALLOE сказал:
На ком практиковаться собрался, убивец!
хах, не не не, никаких опытов на живых существах. Биоэтика и все такое =D Практика самого синтеза канэшна!
Ну а если мы уже затронули тему практического применения, то какие основные угрозы могут быть со стороны вот такого, хенд-мейд продукта?
-
А есть у кого руководство провереное как аспирин изготовлять? (очевидно употреблять я его не рискну, но для практики можно)
-
9 минут назад, Nemo_78 сказал:
Попробуйте вот здесь почитать https://www.yandex.ru/search/touch/?lr=15&text=предельные+структуры+азотной+кислоты&suggest_reqid=25276701944892271909481557232712
Там сразу в первой ссылке pdf-овский файл со школьным(углубленным) изложением спрашиваемого Вами.
. С уважением
Ооо спасибо! Я пробовал искать да как-то не те слова вписывал поисковые или что-то в том роде.
Если Вас это не затруднит, могли бы Вы глянуть на фото которое я на imgur разместил? Просто скажите что из этого неправильно. Вы очень поможете.
-
1 минуту назад, Nemo_78 сказал:
. Откуда в азоте sp3d-гибридизация-то возьмётся, если на втором энергетическом уровне (азот - элемент второго периода ПСХЭ) d-орбитали нет и в помине?!
. С уважением
Ну вот собствено то для этого и пишу :D самообразование штука такая, подлая.
Тогда заполнятся будет 3s? Должно быть 5 валентных електронов же ж.
-
-
Медь не реагирует с соляной кислотой, тоесть в реакцию пойдет только цинк.
Zn + 2HCl ----> ZnCl2 + H2↑
H2 + CuO ----t°---> Cu + H2O
Мы знаем что воды выделилось 4.5 грамма (отсюда и потеря масы- вода испаряется). А 4.5 грамма воды это 0.25 моля. Из чего делаем заключение что столько же было и водорода, а если водорода тоже было 0.25 моля то и цинка в самом начале у нас было 0.25 моля.
Из выше сказаного:
масса цинка в добавленой порции латуни 16.34гр, что составляет примерно 31% и маса меди 36.65гр что составляет примерно 69%.
-
 1
1
-
-
Добрый день,
Заранее прошу меня извинить за то что это второй пост про гибридизацию и то что нужно смотреть на мои каракули
 Но это тема которую я благополучно забросил дважды, но теперь хочу её понять.
Но это тема которую я благополучно забросил дважды, но теперь хочу её понять.
Альзо, подскажите пожалуйста как изобразить координационую связь (или резонанс) в азотной кислоте? И тип гибридизации у азотной кислоты sp3d?
Прошу вас также глянуть на эти орбитальные структуры которые я написал. Форма не всегда соответствует на рисунке, но я её выделял отдельным пунктом (справа, выше от рисунков).
АХЕ таблица с которой я брал информацию относительно формы молекулы.
Буду очень признателен если вы уделите этому время

Заранее благодарен
-
30 минут назад, M_GM сказал:
У кислорода в ОН-группах sp3, т.к. кроме двух сигма-связей есть еще две электронные пары
У серы тоже sp3, т.к. образует 4 сигма-связи с четырьмя атомами кислорода. Пи-связи на гибридизацию не влияют.
И да, окружение серы примерно тетраэдрическое
Огромное спасибо! Разрешите только поинтересоватся с какой литературы вы взяли изображение?

Я сам сейчас подтягиваю школьную химию (уже пора) то мне бы пригодилось что-нибудь о гибридизации
-
Добрый день,
Пробую нарисовать как бы могла выглядеть структура сульфатной кислоты.
Выходит так что на ОН группах у меня SP2 гибридизация (из-за наличия Н атомов). П связь я провел от p орбиталей сульфура и кислорода (который должен иметь 2 выше упомянутых орбитали с 1 ел на каждой).
Форма тетраэдра.
Скорее всего это ересь :/ но я надеюсь вы сможете подсказать что не так
заранее спасибо!
-
В 08.10.2018 в 23:07, aversun сказал:
Возможна, железо окислится ло +3, а Mn восстановится до +2
23 часа назад, LegendXumuk сказал:автор не уточнял, что именно ему необходимо в полуреакциях. А мы писали так. А насчет того что первым окисляется железо, не согласен. Хлор более активен и при диссоциации в растворе эти реакции идут либо параллельно, либо первым окисляется хлор.
И вообще у меня эта самая реакция есть в лабнике. С наблюдением. Я бы не стал говорить того, чего не видел...22 часа назад, Аль де Баран сказал:Уравнения ОВР пишутся для стехиометрических соотношений веществ. Если у вас выделялся хлор, то это значит, что вы вбухали туда немеряное количество марганцовки. В таких условиях хлор будет выделятся из любого хлорида, да хоть из простой соли. Измените условия проведения реакции, постепенно добавляйте к подкисленному раствору хлорида железа(II) раствор марганцовки при перемешивании, и будет вам счастье.
ОГРОМНОЕ человеческое спасибо, тоесть будет что-то типа:
6KMnO4 + 24H2SO4 + 30FeCl2 ----> 6MnSO4 + 3K2SO4 + 20FeCl3 + 5Fe2(SO4)3 + 24H2O ?
в полуреакции не смог =( просто прикинул что для баланса FeCl2 и FeCl3 вместе с Fe2(SO4)3 нужно 30 молекул того самого FeCl2 (сначала ринулся было в 15, но с железом были проблемы). А если нужно 30 молекул ферум 2 хлорида то соответсвенно во время окисления будет выделено 30е. Ну а я знаю что количество "выделеных" и "взятых" (тобиш електроны с окисления и востановления) должно быть одинаковым. Вот и вышло у меня что нужно 6 молекул марганцовки что-бы было 30е.
-
 1
1
-
-
Добрый день,
Возможна ли такая реакция?
2KMnO4 + 3H2SO4 +FeCl2 -->
Если да, то, пожалуйста, как её расписать
Заранее благодарен
-
Добрый день!
Вот не могу понять что не так с Mn2O5. Имеется ввиду что его не можна купить (из чего я делаю поспешный вывод что его несуществует в стабильной форме). Но при этом есть всякие pubchem"ы где про него пишут.
Можете сказать существует ли это вообще? Если да то где?
Заранее спасибо
-
рН при разбавлении посчитать думаю
и как этим воспользоватся потом? Это должна быть определенная кислотность в которой данная соль растворяется?
-
-
Тоесть уравнение само по себе должно выглядеть так: pH=pKa - log(соль/кислота)? //Нет
А разве х у вас соль?
В этой паре, NaH2PO4 выполняет роль кислоты, Na2HPO4 роль соли.
Поэтому у вас формула pH=pKa - log(кислота/соль) и поэтому знак минус
Почему Хассельбаха иногда пишут с +лог а иногда с -лог?
А вот если под логарифмом стоит (соль/кислота) тогда надо писать +
Очень Вам признателен!
-
То есть вы не видите функции "логарифм" в своем решении?
И не видите какой знак перед ней стоит?
Поменяйте его на "минус"
После чего ищите заново х
Тоесть уравнение само по себе должно выглядеть так: pH=pKa - log(соль/кислота)?
10^0.2=10^(-log(x/0.1-x))
1.5848=1/(x/0.1-x) | x (x/0.1-x)
1.5848x/0.1-x = 1 |x (0.1-x)
1.5848x = 0.1-x
2.5848x=0.1
х= 0.03868
магия... Спасибо! Но последний воопрос к Вам
Почему Хассельбаха иногда пишут с +лог а иногда с -лог?
-
Хорошо бы поставить "минус" перед логарифмом,
а то получается, чем больше кислоты, тем выше рН

Извините не понимаю про что вы говорите?

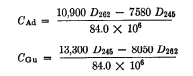

Диоксид азота
в Токсикологическая химия
Опубликовано
Тоже удушило немного, чучуть горло продрало, но прошло быстро (буквально через час-два уже было все в порядке). dmr правильно предположил.