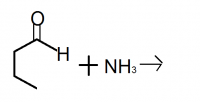Поиск
Показаны результаты для тегов 'Аммиак'.
Найдено 52 результата
-
Появилась идея однокомпонентного ЖРТ: 3H2O2*2NH3*H2O→N2+7H2O Подкупает мизерная молярная масса и отсутствие сажи, но возникают вопросы: 0) Как повлияет аммиак на разложение перекиси при хранении? 1) Будет ли реагировать перекись с аммиаком при длительном хранении? 2) Не долбанёт ли? 3) Как поведёт себя серебряный катализатор перед соплом?
-
Есть соединение: полиакрилат натрия, которое способно абсорбировать воду в 200-300 раз больше собственной массы. А есть ли вещества, спобобные абсорбировать или образовывать не слишком устойчивые комплексы с аммиаком? Цель: использовать твёрдое или жидкое вещество в к качестве источника аммиака.
-
Выбор между CuSO4 и ZnSO4 при реакции с NH3 в растворе
Misha20062006 опубликовал тема в Решение заданий
В двух колбах находились бесцветные растворы веществ X и Y. В обе колбы добавили избыток водного раствора аммиака. В колбе с веществом X осадок сначала выпал, а затем растворился, а в колбе с веществом Y осадок выпал и не растворился в избытке реагента. Из предложенного перечня выберите вещества X и Y, которые обладают описанными свойствами. CuSO4 H2SO4 ZnSO4 Fe2(SO4)3 K2SO4 При решении этого задания у меня возник вопрос, почему правильным ответом считается 34. То есть как вещество X взят именно ZnSO4. Почему не подходит CuSO4. Видел похожую тему на этом форуме, где человек прописал эти реакции. Они идентичны, но тогда почему не подходит CuSO4? > -
1.4Рассчитайте состав газовой смеси, выходящей из контактного аппарата. Селективность окисления аммиака до оксида азота(II) составляет 98% (остальной аммиак окисляется до N2). Содержание аммиака в аммиачно-воздушной смеси составляет 11.5% (по объему).
-
- аммиак
- оксид азота
-
(и ещё 1 )
C тегом:
-
Привет, подскажите, пожалуйста, может ли окислить сернистый газ аммиак. идет ли подобная овр реакция? Заранее спасибо
- 3 ответа
-
- аммиак
- сернистый газ
-
(и ещё 1 )
C тегом:
-
Будет ли эффективна реакция CO(NH2)2 + H2O + CaO ---> CaCO3 + 2NH3 при нагревании, или с неким катализатором?
-
Здравствуйте. 1. При добавлении в 'известковое молоко' сульфата аммония изменится ли как-то равновесие в сторону образования аммиака? Ca(OH)2 + (NH4)2SO4 -> ? -> CaSO4 + NH4OH ? Растворимость в воде извести и гипса примерно одинаковы. Известна комплексная соль аммоний-кальций сульфат, также малорастворима. Аммиакаты кальция в водном растворе вроде не существуют. 2. При нагревании сухой смеси CaO с сульфатом аммония какая реакция начнется и при какой температуре? 3. При нагревании Ca(OH)2 с сульфатом аммония? Заранее спасибо за ответы.
-
Здравствуйте, уважаемые химики! Простите, заранее прошу, мой непрофессионализм. Вопрос уже поднимался на этом форуме, но спрашивающий напустил туману, поэтому ничего не понятно. Вопрос: в сети появилась информация, что смешав каким то образом ацетат серебра с аммиаком, можно получить прозрачную чистую жидкость малой вязкости, которую можно залить в струйный принтер и распечатать проводники. После нагрева до 90 градусов это вещество восстанавливается до серебра и мы получаем токопроводящий слой. Возможно ли это с точки зрения химии? Или, может быть, существует другой способ восстановить серебро, не прибегая к воздействию высоких температур? Или не серебро, а медь, к примеру? Дорожки печатаются на пластик, который не выдержит нагрев более 100 градусов. Поскольку в принтере несколько раздельных картриджей, то возможно использование 2ух или более компонентных составов, чтобы реакция не проходила в чернилах до печати. Компоненты, по идее, будут перемешиваться непосредственно при печати, как цвета при цветной печати. В идеальном случае, это позволит печатать токопроводящие дорожки с высоким разрешением, поскольку отсутствуют частицы серебра в чернилах. Чернила на основе серебряной пыли уже есть, но они не позволяют добиться высокого качества, из-за размера частиц, образования агломераций, выпадения в осадок, низкого сопротивления и необходимости отжига для сплавления частиц пыли. Извините, что длинно, просто ужасно интересно. Спасибо заранее всем заинтересовавшимся!
- 60 ответов
-
- ацетат серебра
- аммиак
-
(и ещё 1 )
C тегом:
-
Пару дней назад провёл эксперимент с новокаином. Новокаин - это местный анестетик, который выпускается в форме раствора для инъекций в концентрации 0.5%. Именно такой у меня нашёлся в ампулах по 6 мл. Действующее вещество называется прокаин (procaine). Вскрыл ампулу и перелил шприцем 3 мл 0.5% раствора новокаина в пробирку. Добавил 2 мл аммиака водного 10%. На этом шаге никаких видимых признаков реакции не обнаружил. Стал добавлять спиртовую настойку йода 5% по каплям. Первая же капля дала образование чёрного вещества (трийодид азота) в месте своего падения. Чернота стала растекаться сверху вниз пробирки, но осадка не образовала. По мере распространения чернота обесцветилась. То же самое происходило и со следующими каплями. После добавления 3-4 капель можно было наблюдать очень слабое зеленоватое окрашивание. Ни черноты, ни йодной желтизны не было. Из этого я сделал вывод о том, что трийодид азота реагирует с новокаином при комнатной температуре в среде водного раствора аммиака. Хотелось бы знать, какие вещества образуются в проделанном эксперименте и могут ли они иметь какое-либо фармакологическое значение.
- 7 ответов
-
- прокаин
- трийодид азота
-
(и ещё 1 )
C тегом:
-
Добрый день! Можно ли хранить 25% ра-р аммиака на одной полке с парящими и летучими кислотами (соляная, азотная, уксусная, бромистоводородная и т.п.). Не будет ли налета на банках? Могу резьбу обмотать ФУМ-лентой если что...
-
Здраствуйте! Нужна помощь. Прочитал в интернете способ чистки монет из алюминиевой бронзы: окунуть в NH4OH на 15-20 минут, потом чистить с содой. Решил испробовать сначала на монетах из латуни - всё прошло удачно. Потом окунул в аммиак монеты из алюминиевой бронзы (украинские), закрыл крышкой, через 15 мин вытащил из раствора и положил в воду с расчётом сейчас же отмыть от аммиака и высушить, но отвлёкся на другое дело и забыл о них. В результате имею 2 тёмные монеты, которые окислила вода. Я решил их опять окунуть в аммиак, но это ничего не дало. Но на этом история не закончилась. Ещё 2 монеты я передержал в аммиаке (да, я забывчивый такой...) - в результате аммиак окрасился в тёмно-синий цвет, а монеты сильно потемнели (тоже с синим оттенком), водой не отмывается. Использовал нашатырный спирт 10% из аптеки. Накрывал его крышкой, чтобы не испарился весь. Как я понимаю суть реакций: аммиак восстанавливает оксиды алюминия и меди до чистых металов, не защищённых оксидной плёнкой, поэтому они быстро прореагировали с водой, но почему монеты почернели? Я так понимаю, что оксид и гидроксид алюминия светлые, а медь вообще не должна реагировать с водой. Вообще-то я окунал монеты сначала в воду перед сушкой, так как они на воздухе быстро чернеют, если на них есть капли раствора аммиака. Но чернота, образованная на воздухе, с лёгкостью снова востанавливается аммиаком, а чернота, образованная в воде - не восстанавливается. В чём разница? Каким образом аммиак реагирует с алюминием или медью, что раствор окрашивается в синий цвет, а на самих монетах остаётся несмываемый тёмно-синий налёт? Неужели здесь проявляется амфотерность алюминия? Зачем использовать соду для чистки? Она нужна только как абразив или нужны её щелочные свойства? Всё это произошло вчера, на сегодня монеты не изменили свой цвет сами. Поэтому вопрос: как восстановить золотистый цвет монет? Но не надо мне отвечать: не парся, вибрось, оно того не стоит. Я знаю точно: оно стоит того.
-
В колбу с 95% этанолом и Al2O3 будет поступать аммиак по газоотводной трубке из колбы, в которой примерно 10% раствор аммиака, а он в свою очередь нагревается. Получается ли этиламин?
-
Требуется провести две реакции, что из этого получится, есть ли обоатный ход реакции? NH3×AgCl NH3×HCl ПОМОГИТЕ.
-
Известен также способ отбелки бумаги перекисью водорода в смеси этилового спирта и воды в соотношении 1:1. Щелочную среду отбеливающего раствора создают добавлением аммиака. Помогите разобраться. Что значит 1:1 - вода : спирт, или 1:1 - перекись водорода : спирт, ил все три компонента поровну, все по одной части смешивать? Полученный раствор будет кислым? И в него надо добавить еще четвертый компонент - аммиак? Нужно удалить пятна от плесени, они темно серые и желтые. Бумага акварельная.
- 11 ответов
-
- реставрация графики
- аммиак
- (и ещё 3 )
-
Очень интересен процесс диссоциации, есть ли конкретные сведения об этом процессе?
-
Делаем на лабораторной ксантопротеиновую р-цию с белком, все нормально, добавляется азотная к-та, появляется желтое окрашивание, но потом добавляем не NaOH (как в примере) а аммиак... Подскажите, пожалуйста, что должно получиться, какой окрас и как реакция пойдет
- 4 ответа
-
- цветные реакции
- белки
-
(и ещё 1 )
C тегом:
-
Как пропитать циолит для нейтрализации аммиака и мочевины?
tima25 опубликовал тема в Решение заданий
Здравствуйте. Мы производим биотуалеты для кошек. В один из компонентов сборки природный Циолит фракция 3-6 мм. Подскажите чем пропитать Циолит для нейтрализации аммиака и мочевины. Безопасным для питомца и доступным $. Можно запатентовать. -
Определение хлора в аммиаке. Уточнение формулы ГОСТа
aschegoleva опубликовал тема в Аналитическая химия
Добрый день, коллеги. Уделите, пожалуйста, несколько минут своего времени. Тема вопроса связана методикой определения общего хлора в жидком аммиаке визуально-нефелометрическим методом, предлагаемой ГОСТ 28326.6-89. Принцип, в общем-то, стандартный: подготавливаем пробу, готовим раствор сравнения, помещаем в идентичные пробирки и добиваемся одинаковой мутности растворов. Ничего, казалось бы, сложного. Однако вопрос возник с расчетной формулой, которую нам предлагает ГОСТ. Из рассчитанной массовой доли хлоридов в анализируемой пробе (мг/кг) вычитается загадочное число 0,2, которое расшифровывается как поправка, учитывающая массу общего хлора в растворе сравнения (мг/кг) И вот мы сидим и всей лабораторией думаем, кого же они вычитают и зачем, если необходимо, чтобы доля хлоридов в анализируемом растворе и растворе сравнения была одинаковой. Никаких затравок и холостых проб тут не обнаруживается. Будем весьма признательны, если подскажете, что же мы здесь не учитываем. Ссылка на ГОСТ: http://docs.cntd.ru/document/1200021027 -
К 30 дм3 смеси ,состоящей из пропана и аммиака,добавили 10 дм3 хлороводорода.После приведения новой газовой смеси к первоначальным условиям ее относительная плотность по воздуху составила 0.79.Укажите массовую долю пропана в исходной смеси.(Все объёмы измеряли при Т=20С Р=10^5 Па) NH3+HCl=NH4Cl M(смеси)= 22,91 г/моль ...?
-
Подскажите, что получится в реакции P.S. Надеюсь, это именно бутаналь? Еще не привыкла к такой записи...
-
Доброго дня всем. Есть технология химического "морения" древесины. Там всё вроде просто. В закрытую ёмкость помещают древесную заготовку и вату пропитанную нашатырём (10%). Но я нашёл более старую технологию, в которой предлагалось вместо 10% нашатыря добавлять истолченный известняк и сернокислый аммоний. Этой "технологии" уже почти 100 лет. Естественно нужно, что бы образование аммиака было не лавинообразным, а очень постепенным. Посоветуйте плиз как усовершенствовать эту технологию. Какое сырьё для получение газообразного аммиака посоветуете ?
-
Здравствуйте.Ответьте,пожалуйста.Нитрит калия+цинк+вода+ ещё какое-то вещество=аммиак +неизвестно что.
- 4 ответа
-
- нитрит калия+цинк+вода+...=ам
- нитрит калия
- (и ещё 2 )
-
Ребят, нужен монометилгидразин. Хочу получить гидразин методом Байера, из аммиака и перекиси водорода(2NH3+H2O2=N2H4+2H2O), а потом провести метилирование, но тут проблемка, никак не могу наидти инфу по етой теме, помогите плиз!
- 8 ответов
-
- монометилгидразин
- гидразин
- (и ещё 3 )
-
Возможно ли получение аммиака по такой реакции: NH4NO3+NaOH=NaNO3+NH3+H2O По идее, для того, чтобы началась реакция нужно смешать реактивы в сухом виде и нагреть, но я слышал, что при нагревании аммиачная селитра вначале разлагается на Оксид азота 1, а затем может взорваться. Кто знает, подскажите возможен ли этот способ. Если нет, то подскажите другие способы получения аммиака с помощью нитрата аммония.