-
Постов
1275 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные the_Rion
-
-
Ну короче самое простое и оптимальное если покупать то это анод.
Его можно ножом строгать чтобы стружка получилась или как лучше измельчить?
-
-
7 минут назад, Максим0 сказал:
гейропейцы магниевыми анодами не торгуют?
Ясное дело торгуют. Только стоит от 6 евро за штуку, а по весу сколько он я не знаю, но на вид не более 200 грамм за эти деньги. Хотя я не знаю как он конструктивно сделан, по картинке не видно, может там граммов 100-120 магния.
Есть размер 21x225 за 6 евро, а есть 21x1000 за 17 евро, а есть 21x660 за 11 евро, ну походу выгоднее за 17 евро брать тогда, но сколько в нем магния по весу я хз.
-
19 минут назад, dmr сказал:
Если перегонять в воду, то ничего не потеряете.
Может да, может нет.
Эксперимент вам даст ответ)))
При выпаривании тем более, улетит хлороводород, в присутствии нелетучей "алюминиевой кислоты "
Я в Евросоюзе, а не в России нахожусь вообще-то. Принять вот у меня магний на свалке это да, без проблем. А вот продать мне кусок магния скорее всего что пошлют нах. Не, ну если покупать от 1 тонны или больше, или от 100 кг. А так скупка 700 евро за 1 тонну магния. Можно в принципе я думаю позвонить на свалки, может кто-то что-то и продаст мне из магния, но вероятность очень маленькая.
-
9 минут назад, dmr сказал:
Это дигидрат
Сушить надо в токе хлороводорода. Возможно проканает с NH4Cl сушить
Нашатырь как раз в этом диапазоне температур разлагается
Нашатырь канает, но мне его жаль тратить.
Пишут что :

То есть парить до одноводного, до 300С. Далее выносить воду электролитически, до ее исчерпания. На потери на шлам наплевать и все. Либо, может быть реально вынести воду металлическим алюминием, хз.
-
1 час назад, dmr сказал:1 час назад, dmr сказал:
Ну я вот прочитал в книге как делать надо, там в ней все разжевано. Книга называется "Руководство к лабораторным работам по прикладной электрохимии", 1948 года.
Смысл такой, что делать советуют при температуре от 600 до 700С, а этой большой диапазон температур, то есть точная температура как по Кастнеру не нужна. Это очень славно. В таких условиях магний будет плавать сверху расплава и все. Но я думаю что достаточно просто плавить смесь солей при 439С и должно быть нормально, в принципе что магний отвалится от электрода, что не отвалится, это я думаю - мелочи. Анод пишут брать графит, катод - железо. Плавить смесь в фарфоре. Думаю можно в химстакане стеклянном плавить. Вообще len1 на sciencemadness писал что NaCl+CaCl2 не портит стекло и фарфор, я думаю что и NaCl+MgCl2 не портит, тем более в книге говорят брать фарфор.
Второе, как я понял, если прокаливать смесь NaCl (можно и KCl) с MgCl2 , то тогда разложение минимальное, несколько процентов всего. Кроме того, пишут что вода дает шлам и это почти вся проблема, ну разве что уменьшит выход магния. Зато не взрывает как натрий по Кастнеру. Шлам я думаю будет валиться отдельно, в конце-концов, нужно будет просушить по максимуму, то что не высохнет - все равно исчерпается рано или поздно в ходе электролиза, ведь вода в смеси солей не бесконечная. Кончится вода, убрал шлам и тогда я думаю будет стабильно все идти.
Хлорид магния из сульфата сделать, ну как обычно - осадить карбонат магния содой, обработать соляной кислотой и получить шестиводный хлорид магния, смешать с солью и просушить. Я думаю это будет попроще, чем просушить хлорид кальция, который по Карякину сушат при 1000С емнип. Это если делать процесс из NaCl+CaCl2.
И в принципе это получается рециклинг магния, если делать по NurdRage из магния, щелочи и масла, то будут отходы в виде гидроксида магния. Тем более что 439С это куда проще чем теже 580С для NaCl+CaCl2, ну и к тому же хлор будет, а имхо хлор это всегда хорошо и немного хлора еще никому не навредило. И самое главное что не взрывает от воды, и что не нужен точный контроль температуры как по Кастнеру. Плюс еще рециклинг отходов гидроксида магния. Греть тоже не сложно, думаю газовая горелка потянет, если нет то мангал 100% на углях потянет.
Короче, буду пробовать. Надеюсь что получится.
ПС. Аноды дорогие у нас если их покупать, а на свалках хз, есть или нет. Ну и отходы в виде гидроксида магния тоже куда-то девать надо, выбрасывать неохота, можно их рециклить назад в магний.
-
6 минут назад, главный колбасист сказал:
А если стиральный порошок дешевый без добавок растопить и подвергнуть электролизу?
Это типа фосфат натрия? Хмм, этих фосфатов несколько разных существует, надо смотреть температуры плавления и заодно разложения.
Вообще кстати на sciencemadness кто-то даже и хлорат натрия плавил, правда не помню какие в итоге результаты были.
-
30 минут назад, dmr сказал:
Не понятно что хотели сказать.
Выделяться, в результате электролизе, будет скорее магний, чем натрий.
Я имею ввиду, магний на электроде будет "расти", так? Поскольку если до плавления самого магния не нагревать, то магний не будет плавиться и плавать на поверхности расплава смеси солей. Или магний будет отваливаться от электрода?
А натрия не должно быть в этом процессе, его ведь не приглашали, бгггг....
Хотя кстати в чем плавить эту хрень, наверное в химстакане прокатит? Поскольку думаю что нержавейку разьест. Электроды тоже кстати какие брать, стальные или медные покатят, или надо графит?
У меня просто сульфата магния много очень, можно жопу в клочья порвать! Поэтому план такой - надо "вылечить" сульфат, чтобы он не болел и стал хлоридом, замесить с кухонной солью и подпалить, т.е. заплавить и сделать металл магний, дальше едкий натр и маслице, и все, все довольно просто и куда легче чем процесс Кастнера.
-
Интересно, а что если плавить эвтектику NaCl+MgCl2, где 45% NaCl и 55% MgCl2 и плавится при 439С, будет ли из этой фигни отпочковываться металлический магний, я так понимаю что если не поднимать температуру расплава до точки плавления магния, то в таком случае магний осядет на электроде, правильно? Ну и магний потом в маслице и с едким натром его тогда на натрий пускать, как дядя NurdRage учил.
Должен по идее без тонкой настройки как процесс Кастнера, короче из гавна и палок без особого контроля температуры и прочего получаться магний не? Ну то есть взрываться не будет как по Кастнеру от воды, короче особых проблем не должно быть, да и магний в расплаве думаю особо растворяться не должен, как думаете?
-
Кстати нет ли методики, как сделать себациновую из касторового масла? Искал, не нашел нигде.
-
-
3 часа назад, St2Ra3nn8ik сказал:
Тоже не получите: нитрат в расплаве - окислитель и он даже не даст образоваться натрию в каком либо количестве. Разве что применив известный "метод с лампочкой", применяя расплав только NaNO3, по эстонски меееедленно и печально наработаете. Внутри лампочки.
Да уж, ну так то нитраты уже Владимир с chemistry-chemists плавил, ничего там существенного не происходило, натрий не получался, но и не взрывалось ничего. Так что нитраты отпадают.
-
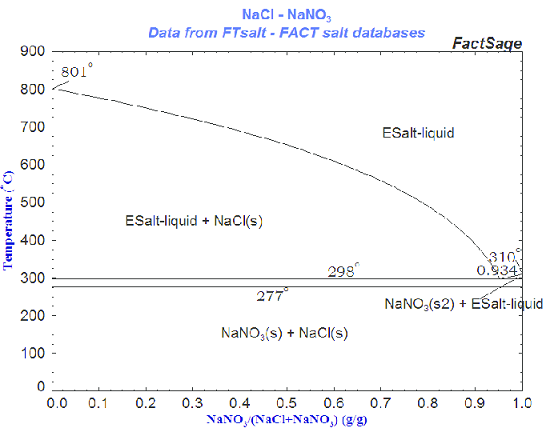
Есть вообще эвтектика NaCl+NaNO3, плавится при 300С, хз может из нее можно выделить натрий.

Или в принципе брать NaOH+KOH, но в пределах плавления 200-250С, поскольку Нака жидкая судя по Википедии от 40% К в Наке и более, плюс я думаю что не всякая Нака бахает на воздухе, а только лишь та Нака, которая богата калием.
Хотя имхо Нака - это кака, ну ее нах.
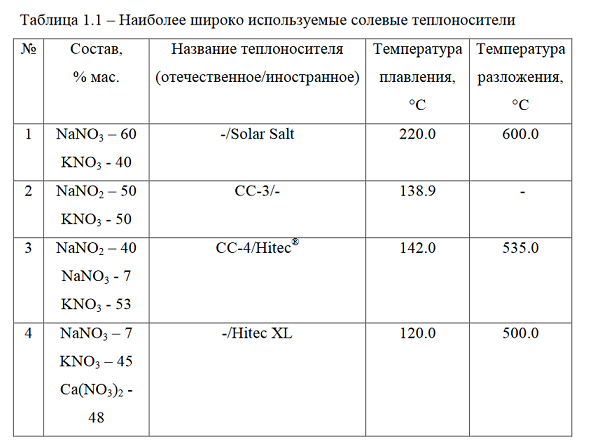
Есть еще нитратные эвтектики, можно попробовать их электролизить, не факт что ебнет кстати :

-
5 часов назад, Ruslan_Sharipov сказал:
Перчатки явно не помешают, хотя хз сколько там того цианида наплавится по количеству.
1 час назад, St2Ra3nn8ik сказал:а посему ацетон, ДМСО точно идут лесом.
Думаю что да, хотя я делал с ДМСО еще вот что -
Брал раствор прокаленного нитрита натрия в аптечном Димексиде и машинное масло 10w40, масло не смешивается с Димексидом и всплывает наверх. Опускал во все это медные электроды и подавал ток. В результате на границе фаз возникало множество пузырьков или шариков вещества, может натрий, а может и нет, хз - на глаз не видно что это, которые проникали в масло и эмульгировались с ним. При этом размешивая оба слоя нельзя было добиться чтобы эмульсия слилась в одно целое и отслоилась от масла. Постепенно это вещество растворялось в масле, но очень медленно. По идее, натрий наверное растворим в машинном масле, но если брать детское масло как у NurdRage, то возможно это прокатит. При условии что эти шарики были именно натрием, а не чем-то другим.
-
1 час назад, Ruslan_Sharipov сказал:
Цианид можно сделать, вот Chemplayer делал, сперва плавил KOH с мочевиной, потом отделял цианат и сплавлял с углем. У него даже тест на Prussian Blue получался потом, т.е. должно работать, но хз что там за выходы. Но я лично думаю сразу сплавить едкий кали с мочевиной и углем, думаю прокатит, не знаю правда сколько там побочки будет, так то по идее будут остатки карбамида и цианата в расплаве, но попробовать можно. Главное чтобы газовая горелка потянула достаточный нагрев.
А так да, цианид очень полезный реактив в органике, мне бы пригодился.
-
30 минут назад, главный колбасист сказал:
А синтетические моющие средства,сульфокислоты,то есть?
p.s. А с калием прокатят все эти вышеописанные предполагаемые манипуляции?
Не знаю, вообще была (и сейчас до сих пор осталась) большая тема на sciencemadness, там пробовали подбирать разные органические соли натрия, но по-моему так ни к чему и не пришли.
Так-то в принципе было бы здорово электролиз расплава цианата натрия сделать, всего-то 550С и на аноде я думаю азот и натрий, на катоде мне лично похуй что будет, но надо два условия - чтобы расплав был проводником и чтобы натрий не растворялся в расплаве. Тем более что если цианат мог бы работать, тогда нет нужды в эвтетике скажем NaCl+CaCl2, поскольку CaCl2 слишком геморно обезвоживается.
Хотя я думаю что потом продолжу свои эксперименты по процессу Кастнера, и буду пробовать стабилизировать расплав едкого натра металлическим алюминием, чтобы убить в нем воду, поскольку даже возможная примесь алюминия с натрием не должна мешать Кляйзену, либо возможно попробую этилат натрия сделать азеотропной отгонкой, мне в целом необязательно иметь именно металл натрий, этилат тоже покатит.
А так вообще да, надо реально попробовать сделать этилат, так как толуола у меня очень много, могу достать его канистрами и очень дешево, азеотропно разогнать спиртягу, воду и толуол, в принципе даже если эталат чутка окислится, ну так весь то он все же не должен окисляться, для Кляйзена покатит, а если покатит, то мне металл натрий нахуй не нужен тогда. И кстати этилат тоже довольно дешево будет, дешевле чем через магний, ну это если аноды покупать. Поскольку меня лично очень жаба давит аноды брать магниевые, они слишком дорогие.
-
15 часов назад, St2Ra3nn8ik сказал:
В ДМСО из щелочных можно получать только литий, остальные с ним слишком быстро реагируют. Не исключено, что можно попытаться применить другой апротонный полярный растворитель, например, пропиленкарбонат. Но в любом случае он должен быть максимально сухим.
А пропиленкарбонат пишут что реально работает. Вопрос в том где его брать и сколько он стоит. У моих знакомых барыг его нет. Делать его через карбонат серебра у меня лично сырья не хватает и реактивов.
8 часов назад, sibra сказал:Дома, натрий... а на кой ляд ?
А сделайте этилацетоацетат из этилацетата, но без натрия. Вообще можно сделать, имея только едкий натр и этанол, отгоняя воду бензолом или толуолом, но думается мне что этилат будет резво окисляться на воздухе при попытке его выделить, а раствор этилата в спирте для реакции не прокатит.
5 часов назад, Ruslan_Sharipov сказал:Пиридин и ДМФА надо покупать где-то, они дешевые, не? И кстати я нигде истории успеха с пиридином или ДМФА не видел, теории то да, дохрена понаписано. И насчет лимонада я сказал именно про карбамид и соду, это реально лимонад был бы по цене и доступности реактивов, если бы это работало. А пиридин и ДМФА, если это и работает, то нихрена это не лимонад уже, их еще где-то доставать надо.
Иначе кому-то из магния делать вполне лимонад, но не всем, а только лишь тем у кого дохуя магния халявного с металлоприемки или откуда-то со свалок, мало ли. Если магний покупать аноды, тогда не лимонад нихрена уже будет. То есть, это смотря у кого что есть из реактивов.
28 минут назад, Ruslan_Sharipov сказал:Хорошая мысль.
В керосине должна растворяться натриевая соль какой-нибудь жирной кислоты с длинным углеводородным хвостом. Попросту говоря, надо растворить в керосине мыло.
В полученном растворе, возможно, будет растворяться менее жирная соль, от менее длиннохвостой кислоты, вплоть до ацетата. После этого можно добавить хлорид или сульфат натрия для диссоциации. И это всё подвергнуть электролизу.
Олеат или пальмитат натрия, они проводники то хоть?
Имхо мокрым способом если и делать то через магний, как NurdRage делал. Правда дороговато получится, зато реально работает, ну ментол для затравки вполне достать можно, он сравнительно недорог.
-
38 минут назад, Ruslan_Sharipov сказал:
Не знаю. Но в момент протекания реакции карбоната натрия и мочевины какие-либо ионы могут образовываться. Электролиз их растащит и может дать много интересного в том числе и для понимания механизма самой реакции.
Цианат будет падать в осадок в расплаве карбамида и все, есть похожий патент СССР, сводится к тому что получают цианат натрия электролизом расплава смеси карбамида и нитрата натрия, откуда цианат натрия падает в осадок и происходит сий процесс при 120С, то есть думаю даже до 140С поднять ничего не изменит.
Ссылка на патент - https://yandex.ru/patents/doc/SU558971A1_19770525
Ах да, по идее чистый расплав цианата натрия мог бы дать азот и натрий и наверное СО2 на втором электроде, но это при условии что расплав цианата натрия как минимум проводник электричества, поскольку я хз проводит ли вообще ток расплав цианата натрия (при 550С), возможно он не проводник даже.
Был бы такой лимонад, сделать мателлический натрий всего-то при 140С из мочевины и соды, да нафига тогда процесс Кастнера вообще нужен был бы.
-
31 минуту назад, Ruslan_Sharipov сказал:
Ну образуется, ну и что? Он кристаллизованный будет или будет раствор цианата в расплаве карбамида? Если будет кристаллический, то электролиз цианата до натрия не пойдет. Если будет в растворе в расплаве карбамида, тогда там дофига побочки будет, на Википедии там расписано сплавление - побочки немеряно, это и СО2 и вода и аммиак, короче целый зверинец.
Смотря что вы получить предлагаете, по идее даже электролиз расплава карбамида без ничего больше тоже что-нибудь да даст в итоге, правда хз как он ток проводит вообще.
Плюс даже если и прокатит как вы предложили для получения натрия, то там по-любому вода получается в процессе, наверняка натрий будет сразу с этой водой реагировать и сгорать, а ну и да, еще вода будет разлагаться, короче имхо примерно таже шляпа, что и едкий натр плавить и электролизить - вода сильно мешает. Еще кстати надо учесть растворимость натрия в расплаве карбамида и прочей шняги побочной, биурет и так далее.
Имхо если что и есть рабочее электролизом расплавов это Castner's cell и Down's process.
-
1 час назад, Ruslan_Sharipov сказал:
Карбонат натрия при сплавлении с мочевиной даёт изоцианат натрия: 3 (NH2)2CO + Na2CO3 = 2 NaNCO + 2 CO2 + 4 NH3. Попробуйте в этот момент подключить электролиз. Явно следует ожидать чего-то интересного. Делайте всё на открытом воздухе во избежание возможных отравлений.
И в чем смысл? Цианат натрия плавится при 550С, проще поступить стандартно и плавить эвтектику NaCl+CaCl2, при 580С то есть всего-то поднять t на 30 градусов, это мелочи, что является уже обкатанным, проверенным и рабочим методом.
Кстати пробовал в ДМСО электролизить раствор NaNO2, который в ДМСО растворим куда лучше, чем NaCl, ничего это полезного не дает, хотя вроде бы (это не точно) даже и появляются мельчайшие капли натрия, которые тут же растворяются, вобщем натрий не получается таким образом сделать.
Либо делать как NurdRage натрий тогда, через магний и ментол в масле с NaOH. Правда дороговато получится, это если магний брать в виде анодов бойлерных.
-
1 час назад, Ruslan_Sharipov сказал:
Что значит бггг... ? Оно дурно пахнет или что?
Я бы не сказал, что дурно пахнет, примерно как фенол, да это и есть фенол, просто окисленный. У меня кристаллический фенол имеется, он также розовеет от воздуха, а потом цвет становится более бордовый.
Эти феноляты которые у вас получаются, я думаю что они особой ценности не имеют и получать их таким образом не препаративно.
А получать салицилат наверное лучше в абсолютном этаноле или метаноле из едкого кали и салицилки, поскольку из аспирина в таких условиях скорее всего будет ацетилсалицилат все-таки, хотя может и пойдет с K2CO3 реакция, хз...
Да и вообще на мой взгляд феноляты калия более устойчивые, чем натрия.
-
57 минут назад, Ruslan_Sharipov сказал:
А что там происходит?
Прочитал. Действительно, написано следующее. Необходимо также брать небольшой избыток салициловой кислоты, так как слабо щелочные и даже нейтральные растворы салициловокислого натра при выпаривании окрашиваются в тёмный цвет. Что же всё-таки там происходит?
Я думаю там происходит примерно тоже самое, что и с парацетамолом делается в водном растворе в щелочной среде, при том что в кислой среде парацетамол (или его производное) гораздо устойчивее, чем в щелочной, имхо если совсем по-простому, то это окисление фенольной группы кислородом воздуха происходит вобщем, ну и в водном растворе может еще и гидролиз идет кстати тоже, да.
Я думаю что аспирин будет вести себя несколько иначе, если его прореагировать с KOH в абсолютном или хотя бы 96% этаноле, короче в безводной среде. Хотя не факт.
А так вобщем-то у меня аспирин с содой на холоду (примерно +5С...+10С) не темнел, правда и реакция не слишком-то и быстрая, но газит эта смесь довольно долго. Кстати если этот раствор пролить на раскаленную или достаточно горячую конфорку электроплитки, то образуется розового цвета вещество, бггг...
-
Салицилат натрия должен кристаллизоваться из подкисленного раствора, а не из нейтрального или щелочного, иначе темнеть будет.
Читайте Кацнельсона, у него все написано.
Кстати если соду с аспирином покипятить, то раствор темнеет прямо на глазах, становится как чай по цвету.
-
18 минут назад, dmr сказал:
Ну и что, это не показатель. У меня краска есть вишневая, на банке написано - содержит кобальт. Какое именно соеденинение я хз, но таки кобальт может быть вишневым пигментом.
Даже марганец может быть вишневым - я как-то взял черную бурду от солевых батарей, а там есть NH4Cl, залил электролитом и получил темно-вишневый раствор, ну и что, марганец тоже не дает вишневый цвет, а дает розовый, с черной шнягой от щелочных батарей так и происходит, но это не показатель, в солевых батареяк есть соль аммония, а аммоний дает квасцы с марганцем, как раз квасцы и есть вишневого цвета.
А больше в принципе и нечему там быть, никель наврят-ли, неодим да дает розовые соли, но наврят ли у вас там неодим. Кандидаты имхо в основном это хром, марганец, кобальт и железо. Может медь еще, но маловероятно, явно это не она.



Получения натрия в домашних условиях
в Неорганическая химия
Опубликовано · Изменено пользователем the_Rion
Мне возможно найдут на свалке кусок магния бесплатно, как ни странно.
Точить его нечем, у меня только дрель есть ну и шуруповерт. Можно по идее широким сверлом пытаться крошить, хз.
Может на терке можно тереть, как морковку, ахахах?
Не на взрывпакет, а стружку или крупу на получение натрия по NurdRage.