бродяга_
Участник-
Постов
13189 -
Зарегистрирован
-
Посещение
-
Победитель дней
328
Тип контента
Профили
Форумы
События
Весь контент бродяга_
-
ну не в лоб, так по лбу. вода не выделяется, она связывается. а может это бот?
-
надо и в масло тоже давать присадку + учитывать срок работы деталей. иначе выводы будут весьма ошибочны. Влияние данных присадок на топливную систему и механические детали двигателя не оценивалось. Использование данных активаторов экономически не оправдано. ссылка на патент... https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwj67_GMhPn3AhXuk4sKHYbzBt8QFnoECAUQAQ&url=https%3A%2F%2Fpatents.google.com%2Fpatent%2FUS5258048A%2Fen&usg=AOvVaw0aBQH6sNHgo7AWjfls3rA7
-
что и предложил выше. проясню подробней. сера в солярке нужна для нормальной работы топливного оборудования, сернистая пленка на плунжерных парах препятствует задирам и вымыванию железа давлением. есть цифры по оптимальному содержанию серы, возможно их найти при желании, так вот, превышение нормы серы, уже будет давать кислотность для коррозийного износа цпг. то есть нужно по содержанию серы вложиться в определенный коридор допуска. если же в солярку добавлять присадки, тогда содержание серы возможно уменьшить на порядок, улучшив еще несколько параметров по износу топливной и цпг. однако все это надо проверять на практике.
-
к тому что даже 80% потраченной на разложение воды энергии допустимо для удачного электролиза.
-
по ссылке нет ничего про лечение. а здесь есть... https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwiBq43w1IuAAxVxGxAIHaK-A10QFnoECA0QAQ&url=https%3A%2F%2Fpubmed.ncbi.nlm.nih.gov%2F27350395%2F&usg=AOvVaw11W42WTxH2LkA6LqX2HdQN&opi=89978449
- 4189 ответов
-
- коронавирус
- противовирусный
- (и ещё 8 )
-
например... https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwjN0or50ouAAxXIHhAIHYpIAlEQFnoECBAQAQ&url=https%3A%2F%2Fnauka.tass.ru%2Fnauka%2F7013084&usg=AOvVaw03k3CcbEdQ5-MPk-sDVGE0&opi=89978449 Российские биологи выяснили, что фуллерены, "наномячи" из углерода, могут поглощать токсичные белки и препятствуют накоплению белкового "мусора" в клетках мозга. Авторы работы считают, что эти наноструктуры помогут создать лекарство от болезни Альцгеймера.
- 4189 ответов
-
- коронавирус
- противовирусный
- (и ещё 8 )
-
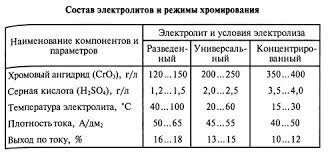
Параметры режима хромирования в данном случае следующие: температура t = 16 ... 25° С; Dк = 20 ... 80 А/дм2; a = 25 ... 30 %. Высока кроющая способность данного электролита. Корки получаются относительно мягкими, пластичными с малой пористостью. Скорость осаждения хрома в два раза выше по сравнению с простыми сернокислыми электролитами. a = 25 ... 30 %. выход по току.
-
есть тетрохроматный у него выход по току чуть лучше. Для хромирования также используют тетрохроматный электролит, положительным качеством которого от ранее рассмотренных является значительно меньшая агрессивность, так как большая часть хромовой кислоты нейтрализуется щёлочью, образуя тетрохромат натрия Na2O × 4CrO3. Данный электролит имеет следующий состав: CrO3 = 350 ... 400 г/л; H2SO4 = 2,5 ... 3,0 г/л; едкий натр NaOH = 40 ... 60 г/л. https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwiu6bmuzIuAAxVmKhAIHU5xAFUQFnoECBIQAQ&url=http%3A%2F%2Fwww.rvideo-kaluga.ru%2Fsho%2Fba0321.htm&usg=AOvVaw1NBcNne6nEBbyEBzLUWnT3&opi=89978449
- 41 ответ
-
- 1
-

-
и где тут логика? у меня есть присадка к маслу и к топливу, если есть желание и возможность протестировать пиши в лс.
-
все как армейском анекдоте про шомпол из того же сплава.
- 41 ответ
-
- 1
-

-
-
тут капнул гуглом интересный процесс откопал... https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwiX3ICvyIiAAxXQGRAIHXMZBo4QFnoECA8QAQ&url=https%3A%2F%2Fmnsl-journal.springeropen.com%2Farticles%2F10.1186%2Fs40486-021-00141-4&usg=AOvVaw3B6DFPu_h5qsv40_omia4Y&opi=89978449
-
с никелем или медью происходит так же. в электролиты вводят буферные добавки для стабилизации кислотности или избыток кислоты. это конечно практика, а не задачи.
-
хром может осаждаться металлом на катоде из водных растворов в отличии от ал. https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&ved=2ahUKEwjRhtvztYeAAxXNwosKHS-XDzMQFnoECBQQAQ&url=https%3A%2F%2Fchemer.ru%2Fservices%2Felectrolysis%2Fsolutions%2FCrBr3&usg=AOvVaw2dMTbg3maXsHAsvNFX3Tkr&opi=89978449
-
на аноде будут выделятся анионы, то есть хлор, кислород или окислы хлора, зависит от потенциала, то есть напряжения. на катоде, водород и гидроксиды растворенных металлов.
-
у кого то с этого форума покупал аноды титановые с покрытием. https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwiW6oPa-oaAAxWlKBAIHVYOAWAQFnoECBMQAQ&url=https%3A%2F%2Fwww.forumhouse.ru%2Fthreads%2F494216%2Fpage-4&usg=AOvVaw1Mj8yBQ8j6-_h3fQv0ajc_&opi=89978449 потом перешел на платиновые в своей технологии. ток считают по площади электродов. обычно амперы на дм2.