-
Постов
660 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Nimicus
-
-
Для простоты расчетов положим, что масса смеси = 100 г. Обозначаем количество вещества 12CH4 равным X моль, количество вещества 14CH4 равным Y моль и выражаем массу смеси и массу в ней водорода ( = 0,23 x 100 = 23 г) через X и Y - получается система из двух уравнений с двумя неизвестными. Решаем ее, ну а дальше по известным количествам 12CH4 и 14CH4 находим массовую долю углерода-12.
-
 1
1
-
-
Там не только избыток метилиодида нужен, но и основание. Такое алкилирование с карбонатом калия пойдёт при комнатной температуре до четвертичной соли.
То есть при комнатной температуре анилин будет реагировать с метилйодидом с образованием йодида метилфениламмония и дальше не будет?
-
Здравствуйте!
Подскажите, пожалуйста, будет ли взаимодействовать анилин с метилйодидом при 30 oС (так указано в условии задачи)? Понятно, что метилйодид алкилирует анилин, но при какой температуре (комнатной или повышенной) - нигде не могу найти. Если будет-таки алкилировать при комнатной температуре, то до моно-, ди- или триметилпроизводного (при избытке метилйодида)? -
Этан + Cl2, hn = A
A + PrCl (+2Na) = B + C + D --(Cl2, hn)-- > E --(NaNO2)--> F + L --(6[H])--> M
Понятно, что B, C, D - бутан, пентан и гексан.
Предположим, что только бутан при хлорировании образует преимущественно одно производное, тогда E - 2-хлорбутан.
Но что такое F и L - откуда 2 производных?
вверх
Возможно, имелось ввиду, что при взаимодействии хлорпроизводного с NaNO2 образуется смесь нитропроизводного (R-NO2) и алкилнитрита (R-O-NO), т.к. нитрит-анион является амбидентным нуклеофилом.
-
с каллием в пара
А можете скинуть мне ссылку на статью, где вот таким образом хинолин получается, но с метокси-группами в фенильных кольцах (в пара-положениях) дикетона? А то преподаватель утверждает, что там будет другая какая-то конденсация
-
по третьей, тебе коллега верно написал
Спасибо!
Но в третьей реакции - пинаколиновой перегруппировке - все-таки другого рода субстрат. В найденной реакции просто циклогександиол, в нем нет аннелированного бензольного кольца, а оно, как мне кажется, может изменить направление реакции. Нельзя ли поискать реакции с такого рода субстратами (гидрированные нафтодиолы)?
-
С оксимом я лоханулся, откуда там оксиму взяться...
Пинаколиновая перегруппировка тут может быть, только "наоборот" - атакуется третичный гидроксил, а переносится гидрид от углерода с вторичным гидроксилом.
Видел такое, но без специального названия.
Но по идее протонироваться должен легче вторичный гидкросил + катион соответствующий хоть и вторичный, но бензильного типа, т.е. более устойчив, чем третичный. Потом сдвиг метидной группы. Как мне казалось
-
Бро, найдёшь ответ - черканёшь? Самому интересно.
Особенно - второй процесс.
В первом мохбыть оксим циклизуется и восстанавливается? Тут есть варианты, но как-то всё - кривобоко.
А во втором, кроме ретроДильса-Альдера, чёто и не кажется ничего. Да и дальше - что там делать с фураном и малеиновой кислотой?
Мне вот тоже ничего, кроме Дильса-Альдера, не приходит в голову во втором. А вот в первом - не совсем понял, как там оксим получится и что дальше происходит. Можете нарисовать, что там может быть по Вашем мнению?
И еще хотел спросить насчет вот такой реакции:
Я посчитал, что будет пинаколиновая перегруппировка с образованием вот такого продукта, но оказывается, что это неправильно.
Кстати, может быть Вы знаете, как называется реакция "димеризации" малонового эфира под действием йода в основной среде? Нигде не могу найти.
-
-
Здравствуйте, почему при прокаливании сукцината натрия( NaOOC-CH2-CH2-COONa) образуется преимущественно этан? Как эту реакцию записать? Также вопрос по прокаливанию смеси ацетата кальция( CH3COO)2Ca и формиата кальция (HCOO)2Ca ( преимущественно образуется этаналь) . Ответ на тест есть, а реакции найти не могу. Подскажите,пожалуйста.
Предполагается, что сукцинат натрия прокаливается вместе с гидроксидом натрия:
NaOOC-CH2-CH2-COONa + 2NaOH (нагревание) → CH3-CH3 + 2Na2CO3
При прокаливании кальциевых солей карбоновых кислот образуются карбонильные соединения в соответствии со схемой:
(RCOO)2Ca (нагревание) → R-CO-R + CaCO3
Смесь ацетата и формиата кальция будет представлять собой смешанную соль (CH3COO)Ca(OOCH), при ее прокаливании и образуется этаналь.
-
У меня тоже пишет
Не удается получить доступ к сайту
Это происходит на последних версиях Хрома и Оперы. Но, старая Opera 12.18 нормально его открывает и скачивает.
Спасибо, скачал!
-
Спасибо! Только про синтез почитать не могу - пишет, что сайт закблокирован.
-
-
-
чувак вот А
дальше декарбоксилируешь одну карбоксильную,
дальше с цинком, думаю, что аминокислоту хотели, порисуй в этом направлении
У меня получается вот так, но что-то я опять сомневаюсь(( :
-
Восстановление кислоты с помощью LiAlH4 до этанола, затем превращение в бромэтан и, наконец, реакция Вюрца с образованием бутана.
-
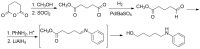
продукт А - это реакция Яппа - клингемана
Ого, как все хитро! Я глянул, что это за реакция и переделал:
Однако, не понятно, будет ли протекать в первом переходе внутримолекулярная циклизация при действии на малоновый эфир этилакрилата с образованием ди(этоксикарбонил)циклопентанона, а затем его реакция Яппа-Клингемана, или как я написал?
-
Спасибо! Вот и мне не понятно, что задумывал автор в последнем переходе, слишком много всего можно предполагать.
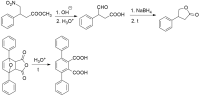
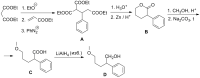
Я еще хотел спросить у Вас насчет вот такой цепочки превращений:
Мне кажется, что будет приблизительно вот так, но не уверен:
Особенно неуверен насчет перехода из B в С - не понятно, какой из изомеров при восстановлении будет образовываться, а может быть, я просто ошибся со структурой.
Что думаете? -
А что дальше? Амид восстановится до амина. Получится N-фенил-1,2,3,4-тетрагидропиридин.
Алюмогидрид с хлористым алюминием енамины расщепляет по С-N связи до алкенов. Нашёл упоминание в патенте о гидрировании енаминов алюмогидридом до третичных аминов, но в букварях такой реакции не встречал.
Может и ну его? Пускай остаётся
Спасибо, тоже предполагал, что здесь может быть такая циклизация и с самого начала обратил внимание на то, кислая среда, но решил уточнить. А насчет восстановления LiAlH4 - пускай N-фенил-1,2,3,4-тетрагидропиридин остается, да )
в точку!
аййй, и водичку отжимай!
http://pubs.acs.org/doi/suppl/10.1021/acscentsci.6b00113/suppl_file/oc6b00113_si_001.pdf
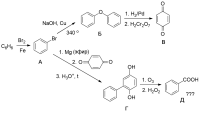
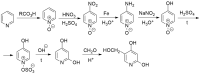
А вот еще одна спорная цепочка превращений:
Как Вы считаете, продукты будут такими, как я нарисовал? Особенно обеспокоен последним переход - из Г в Д (озонирование и расщеплением перекисью), и там вообще куча всего может образоваться. Да и насчет гидрирования дифенилоксида не совсем уверен...
-
-
N-окись пиридина не переживет железа.
она остается только при каталитическом гидрировании (см. файл NO.pdf)
и третье положение пиридина слишком слабый нуклеофил для формалина.
что бы формалин в пиридин засунуть, то сначала булем срывают протон, а потом формалин
Спасибо! Да, N-окись восстанавливается, Fe/Zn/Sn в кислотах, буду знать. Дальше, видимо, действительно так, как Вы написали.
-
-
На хрена делать фото на телефон с экрана компьютера, когда можно получить его в виде файла на самом компьютере.
¯\_(ツ)_/¯
-
KNaSO4 не имеет никакого отношения к маслу.
Не представляю зачем он может использоваться для обработки камней.
Это не фото, а скан с какого-то буклета, да еще и с муаром от неправильного сканирования.
Понять из описания, кроме фразы о сульфате калия-натрия, ничего невозможно.
Это просто фото на телефон с экрана компьютера, поэтому такой эффект муара, мне кажется. Несмотря на плохое качество, я увидел там слово "Hui", боюсь даже предположить, на что этот китаец намекает))

.thumb.jpg.57673d9b078af8ea6b76813bd85797f0.jpg)
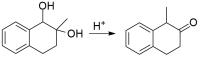
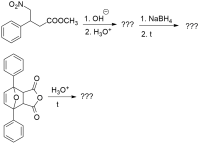

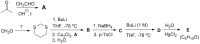

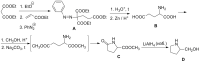
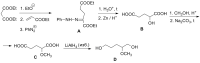

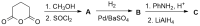

Задача на смеси, органика
в Решение заданий
Опубликовано
Да