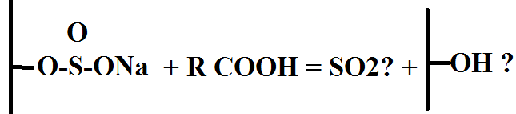-
Постов
3929 -
Зарегистрирован
-
Победитель дней
101
Тип контента
Профили
Форумы
События
Весь контент москатель
-
В паспортах на товарный ЛСТ (лигносульфонат) указывается, что продукт содержит до 40% золы. Зола, остающаяся после сжигания растений в основном - поташ (так раньше его и добывали). Но, при производстве ЛСТ нет такого жёсткого воздействия на древесные материалы. Да и раствор продукта даже паспорту предполагается с рН не менее 4,6, что не может быть при содержании в золе поташа. Что же может содержаться в золе?
-
100 м.ч. СКТН (низкомолекулярный кремнийорганический каучук жидкий) + 5 м. ч. этилсиликат -32 + катализатор. Я брал олигоаминоамид (Л-19, Л -20 или ПО-300). Чем больше катализатора - тем дольше время гелирования! График построили, что бы "назначать" время схватывания. Этот герметик нам больше нравился отличием от триацетоксисиланов и их аминных коллег чёткой предсказуемостью и независимостью от толщины и доступа влаги.
-
Стал сушить продукт под ИК лампой - противный едкий запах. На SO2 не похож. Сушить стал, потому что скомковалась - воды набрала и, действительно, гидролиз пошёл, что ли? И что получается? На сковородке сушил. Так металл сковородки, что ли "поела"? Цвет воды (залил, что бы отмокла перед мытьём) ярко рыжий.
-
Обычные сульфиты даже слабыми кислотами разлагаются, но в эфире сернистой кислоты индукционный эффект углерода молекулы изменяет ситуацию с электронной плотностью на О и опосредованно на S. Не изменяет ли это способность к диссоциации солевого остатка и стабильность SOONa? Разложится ли солевой остаток кислотой, и что останется на углеродном остове молекулы? ОН? То есть, гидролиз эфира пойдёт? Как оцениваете эту возможность?
-
Это растворитель: метилпирролидон. Как и со всеми растворителями - осторожность. Токсичность: LD50 при дермальном нанесении - кролик - 8000 мг / кг. Вы, ChemistryKate, на свой вес пересчитайте. Данные для кролика, конечно, но Вы морковку едите же? И от кролика образованием и размером тела отличаетесь. Ну, а если, всё же опасаетесь - интенсифицируйте метаболизм - знаете, как кролики это делают?
- 2 ответа
-
- 1
-

-
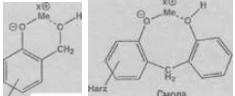
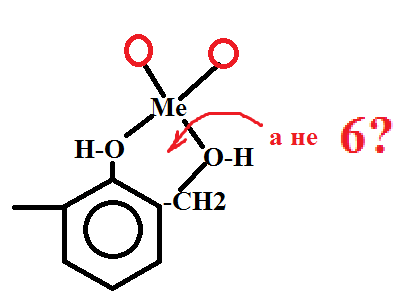
Вот только условия образования таких хелатов? И какие металлы могут хелатироваться? Просто в растворе, обеспечивающим встречу участников? Я разные хелаты получал, но именно с (незнакомыми мне) метилолами ФФС никогда дела не имел. Потому и спрашиваю.
-
Спасибо, Arkadiy. Тогда, вообще, 8 выходит! Я видел некоторое время назад в Сети структурные формулы хелатов ФФС с Ме. Сейчас многие сайты отказывают в приёме меня. Видимо, по ай пи России. Никак не могу найти! Как провалилась эта информация!
-
Здравствуйте! Комплексные соединения металлов с фенол – формальдегидными смолами – помню, что образуются, но стал искать – ни в справочниках – словарях, ни в Сети не нашёл конкретики. 101 смолу (третбутилфенольную) – у себя в коллекции нашёл. В паспорте не указывается самое, как мне казалось, главное: содержание метилольных групп. Они же у 101 смолы, видимо, с концов молекулярной цепочки – знать бы – молекулярную массу подсчитал - прикинул бы сколько соли металла брать. И задумался: а, вообще, на сколько легко образуются хелаты с этими смолами? рКа метилольной группы не знаю, как оценить. Металлы, наверное, хелатируются фенольной и метилольной группами. Кто имел дело с металлохелатами ФФС – подскажите, пожалуйста: образуются хелаты с третбутилфенольной смолой? И при каких условиях?
-
В общем случае, от наличия, хотя бы двух фаз с разными показателями преломления.
-
ЗдОрово сказано! послали на стройку... Бугор в бараке к столу подзывает по очереди: какими профессиями владеешь? Парень впереди меня: могу маркшейдером, могу землемером, могу... Моя очередь. Я с достоинством сообщил, что химик я. Стенки барака, казалось разлетятся от хохота. Бугор ручку уронил. А я узнал, что "химиков" много, но не все химики химики.
-
Эх, мастер, мастер! Разочарован я весьма: после такого подробного дознания (что, где, рН) я подумал: вот, человек обстоятельный, скрупулёзно всё переспрашивает - щас выдаст (не какой нибудь форумный стриммер) что-то! А он: барбитуру( ( Зачем же про растворимость выпытывал? Она ж в спирте плохо растворима. Про сольвент - нет упоминания. Одно достоинство: уреид. Так, есть же мочевина - средство для "обрубания" всех водородных связей - я использую - разжижает. У барбитуровой молекула плоская, ни объёма, ни растворимости. И барбитура... а чего сразу не кокс? Тропановые, хоть объёмны, как камфора. А ограничения в использовании, наверное, такие же, как и у барбитуровой.
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
+ от 15 до 800С смотреть выше и ещё выше (в старттопике) среды не содержат воды в значимых количествах = оценивать рН не корректно, но, если добавить дистиллированной воды, то она экстрагирует кислоты из органической массы и рН будет ниже 7. В диапазоне 5-6. Мастер, я ответил на все околосутьные вопросы? Может по теме, что ответите? Вопрос - в трёх последних строчках старттопика.
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
патамушта: а нитросорбид всего лишь Надо большую, но с близкой к шарообразной форме молекулу взрывобезопасного нитросоединения.
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
Спасибо,Arkadiy! Я с этого и начинал думать: пронитровать, что ли неонол? Но, я хочу получить лиотроп без "ароматики", что бы не только для нынешнего случая, но и на перспективу. Вот был у меня прецедент: крутой гель полиакриламида (6%) превратился в жидкость от прибавления кремнефтористого калия. Соль эта растворима всего 0,7%, но какой эффект был! А сейчас органика. И, если получится сейчас, я бы и в систему со свободными радикалами ввёл бы. Но, я плохо знаю поведение радикалов - как скажется введение соединений с бензольным кольцом. посмотрел: наверное, почти всё может быть прекурсором! И цена у пропионового!! Фталевый у меня есть - но это ароматика и он твёрдый - как нитрование вести? А вот МТГФА! Спасибо за подсказку! Он жидкий. У меня есть малеиновый. Но, они же твёрдые оба. Плавление около 90. Как же нитрование вести? В какой среде или в расплаве?
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
Да, поф. Я нитросорбид использовал (это нитроэфир), фурацилин, фуразолидон и фурадонин - это нитро к углероду напрямую. У нитро-группы большое лиотропное число. Она вторая после роданида по эффективности разгелирования (расплавления гелей). Нужна объёмная группа с минимальным зарядом. Нитросоединения, видите ли, получаются не только при использовании нитрующей смеси азотной с серной, но и в мягких условиях - с уксусным ангидридом. он тупо не растворим в органике. Мне нужно нитросоединение с алкильным или сложноэфирным фрагментом.
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
увы, я это знаю. Не знаю вот подойдут ли мне эфиры или углеводороды с нитрогруппой, связанной непосредственно с С. Вот нитрофураны и пробовал - у них именно так. А чем они примечательны? Почему Вам эта мысль пришла в голову? Они же - соли. С органикой, если только гидротроп дадут? Анион у них большой - поэтому считаете, что лучше?
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
Провожу работы с гельными массами. Управлять консистенцией, растворимостью и вязкостью предполагал введением анионов с высокими лиотропными числами. CaNO3, например, хорошо растворим в ацетоне и спиртах. Но, катион, что ли «высаливает» - получаются гетерегонные системы. Неплохо показали себя органические нитросоединения (нитросорбид). Фурацилин и прочие всё-таки плохо растворимы. Видимо, хорошим вариантом был бы жидкий нитроалкил (или что-либо подобное). Но, низшие ядовиты и взрывоопасны. А выбрать получение нитросоединения со взрывобезопасной стехиометрией сейчас затруднительно из-за запрещённости уксусного ангидрида. В СССРовском а.с., например, описывается простой способ нитрования циклогексанола. Но. Мягко нитруются соединения с активированной метиленовой группой. В J. Am. Chem. Soc.описывается синтез с малоновыми эфирами. Может, кто имел опыт нитрования, например, эфиров лимонной кислоты (более доступной для меня). Или других соединений с достаточно длинной органической частью (что бы снизилась опасность и растворимость в ароматических углеводородах была хорошей)?
- 15 ответов
-
- нитрование
- мягкие условия
-
(и ещё 1 )
C тегом:
-
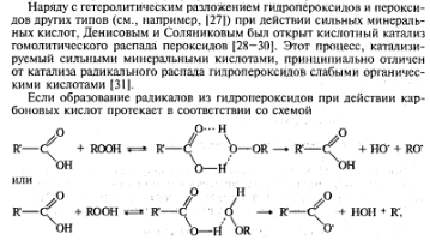
Вот странно: я и не задумывался - а может в этом всё и дело? Нук быстро образуется и быстро исчезает. Сам ГП оочень медленно окисляет, да ещё и не прицельно: путей распада ГП несколько - не каждый ведёт к желаемому нами окислению сульфидов. И перевод ГП в надкислоты - это находка для практика, использующего ГП для окисления. В литературе встречается описание распада ГП кумола тяжёлыми металлами и кислотами (в основном серной). От катализатора зависит путь распада и какие продукты образуются. И вот любопытно: Что же совсем без воды, значит надо, что ли, а то и распада по радикалам не будет? Поэтому у меня с серной и не получилось, видимо. Но, безводная серная - это, что-то совсем круто. А распад ГП, катализируемый слабыми карбоновыми кислотами идёт с образованием именно тех радикалов, которые считаются самыми сильными окислителями: а это уже для Вашего, пожалуй случая: Но, я так и не понял: что же принципиально отличного от катализа слабыми органическими Денисов и Соляников увидели у сильных неорганических кислот? Гомолитический распад, как и у органических кислот и в чём отличие? Количество воды (даже минимальное) может, действительно сильно изменить процесс. Ладно, вариант объяснения окисления ГП без образования надкислот я вот и нашёл. С сильными кислотами сложнее... Завтра в лаб подумаю.
-
Сколько? Вы оцениваете. Даже "чда" (смотришь на данные анализа - о!) проявляют кислотные свойства. В растворе ацетатов карбоксилсодержащие полимеры не гелируют. Из-за содержащейся там примеси УК? Раствор карбоксилсодержащих полимеров превращается в крепкий студень из смесевых углеводородных растворов (в одном ксилоле или сольвенте, вообще не растворимы). А "разкозление" требует вполне стехиометрически обоснованных количеств кислот. И? В ацетатных растворителях столько УК? Ну, наконец-то мы поладили и пришли к одному! Во как! Если она работает в НЕэквимолярном (не по стехиометрии) количестве - кто она? Катализатор? Но, катализаторы же САМИ в реакцию не вступают и не расходуются) Может согласитесь на "посредника"? Или может она (втихую) образуется из ГП и УК по мере расходования? ГП медленно окисляет (у Вас он, вообще, "не в своей фазе"), а НУК быстро. Так быстро, что наблюдательные учёные только к компу повернутся, а НУК из ГП образовавшись, уже сработала и исчезла? А? так а причём тут тогда моя схема: "слабая кислота + ГП + катализатор их взаимодействия = отличный результат" ? рассеяние. она и мне нужна, но и с деталями: мне же процесс вести с последующей демонстрацией сделанного под видеокамеру и ироничные ухмылки. О-о. "Даже светлые подвиги — это только ступени В бесконечные пропасти — к недоступной Весне!" (с) Увы, у меня тоже не последняя. Но, Весна! Может лаб моя реанимируется . Кстати! Про ступени. Корпус нового здания построили и проход в мою лаб теперь крайне сложен. В последний сессин я, каждый раз идя в лаб, забывал за поворотами про трубу, и она мне "напоминала" ударом то по лбу, то по темени. К завтрашнему сессину обещали всё исправить. Спасибо, Вам, terri! Коллега по над/пер кислотам.
-
Ну! Вы - коллега. Она интенсифицировала процесс - сильный разогрев и то ли пар, то ли дымок. А % конверсии не вырос. Я бензойную вводил в смесь субстрата с индуктором ГП (без слабой кислоты) и потом через несколько лет бензойную в смесь с синтезированной мной кислотой. И в первом и во втором случае заметно было разогревание и выделение "парка". А увеличение конверсии ни в первом, ни во втором эпизоде не было. Кстати, о кислотах: БА - проявляет кислотные свойства. То ли из-за примеси УК, то ли ацетаты с водой комплекс дают, работающий, как кислоты Бренстеда. Это я к тому, что хотелось бы понять механизм окисления. Наверное, их в наших случаях несколько. Но, найти бы ключ к управлению ими, и сделать один из механизмов преобладающим. С высокой конверсией и селективностью. А вы: во как? И всё-всё понятно? Тогда что скажете про мой вывод? + Согласны со мной? Или для Вас и остальное только диссипация научной энергии? Касательно воды. То есть, на сам процесс образования НУК и окисления она мало влияет, так, ведь? А лишь на конечный продукт:
-
Да. То есть, получается, что УК всё-таки значительно интенсифицирует процесс? Но, почему именно (и только) УК? + = вывод? Окисление идёт и через ГП и через НАД кислоты к одному и тому же результату. Но, с надкислотой (возможно в качестве посредника) идёт явно лучше. Согласны со мной? Ха. А "каталитические" количества УК, прибавленные к ним? Может главное: слабая кислота + ГП + катализатор их взаимодействия = отличный результат (и по % конверсии и селективности окисления - "в сторону продукта")? А серная - двухфункциональная и сильная. В тех концентрациях, что Вы брали, неокислитель. Но, ведь, могут быть и другие катализаторы процесса работы ГП + слабая кислота? Механизм работы комплекса ГП+ УК + серная - Вам же не ясен? Я сейчас Вас (Вы уж извините) усиленно "подталкиваю" к своим представлениям - мне же завтра в "поле" работать. Я (химик, но не спец по радикалам и полимерам) + биолог (увлекающаяся видом и "характером" молекул) + математик (20 лет с ПУ работал) + ироничный физик. Может и Вам что полезным окажется: мне объясняя, системность увидите. Или из моих опытов - что пригодится?
-
1. Отлично! В ИП, даже после непродолжительного УФ (длинноволновой части) облучения, обнаруживались ГП (я убедился). То есть, среда для "размножения" ГП благоприятная. 2. Ого! А Вы системно работаете. Уважуха. То есть, получается каталитическая способность кислот от силы (рКа) их зависит? Но, ИП, ведь, у Вас безводный? Может кат/активность зависит не столько от силы, сколько от функциональности? Последние кислоты - монофункционалы. Фосфорная - "хромая". Только серная и сильная и, по настоящему, двухфункциональная. 3. О! А так восхищались названием! "...как ветер в мае.." 4.Вот было всё понятно (хотя и огорчительно, и на сомнения меня повело), но вот этот пассаж : Но, как же это следует из п.2? Откуда вдруг у Вас взялось убеждение, что УК - имеет отношение к катализу!!!? Нигде же не было упоминания! Понимаете, terri, это же, как раз по моим представлениям! И опять: Вы же сначала мои представления сразу и решительно опровергли 29 марта: и вдруг: !? Понимаете, я-то столько лет так и считал: синтезированная мной слабая кислота - лишь катализатор/транспортёр кислорода, а главный поставщик О на окисление сульфидов - это ГП! А потом + опыты с кислотами (серная и фосфорная не подошли - бензойная интенсифицировала процесс - разогрев!) и... Вы со своими близкими к моей тематике опытами! Завтра съезжаются мои коллаборанты - а я "на распутье"! Откуда у Вас взялось намерение использовать УК в комплексе с ГП? Почему УК, а не муравьиная, например? У неё же 55%! здОрово. Значит всё же это именно окисление - лимитирующая время реакция? Окисление медленно идёт, а не образование НУК? Откуда Вам это стало известно? Почему Вы так решили? Я не оспариваю - хочу уточнить - Вы как к этому пришли? Вот это да! Началось в деревне лето! В какую, не в ту сторону? Сульфиды не окисляются? Вы сами-то не думали: что-то нет охватывающей и объясняющей всё это концепции? Малейшие, вроде незначительные изменения - и вместо гвоздей получаются розы!

.thumb.jpg.f9465747e1c4e32f09f53c6bfd45c2e4.jpg)