
ВНС
-
Постов
626 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные ВНС
-
-
1)Вычислите концентрацию ионов водород и гидроксила в 0,03 М растворе селеновой кислоты и pH этого раствора
2)Сколько граммов цианида натрия необходимо растворить в одном литре 0,2М раствора цианида натрия ,чтобы концентрация ионов серебра составила 2*10^-22 моль/л
3)При электролизе раствора нитрата натрия с никелевыми электродами масса анода уменьшилась на 1 г.Какие вещества и в каком количестве образовались при этом
На аноде
Ni – 2e = Ni2+
На катоде
Kатод 2H2O + 2ē = H2 + 2OH–
В растворе
Ni2+ + 2OH– = Ni(OH)2
Вещества в растворе и на катоде выделятся в эквивалентных количествах
ЭNi = M\2 = 29,5 г\моль
В 1 г будет 1\29,5 = 0,034экв
Для водорода это составит 0,034г или 0,017 моль
Для Ni(OH)2 0,034*46,5 = 1,581г или 0,017 моль
4)Определить ЭДС гальванического элемента (Pt)/ ClO- ,Cl- , OH- //FeSO4 /,Fe,если =0,01 моль/Л PH=9,
[ φ ]=ClO /Cl ,2 OH)=0.88 В
pOH = 14 – pH = 5
[OH-] = 10-5моль\л
Полуреакция
ClO- + H2O + 2e = 2Cl- + 2OH-
Eкатода = Е0 + 0,059\2lg10^-5 = 0,7325B
Eанода = Е0FeSO4\Fe + 0,059\2lg0,01 = -0,499B
ЭДС = Eкатода - Eанода = 0,7325 –(-0,499) = 1,23В
5)При температуре 500 С, нормальным давлением, =4,03 г/л.Из какого числа атомов состоит молекула
3 и 4 я решил,но не знаю так или нет в 1 запутался, а 2 и 5 - условие там нормальное или не хватает чего-то Во 2 то явно ошибка, а вот 5 как считать по эти данным?? Помогите,пожалуйста проверить 3 и 4, и подсказать ход решения для 1 и 5????
Первую я решил так
H2SeO4 = 2H+ + SeO42- Селеновая кислота сильная, поэтому диссоциацию можно принять за 100%
Значит [H+] = 0,03*2 = 0,06моль\л
рН = - lg[H+] = 1,22
pOH = 14 – 1,22 = 12,78
[OH-] = 10-12,78 = 1,66*10-13моль\л
Правильно??
-
1)Вычислите концентрацию ионов водород и гидроксила в 0,03 М растворе селеновой кислоты и pH этого раствора
2)Сколько граммов цианида натрия необходимо растворить в одном литре 0,2М раствора цианида натрия ,чтобы концентрация ионов серебра составила 2*10^-22 моль/л
3)При электролизе раствора нитрата натрия с никелевыми электродами масса анода уменьшилась на 1 г.Какие вещества и в каком количестве образовались при этом
На аноде
Ni – 2e = Ni2+
На катоде
Kатод 2H2O + 2ē = H2 + 2OH–
В растворе
Ni2+ + 2OH– = Ni(OH)2
Вещества в растворе и на катоде выделятся в эквивалентных количествах
ЭNi = M\2 = 29,5 г\моль
В 1 г будет 1\29,5 = 0,034экв
Для водорода это составит 0,034г или 0,017 моль
Для Ni(OH)2 0,034*46,5 = 1,581г или 0,017 моль
4)Определить ЭДС гальванического элемента (Pt)/ ClO- ,Cl- , OH- //FeSO4 /,Fe,если =0,01 моль/Л PH=9,
[ φ ]=ClO /Cl ,2 OH)=0.88 В
pOH = 14 – pH = 5
[OH-] = 10-5моль\л
Полуреакция
ClO- + H2O + 2e = 2Cl- + 2OH-
Eкатода = Е0 + 0,059\2lg10^-5 = 0,7325B
Eанода = Е0FeSO4\Fe + 0,059\2lg0,01 = -0,499B
ЭДС = Eкатода - Eанода = 0,7325 –(-0,499) = 1,23В
5)При температуре 500 С, нормальным давлением, р =4,03 г/л.Из какого числа атомов состоит молекула
3 и 4 я решил,но не знаю так или нет в 1 запутался, а 2 и 5 - условие там нормальное или не хватает чего-то Во 2 то явно ошибка, а вот 5 как считать по эти данным?? Помогите,пожалуйста проверить 3 и 4, и подсказать ход решения для 1 и 5????
-
Огромное спасибо
С последней помогите, пожалуйста
Сахарозу подвергните гидролизу. Для полученных соединений напишите реакции с избытком фенилгидразина до соответствующих озазонов. Что образуется при гидролизе озазонов?
C12H22O11 + H2O = C6H12O6 + C6H12O6
(Гидролиз сахарозы)
Очень даже ко двору!!! Спасибо большое! Вот то что здесь вверху сочинял что получится, но мои находки забраковали Вообще не очень понятно чем будут отличаться реакции для глюкозы и фруктозы
-
(-CH(CH=CH2)-CH2-)n
Не очень понятна структура этого вещества особенно СН2 в скобках?? Или СН=СН2 отходит от СН ????
-
Огромное спасибо
С последней помогите, пожалуйста
Сахарозу подвергните гидролизу. Для полученных соединений напишите реакции с избытком фенилгидразина до соответствующих озазонов. Что образуется при гидролизе озазонов?
C12H22O11 + H2O = C6H12O6 + C6H12O6
(Гидролиз сахарозы)
-
В пром-сти этилбензол получают гл. обр. алкилированием бензола этиленом в присут. А1С13 при т-ре 400-450 °С
Спасибо еще раз
C6H5CH2Cl --(Cl2,FeCl3)--> м-хлорбензилхлорид Вот здесь наверное вместоC6H5CH2Cl - C6H5CHCl2 ??
C6H5CHCl2 --(Cl2,FeCl3)-->C6H4(Сl)CH2Cl Так?
-
19а. Получите дивинил конденсацией ацетилена с формальдегидом (спо-соб В. Реппе) и напишите схемы реакций его 1,2- и 1,4-полимеризации. Какое строение имеет цис-1,4-полидивинил?
19б. Из пропилового спирта получите пропин и введите конечный продукт в реакции гидратации и гидрохлорирования.
Третьи задания
37а. Как получить этилбензол, исходя из бензола? Какое соединение образуется при гидрировании этилбензола? Подействуйте на этилбензол концентрированной азотной кислотой (1 моль) в присутствии серной кислоты, перманганатом калия (окисление).
Помогите, пожалуйста, с этими 3-мя заданиями
93а. Сахарозу подвергните гидролизу. Для полу-ченных соединений напишите реакции с избытком фенилгидразина до соответствующих озазонов. Что образуется при гидролизе озазонов?
C12H22O11 + H2O = C6H12O6 + C6H12O6
(Гидролиз сахарозы)
57б. Из толуола в ряд стадий получите м-хлорбензальдегид. На м-хлорбензальдегид подействуйте гидросульфитом натрия, гидроксиламином. Напишите уравнения всех этих реакций.
Еще вот эти задания я сделал но мне их вернули
H3C-CH2-CH2OH (AI2O3,t ) --> H3C-CH=CH2 + H2O
H3C-CH=CH2 + Br2 (CCI4)--> H3C-CH(Br)-CH2Br
H3C-CH(Br)-CH2Br + 2KOH --> C3H4 + 2KBr + 2H2O
C3H4 + H2O (Hg+2в H2SO4) --> H3C-CO-CH3
C3H4 + HCI --> H3C-C(CI)=CH2
C3H4 + 2HCI --> H3C-C(CI)2-CH3
Спасибо большое, с остальными сможете помочь?
-
19а. Получите дивинил конденсацией ацетилена с формальдегидом (спо-соб В. Реппе) и напишите схемы реакций его 1,2- и 1,4-полимеризации. Какое строение имеет цис-1,4-полидивинил?
19б. Из пропилового спирта получите пропин и введите конечный продукт в реакции гидратации и гидрохлорирования.
Третьи задания
37а. Как получить этилбензол, исходя из бензола? Какое соединение образуется при гидрировании этилбензола? Подействуйте на этилбензол концентрированной азотной кислотой (1 моль) в присутствии серной кислоты, перманганатом калия (окисление).
Помогите, пожалуйста, с этими 3-мя заданиями
-
Теперь понятно.
Для изобарно-изотермических процессов (Р,Т=const) тепловой эффект равен изменению энтальпии системы, т.е. Q =ΔH (но ваш препод из курса "общей химии" считает Q = -ΔH)
Спасибо Вам большое
-
Тогда у меня другой вопрос: Откуда вы свой вопрос выкопали?
В физической химии нет Q, есть Qp или Qv (в приложении к химическим реакциям). И не может быть связи Q = —ΔH (см. пост #2)
Хотя формально, исходя из 1-го начала термодинамики, на ваш вопрос можно ответить так Q = ΔH при Р,Т=const
Может Q = --ΔH при Р и Т = const?
-
Тогда у меня другой вопрос: Откуда вы свой вопрос выкопали?
В физической химии нет Q, есть Qp или Qv (в приложении к химическим реакциям). И не может быть связи Q = —ΔH (см. пост #2)
Я тоже не виноват что у нас в тесте пишут При каких условиях Q = -ΔH и 5 ответов 1 из них верный, но надо объяснить почему он выбран а)V - const б)V,P в)Т,Р г)V,P д)V,P,T - const Я думаю подходит б),но как объяснить почему этот ответ подходит а все остальные нет - не знаю,поэтому и спрашиваю
-
Повторяю: Вы сначала определитесь, по какому предмету вопрос.
Прочитайте отредактированный пост #2
Вопрос по физической химии А разве есть разница по какому разделу химии вопрос,если эти две величины должны быть связаны единственно правильным образом друг с другом в зависимости от PVT Я только это и пытаюсь выяснить Я так и назвал свою тему!!
-
Вы сначала определитесь, по какому предмету вопрос.
В "Общей химии": Q=-ΔH
В "Физической химии": Qp=ΔH (P=const), Qv=ΔU (V=const), причем Q - положительная, если система получает теплоту, и Q - отрицательная, если система отдает теплоту
Вопрос по термохимии или термодинамике, мне важно объяснить почему при условии постоянства или V или P Или T или их сочетания это равенство будет соблюдаться обязательно!!!
-
Подскажите, пожалуйста, никак не могу найти
При каких условиях Q = -ΔH ????
При Р,Т =const, при V,P,T = const или при других???
И почему?????
-
[H+] = (K*C)^1/2
Это из этой формулы выводится??
Тогда что, получается что [H+] = α ???
-
Вроде я понял ошибку Такое решение??
CaSO4 = SO3 + CaO
2,1г 6,11кДЖ
136г Х кДж
Q = 136*6,11\2,1 = 395,7кДж
CaSO4 = SO3 + CaO – 395,7кДж
∆Hх.р. = -Q = 395,7 кДж
∆Hх.р. = ∆H(СаO) + ∆H(SO3) - ∆H(CaSO4)
∆H(CaSO4) = ∆H(СаO) + ∆H(SO3) - ∆Hх.р. = -635,5 -395,2 -395,7 = -1426,4кДж\моль
Забыл что нашел Q а не ∆H Решение теперь правильное??
Еще одна задача решается также но не могу найти энтальпию диборана чтобы проверить
2)Определите энтальпию образования диборана(B2H6), если при сгорании 50мл(н.у.) его с образованием оксида бора и жидкой воды выделилось 4,84кДж тепла. Энтальпия B2O3 = -1281,6кДж/моль
В2Н6 + 3О2 = В2О3 + 3Н2О
0,05 л 4,84кДж
22,4 л Х кДж
Q = 22,4*4,84\0,05 = 2168,32 кДж
В2Н6 + 3О2 = В2О3 + 3Н2О + 2168,32 кДж
∆Hх.р. = -Q = -2168,32кДж\моль
∆Hх.р. = 3*∆H(Н2Oж) + ∆H(В2O3) - ∆H(В2Н6) – 3*∆H(О2)
∆H(В2Н6). = 3*∆H(Н2Oж) + ∆H(В2O3) - ∆Hх.р – 3*∆H(О2) = 3*(-285,84) – 1281,6 + 2168,32 – 3*0 = 29,2 кДж\моль
Правильно???
-
Ka = [H+]^2 / C
А можно пояснить почему [H+] взята во второй степени?
[H+] = (K*C)^1/2
Это из этой формулы выводится??
-
1. Ka = [H+]2 / C
α = (Ka / C)0.5
2. Cu(ClO4)2 - наименьшее
KClO2 - наибольшее
Ka = [H+]^2 / C
А можно пояснить почему [H+] взята во второй степени?
-
Проверьте, пожалуйста, задача простая вроде, она просто не подходит под табличные значения??
Вроде я понял ошибку Такое решение??
CaSO4 = SO3 + CaO
2,1г 6,11кДЖ
136г Х кДж
Q = 136*6,11\2,1 = 395,7кДж
CaSO4 = SO3 + CaO – 395,7кДж
∆Hх.р. = -Q = 395,7 кДж
∆Hх.р. = ∆H(СаO) + ∆H(SO3) - ∆H(CaSO4)
∆H(CaSO4) = ∆H(СаO) + ∆H(SO3) - ∆Hх.р. = -635,5 -395,2 -395,7 = -1426,4кДж\моль
Забыл что нашел Q а не ∆H Решение теперь правильное??
-
Определите энтальпию образования сульфата Са, если при разложении 2,10г его на оксиды поглощается 6,11 кДж
CaSO4 = SO3 + CaO
2,1г 6,11кДЖ
136г Х кДж
Нобр = 136*6,11\2,1 = 395,7кДж
Но так как энергия при образовании выделяется, то энтальпия образования будет с обратным знаком - 395,7 кДж\моль
Вроде все правильно посчитал, а почему разница с табличным значением ровно в 4 раза Что здесь не так??
Проверьте, пожалуйста, задача простая вроде, она просто не подходит под табличные значения??
-
Слили попарно следующие растворы:
а) 5%-ный хлорид бария и 4%-ный нитрат калия;
б) аммиачную воду и 5%-ную серную кислоту;
в) известковую воду и газированную минеральную воду;
г) 2%-ный нитрат серебра и 5%-ный нитрат бария;
д) известковую воду и аммиачную воду.
Для той пары растворов, при сливании которой образовался осадок, укажите молекулярную массу вещества в осадке
в) 100г
-
Для приготовления 500мл р-ра было взято 20,00мл хлороводородной кислоты (плотность=1,19 г/см3). Вычислить молярную концентрацию полученного р-ра
По каким формулам решать?
предварительный ответ: 0,5000 моль/л
Не очень понятно что такое хлороводородная кислота в чистом виде, но так как дано mHCl = 20*1,19 =
nHCl = m\M
Cm = n\V
У меня получилось 1,254 моль\л
-
Определите энтальпию образования сульфата Са, если при разложении 2,10г его на оксиды поглощается 6,11 кДж
CaSO4 = SO3 + CaO
2,1г 6,11кДЖ
136г Х кДж
Нобр = 136*6,11\2,1 = 395,7кДж
Но так как энергия при образовании выделяется, то энтальпия образования будет с обратным знаком - 395,7 кДж\моль
Вроде все правильно посчитал, а почему разница с табличным значением ровно в 4 раза Что здесь не так??
Где я ошибся??
-
Екатода = Еанода
ЕFe + 0,059\2lg0,001 = ECu + 0,059lgX
Ищите Х
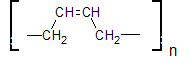
ЭДС, электролиз, рН
в Решение заданий
Опубликовано · Изменено пользователем ВНС
5)При температуре 500 С, нормальным давлением, р=4,03 г/л.Из какого числа атомов состоит молекула
Вот эту задачу можно решить или дмало, и по каким формулам??