-
Постов
660 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Nimicus
-
-
17 минут назад, Kingest16 сказал:
А ответ P2O4 не подходит
Я перемудрил - если соотношение элементов 1:2,25 = 4 : 9, то это P4O9 - такой оксид есть.
-
41 минуту назад, Kingest16 сказал:
Установите брутто-формулу оксида фосфора, в котором массовая доля кислорода равна 53,73%.
В ответе укажите химическую формулу.
P:O=(46.27/31):(53.73/16)=1.49:3.36=1:2.25
Помогите найти ошибку. Ответы PO2 и P2O4 не подходят
Надо проверить другие изотопы элементов. У фосфора больше нет стабильных изотопов, а у кислорода есть - 18O. Если посчитать с учетом этого, то получится мольное соотношение элементов 1:2 = 2:4, т.е. P218O4
-
Ставлю на то, что автор задумывал окисление α-бромкумола до бензойной кислоты.
Но не уверен, что на практике так и будет: чтобы боковой алкильный заместитель окислился до COOH, он должен содержать хотя бы один атом водорода в α-положении. В α-бромкумоле нет атома водорода в α-положении, но теоретически там возможна замена брома на OH, потом дегидратация, всякие окисления-расщепления и в итоге бензойная кислота все-таки получится.-
 1
1
-
-
2 минуты назад, Carryn сказал:
Спасибо! То есть это не вклад фенолята у которого +I на орто?
Не думаю, потому что степень диссоциации фенола в том же хлороформе или ДМСО очень мала, фенолята там просто нет по сути.
-
10 часов назад, Carryn сказал:
Значения сигналов орто/пара-протонов в феноле зависят от растворителя - если в CDCl3 разница между сигналами составляет 0.1 м.д., то в ДМСО-d6 - всего 0.01 м.д., т.е. они по сути равны. Сигнал орто-протонов действительно выходит в чуть более сильном поле, чем сигнал пара-протонов (хотя можно было бы ожидать обратного по обозначенным вами причинам) - я бы объяснил это экранирующим влиянием неподеленных электронных пар кислорода.
-
1 час назад, Диана М. сказал:
Забыла добавить,что синтез нужно провести не длиннее, чем в 5 стадий
Я бы на это глянул, где не длиннее чем 5 стадий делается???
-
54 минуты назад, Paul_S сказал:
Да, точно. Там, где по-взрослому, в органических цепочках такие мелочи, как нейтрализация, не считают за стадию.
Согласен.
-
25 минут назад, Paul_S сказал:
В верхней цепочке SnCl2 восстановит п-нитроанилин до п-диаминобензола. Если на следующей картинке продолжение, то это странно, с едким натром он не должен реагировать. Может быть, авторы считали, что нитроацетанилид гидролизнется до п-нитрофенола, тогда нитрофенол востановится в аминофенол, который даст со щелочью п-аминофенолят натрия. Но это должно в очень жестких условиях происходить, гидролиз п-нитроанилина до фенола.
Во второй цепочке нитробензол восстанавливается железом в соляной кислоте в соль анилина, действием щелочи получают свободный анилин, дальше PhNH2 + OCHPh -> PhN=CHPh + H2O; PhN=CHPh + H2/Ni -> PhNH-CH2Ph; PhNH-CH2Ph + HNO2 -> PhN(NO)-CH2Ph + H2O
Т.к. среда кисля, то образуется дигидрохлорид п-диаминобензола, а на следующей стадии при обработке щелочью эта соль будет разлагаться, давая свободный диамин.
-
34 минуты назад, Paul_S сказал:
Ну, может быть. Но из пропила сделать пропилен термодинамически легче.
В данном случае реакция необратима и ее направление определяется не термодинамикой (устойчивостью продуктов), а кинетикой (энергией активации, устойчивостью переходного состояния). Переходное состояние в случае отщепления водорода в этильной группе должно быть более устойчивым (легче образуется), чем переходное состояние при отщеплении водорода в пропильной группе (из-за стерики), поэтому преимущественное направление реакции - образование этилена, диметиламина и воды (если разница в энергиях активации невелика и синтез проводится при высоких температурах, то образование пропилена, диметилэтиламина и воды также будет протекать, просто с меньшей скоростью и, соответственно, меньшим выходом).
-
14 минут назад, Paul_S сказал:
Подозреваю, что имелась в виду просто реакция с азотистой кислотой. Гексанол отделяется на делительной воронке и переводится в амин реакцией с аммиаком под давлеием или переводом в гексилгалогенид с послед. р-цией с аммиаком.
Вполне возможно!
-
-
Смесь можно обработать избытком водного раствора щелочи и прибавить п-толуолсульфохлорид - гексиламин (первичный амин) образует при этом растворимую соль сульфамида, а триэтиламин (третичный амин) реагировать не будет - его можно проэкстрагировать подходящим растворителем и, отогнав растворитель, получить чистый амин. Водную фазу, содержащую сульфамид, можно подкислить и покипятить - при этом сульфамид гидролизуется до амина (в виде соли). После обработки раствора щелочью, экстракции и отгонки растворителя можно получить чистый гексиламин.
-
Элиминирование по Гофману
-
-
19 минут назад, Elzw сказал:
Это понятно. Но вопрос в том, как, например, изначально проаминировать тиофен?
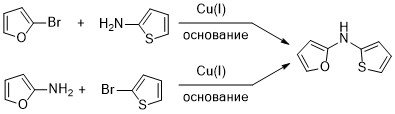
Можно тиофен пронитровать до 2-нитротиофена и восстановить его до амина. Либо бромировать тиофен до 2-бромтиофена и ввести в реакцию с аммиаком в условиях реакции Ульмана
-
 1
1
-
-
Напрашиваются два альтернативных варианта реакции Ульмана

-
 1
1
-
-
3 часа назад, M_GM сказал:
... -дион-3,4
Селин-Дион-3,4???
-
 1
1
-
-
-
6 минут назад, katerina678 сказал:
1. Дати назву за раціональною номенклатурою сполукам: CH 3 a) CH 3 -C S-CH 3 CH 3 CH 3 6) CH 3 -C-CH=CH-CH 2 -C CH H-CH 3 CH 3 CH 3
Это что вообще такое, простите?
-
9 часов назад, Александр-chem сказал:
Потом получится CH3-C(Cтройная связьC-CH3)(CH3)-CH=CH2
Но вряд ли так получится, вдобавок потом H2 1 моль добавляют
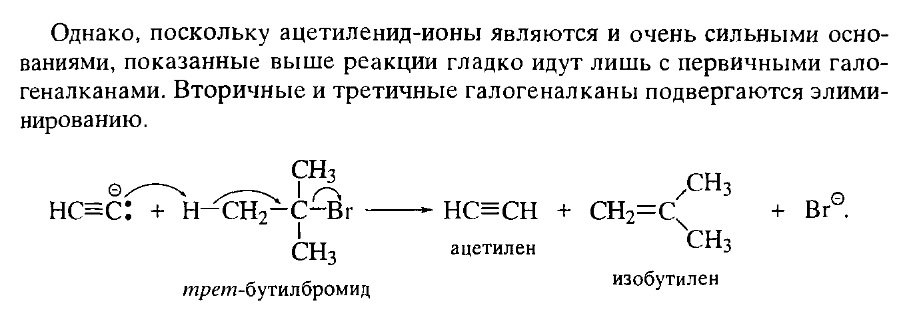
Взаимодействие ацетиленидов со вторичными и третичными галогеналканами сопровождается элиминированием, а не замещением

-
3 часа назад, Александр-chem сказал:
Здравствуйте! Подскажите, пожалуйста, как идёт это реакция?
CH3 -CH(CH3)-CH=CH2 + Br2 (на свету) —>
а вторая реакция +NaCтройная связьC-CH3 —>
CH3-CH(CH3)-CH=CH2 + Br2 (на свету) —> CH3-C(Br)(CH3)-CH=CH2 + HBr
CH3-C(Br)(CH3)-CH=CH2 +NaC☰C-CH3 —> CH2=C(CH3)-CH=CH2 + HC☰C-CH3 + NaBr
-
26 минут назад, Alex-chem сказал:
Хорошо, спасибо
CH3-CH(CH3)-CH2–CH2-CH(CH3)-CH2-CH3 +HNO3 —> CH3-CH(CH3)-CH2–CH2-(NO2)C(CH3)-CH2-CH3 + CH3-(NO2)C(CH3)-CH2–CH2-CН(CH3)-CH2-CH3 +H2O???
Да
26 минут назад, Alex-chem сказал:CH3-CH(CH3)-CH2–CH2-(NO2)C(CH3)-CH2-CH3 +Sn +HCl —> CH3-CH(CH3)-CH2–CH2-(NH2)C(CH3)-CH2-CH3???
извините, гидрохлориды я не знаю, что это такое, поправьте, пожалуйста, если я реакцию неправильно написал.
Да, но можно просто упрощенно Sn + HCl заменить на [H], как в условии на схеме реакции, тогда можно про гидрохлориды забыть. Вот так будет (для второго изомера - аналогично):
CH3-CH(CH3)-CH2–CH2-(NO2)C(CH3)-CH2-CH3 + 6[H] —> CH3-CH(CH3)-CH2–CH2-(NH2)C(CH3)-CH2-CH3 + 2H2O-
 1
1
-
-
7 минут назад, Alex-chem сказал:
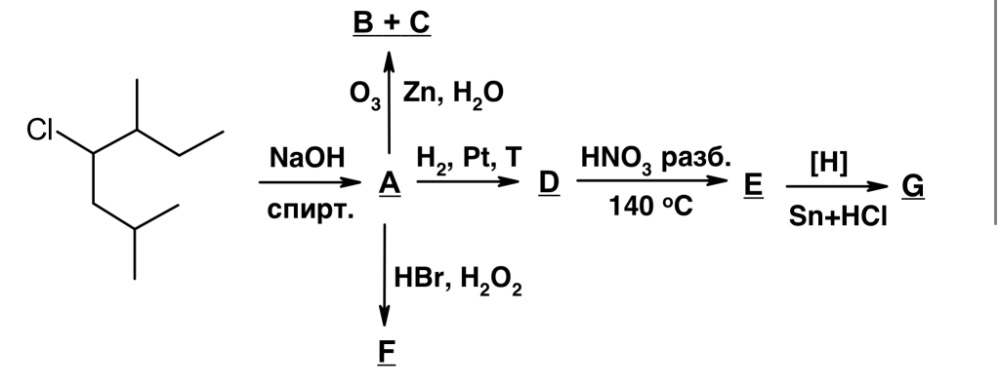
Здравствуйте! Правильно я решил? Помогите,пожалуйста, помочь с G) реакции, не пойму как она идёт.
1) CH3-CH(CH3)-CH2–CH(Cl)-CH(CH3)-CH2-CH3 +NaOHспирт —> CH3-CH(CH3)-CH2–CH=C(CH3)-CH2-CH3 +NaCl+H2O
2) CH3-CH(CH3)-CH2–CH=C(CH3)-CH2-CH3 +O3,Zn,H2O —> CH3-CH(CH3)-CH2-C(O)H + CH3-C(O)-CH2-CH3+H2O2
3)CH3-CH(CH3)-CH2–CH=C(CH3)-CH2-CH3 + HBr+H2O2 —> CH3-CH(CH3)-CH2–CH-(Br)-CH(CH3)-CH2-CH3
4)CH3-CH(CH3)-CH2–CH=C(CH3)-CH2-CH3 +H2 —> CH3-CH(CH3)-CH2–CH2-CH(CH3)-CH2-CH3
5)CH3-CH(CH3)-CH2–CH2-CH(CH3)-CH2-CH3 +HNO3 —> CH3-CH(CH3)-CH2–CH2-(NO2)C(CH3)-CH2-CH3 +H2O
Верно, но в реакции 2 не образуется H2O2 (эту реакцию лучше записывать в виде схемы, указывая только органические продукты). В реакции 5 (нитрование) образуется как минимум еще одно изомерное третичное нитропроизводное. Далее эти нитропроизводные E восстанавливаются до соответствующих аминов G (в виде гидрохлоридов)
-
Тут ніхто за вас вирішувати завдання не буде, максимум підкажуть якісь спірні моменти. Раджу звернутися в розділ "Робота" і замовити рішення завдань за гроші, якщо самі не в змозі зробити

.thumb.jpg.57673d9b078af8ea6b76813bd85797f0.jpg)
Вакуумный насос для роторного испарителя.
в Химическая технология
Опубликовано · Изменено пользователем Nimicus
Для водно-спиртовых растворов и каких-то более-менее тяжелых бромалканов, ДМСО 100 мбар будет маловато. А масляный насос для этих целей слишком глубокий вакуум даст, так что нужен мембранный насос с более глубоким вакуумом и возможностью регулировать давление, мне кажется