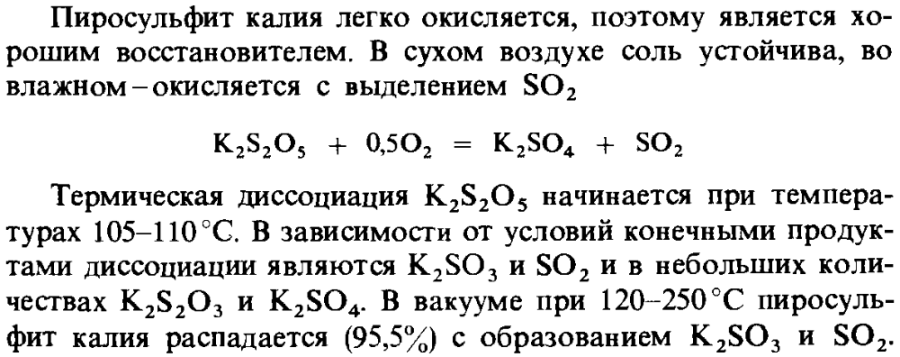-
Постов
1890 -
Зарегистрирован
-
Посещение
-
Победитель дней
6
pauk стал победителем дня 22 мая
pauk имел наиболее популярный контент!
Информация о pauk
Старые поля
-
Пол
Мужчина
Посетители профиля
26045 просмотров профиля
Достижения pauk
-
Ich habe энное количество чистой газовой серы, которую я натырил взял в бессрочную безвозмездную аренду на заводе, где когда-то трудился в поте лица. На вид это мелкий жёлтый пылящий порошок, он получается в процессе очистки природного газа от сероводорода методом Клауса, а у нас он применялся как вулканизатор резино-технических смесей. Если насыпать кучку этой серы и поджечь, то она медленно горит с поверхности маленьким синим пламенем, плавясь и чернея. Кроме вони никакого дыма при этом не выделяется, хотя есть ощущение, что воздух становится слегка мутноватым, так как примесь серного ангидрида в нём таки есть; также возможно, что какая-то часть серы возгоняется, а потом конденсируется в виде мельчайших частичек.
-
1. Ставят в широкий сосуд (например, в кристаллизатор) два стакана на расстоянии 10-20 см друг от друга и наполняют их до краёв растворами двух солей, которые при обменном взаимодействии образуют нерастворимый осадок. Затем кристаллизатор осторожно, стараясь не допустить перемешивания растворов, заполняют чистой водой с таким расчётом, чтобы уровень воды находился на несколько миллиметров выше верхнего края стаканов. После чего кристаллизатор закрывают стеклом и оставляют в покое. Через некоторое время (дни, недели) за счёт диффузии ионов в пространстве между стаканами образуются более-менее сформированные кристаллы нерастворимого вещества. Для каждой пары солей можно эмпирическим путём подобрать наиболее оптимальные условия (концентрации растворов, расстояние между стаканами). Понятно, что для сильно гидролизующихся солей этот метод не подходит. 2. Скачайте из интернета книжку Г. Гениша "Выращивание кристаллов в гелях" (1973) и попробуйте этот метод. Может, удастся что-нибудь вырастить, если не эти кристаллы, так какие-нибудь другие.
-
Если качество исходного PDF-файла меня устраивает, то я загружаю его в онлайн-конвертер PDF --> DjVu. Вариантов здесь много, забейте в поисковик "конвертер из pdf в djvu" и увидите, что наряду с онлайнами встречаются и проги, которые можно установить на компьютер. Но я обычно использую старый добрый Any2DjVu Server, который хорош тем, что может автоматически выбирать наиболее оптимальный режим кодировки для каждой страницы, в зависимости от её контента (текст, фотографии, иллюстрации). Поэтому размер выходного файла в нём обычно меньше, чем во многих других онлайн-конвертерах, которые кодируют все страницы под одну гребёнку. Нехорош он тем, что за редкими исключениями отказывается конвертировать файлы размером больше 20-30 Мб. Иногда отказывается конвертировать файлы, сообщая о некоей внутренней ошибке в файле. Ещё он не принимает файлы с кириллическими символами в названии, их приходится предварительно переименовывать какой-нибудь латинской буквой или цифрой. Наконец, опция введения в файл OCR-слоя хорошо работает для текстов на английском языке, а для текстов на русском языке получается белиберда, поэтому для OCR я использую другие средства. Если исходный файл PDF или DjVu меня не устраивает, или же если с помощью конвертера мне не удалось добиться желаемого качества выходного файла, то я разбираю страницы исходника на картинки формата BMP, для чего существует немало средств, от простых утилит до мегапакетов. После чего обрабатываю картинки графическим редактором либо в пакетном режиме, либо постранично, либо и так, и этак в зависимости от их степени паршивости. Далее собираю все картинки в единый файл редактором DjVu-файлов и напоследок в качестве бонуса добавляю к нему прибамбасы в виде закладок и OCR. Что касается конвертирования DjVu --> PDF, то я делаю это исключительно редко, так как вектор в моей башке направлен ровно в обратную сторону. Поэтому для этой цели мне вполне хватает простой утилиты STDU Viewer с подключенным модулем STDU Converter.
-
Разница объёмов жидкости (V-V0) позволяет вычислить только объём образца металла. Чтобы вычислить плотность, надо знать ещё его массу. Формула: ρ = m/(V-V0). Верёвочка здесь не поможет. Нужны весы.
-
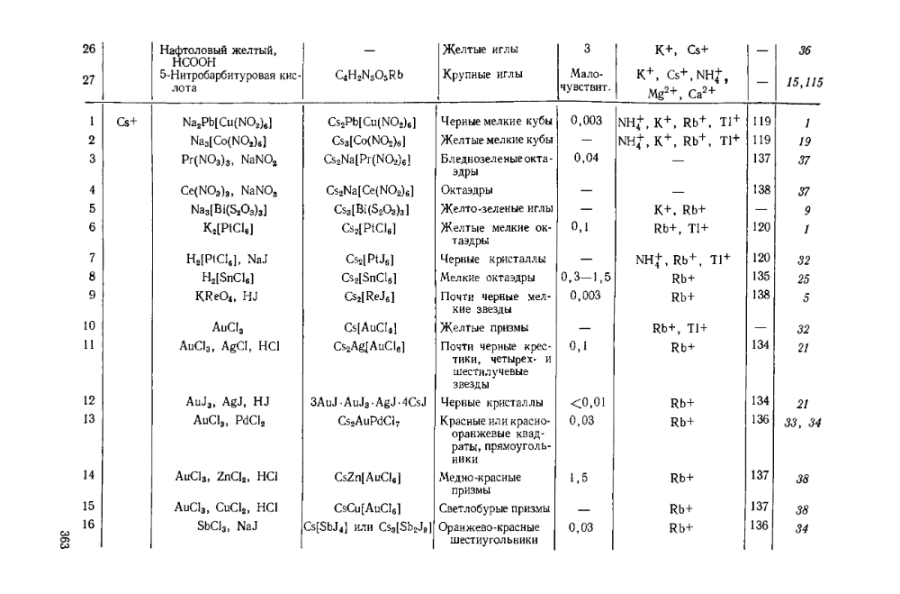
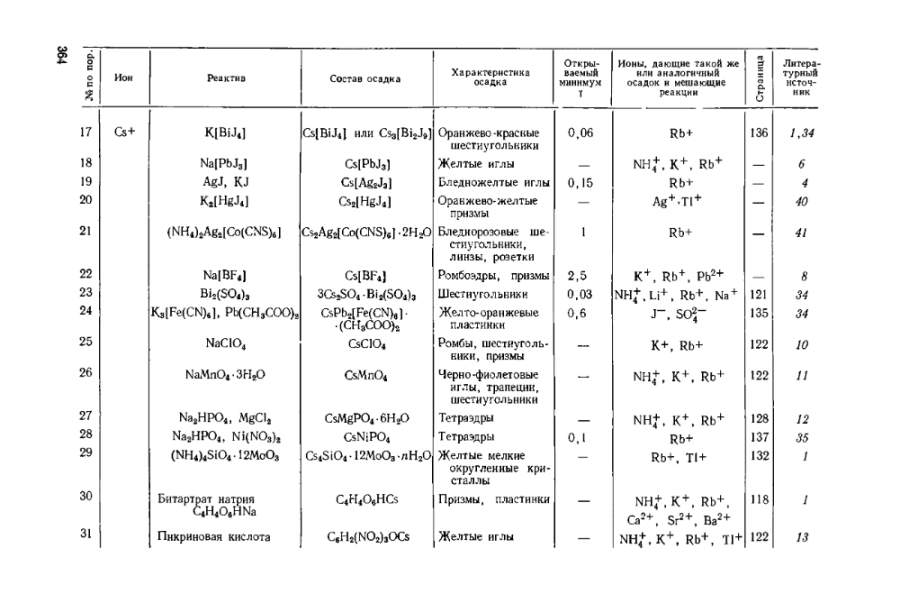
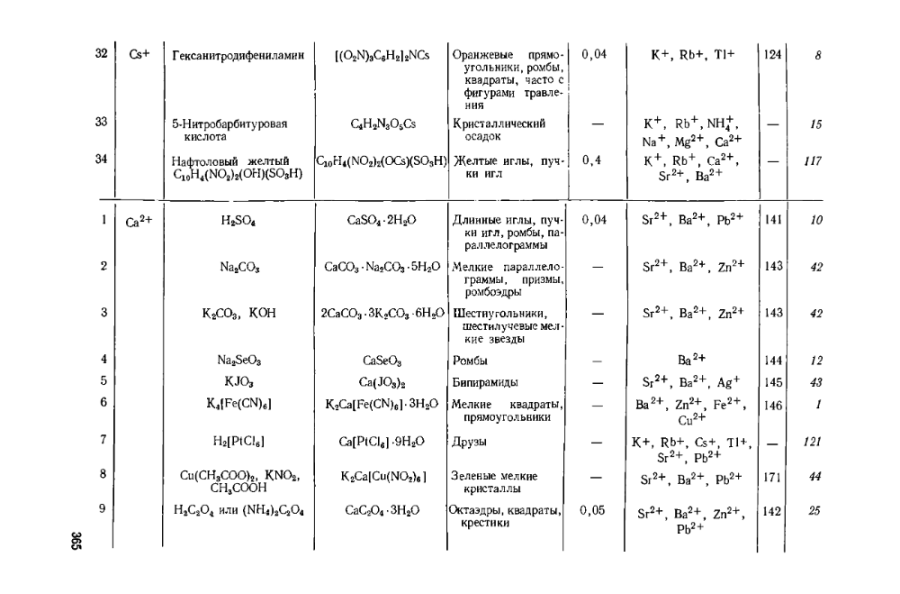
Работа над перекодированием файла в DJVU идёт ни шатко, ни валко, поэтому для особо страждущих приведу фрагмент сводной таблицы, касающийся реакций на цезий. Как видите, только горячо пропагандируемый мною метод с использованием солей РЗЭ свободен от влияния мешающих ионов, тогда как для остальных методов всегда найдётся какая-нибудь зараза, мешающая процессу определения.
-
Стеараты 2-валентных металлов вводятся в пластмассы как смазывающие и антиадгезионные присадки. Они уменьшают трение и прилипание к поверхности изделий из пластмассы, в том числе слипание их друг с другом при хранении, что улучшает их эксплуатационные качества и увеличивает срок службы.
-
WO3 не пойдёт. Несмотря на довольно высокое значение температуры кипения (1700°С), он начинает заметно возгоняться уже при 800°С, а при 1000°С и выше восстанавливается углеродом до металла. Возможно, сгодится B2O3, который нелетуч при высоких температурах и начинает реагировать с углеродом только около 2000°С. Однако меня терзают смутные подозрения насчёт возможности реакции Ca3(PO4)2 + 4B2O3 = 3Ca(BO2)2 + 2BPO4, из-за которой все старания могут пойти коту под хвост.
-
26. P. B. Sarkar a. Goswani, J. Ind. Chem. Soc., 12, 608 (1935) Картинка скопирована со стр. 137-138 книги Коренмана "Микрокристаллоскопия" (1955), которая есть на Либгене, ссылка здесь. Для скачивания предлагаются две PDF-версии циклопических размеров, что меня как ярого приверженца DJVU категорически не устраивает, поэтому я сейчас перегоняю файл в свой любимый формат и в ближайшем будущем планирую представить его в разделе "Книги". Разумеется, здесь приведено описание микрокристаллоскопического метода, ибо для того, чтобы наблюдать образование осадка в капле раствора, требуется либо микроскоп, либо соколиный глаз. Но думаю, что его можно приспособить под обычный полумикрометод. Кремни я помянул на тот случай, если в распоряжении нет солей РЗЭ. Состав кремней для зажигалок примерно следующий (%): Fe 18-19; Ce 49-51; La 26-34; Nd 0-10; Pr 4-7; Mg 3-4. Для тех, кто пойдёт этим кремнистым тернистым путём: а) после растворения кремней в кислоте нужно будет освободить раствор от железа тем или иным способом, так как сосуществование в растворе ионов железа и нитрита не есть гуд, я считаю; б) чистый светло-зелёный цвет осадка с этим составом не получится, так как празеодима в нём с гулькин нос.
-
Цезий непросто открыть в присутствии мешающих ионов K+, Rb+, NH4+ и некоторых других. Стандартного набора реактивов для этого явно недостаточно. Придётся изощряться. Относительно простой реактив для обнаружения цезия можно приготовить из раствора смеси солей РЗЭ, полученного при растворении в кислоте кремней для зажигалок.
-
Через несколько месяцев хранения свежий раствор гипохлорита заметно теряет активность, а через года он полностью "выдохнется", даже не будет пахнуть.
-
Надо думать, что значение 105-110°С относится к началу процесса термической диссоциации пиросульфита калия по реакции K2S2O5 <--> K2SO3 + SO2, тогда как 190°С - к его сходу на нет, когда начинают преобладать другие, более сложные процессы. Для сравнения приведу данные из той же книжки для термической диссоциации пиросульфита натрия (к сожалению, для калия таковых нема). PS. 1 кПа = 7,5 мм рт. ст., если кто забыл.
-
В книжке "Технология сульфитов" (Авербух Т. Д. и др., 1984) пишут, что пиросульфит (дисульфит) калия K2S2O5 начинает разлагаться при 105-110°С. То бишь разницы с натриевой солью практически нет. Влажная соль легко окисляется кислородом воздуха, поэтому сушку её надо вести в вакууме или в защитной атмосфере (азот) при несильном нагреве.
-
ХИМИК-АНАЛИТИК, ПОМНИ: Качественный анализ - это некачественно выполненный количественный анализ. Любишь качественный анализ, люби и количественный.
-
Рекомендую вам скачать две книги В. А. Батыревой с соавторами: "Синтезы соединений редкоземельных элементов", ч. 1, 1983 и ч. 2, 1986. По охвату материала лучше их вы вряд ли найдёте. Файлы в форматах djvu и pdf есть на Либгене, по адресу https://libgen.st/search.php?req=батырева+синтезы&open=0&res=25&view=simple&phrase=1&column=def, но качество их весьма посредственное. Могу предложить свою версию 1-й части в формате djvu, приведённую в более-менее божеский вид с ровно обрезанными и очищенными страницами, закладками и OCR. До причёсывания 2-й части руки пока не дошли, поэтому вторая книга в архиве - это просто копипаст файла c Либгена. Ссылка на скачивание zip-архива из файлообменника действительна в течение 14 дней (https://dropmefiles.com/RataP). Свою версию файла я разместил также на ресурсе Химия и Химики, так что можно скачивать его оттуда (http://www.chemistry-chemists.com/forum/viewtopic.php?p=206654#p206654).