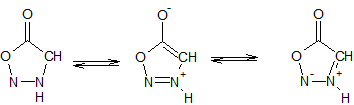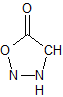-
Постов
34961 -
Зарегистрирован
-
Победитель дней
1166
Весь контент yatcheh
-
Ещё раз, уравнение реакции отражает только СООТНОШЕНИЕ в котором реагируют кислота и щёлочь. О КОЛИЧЕСТВЕ прореагировавшей кислоты и количестве оставшейся уравнение нам НИЧЕГО не говорит. Оно вообще ничего не говорит о количествах, только - о СООТНОШЕНИЯХ. Если уж кислота УЖЕ ПРОРЕАГИРОВАЛА, то она прореагировала с эквивалентом щёлочи, 1:1, и НИКАК иначе. Уравнение именно об этом.
-
В каком количестве они взяты - это совершенно не важно. 1 моль кислоты реагирует с 1 молем основания. Если мы взяли 100500 молей кислоты и 100500 молей основания, а прореагировал только 1 моль кислоты, он всё равно прореагировал точно с одним молем основания. Именно это и отражает уравнение реакции. Если вы толкуете о гидролизе (обратимости реакции), то в уравнении это отражается двойной стрелкой HNO2 + NaOH <=> NaNO2 + H2O Но в любом случае, если кислота УЖЕ прореагировала, то она прореагировала точно в соотношении 1:1.
-
Если греть насухую, то возможна реакция с циано-группой с образованием гидрохлорида бигуанида. R-CN + NH4Cl => R-C(-NH2)=NH*HCl
-
Формула корректна. Просто это одна из мезоформ Кстати - ароматическое соединение. Скажете - ионная связь учитывается, как валентная? Тогда азот в хлористом аммонии пятивалентен, а фосфор в гексафторфосфатах - семивалентен. Вам не кажется, что за пределами некоего магического круга понятие валентности начинает трещать по всем швам?
-
Сиднон. Это - фигня, вот когда я дитиолатами никеля работал - там в литературке до 2000-го года срач был по поводу - у кого там какая валентность. Идиоты... З.Ы. Ну, про 2000-й это я наврал в полемическом задоре, последняя статья там была середины 80-х.
-
Хрен там. Это вещество существует (веществует) именно в таком виде.
-
А тут сколько водородов не хватает? С утилитарной точки зрения тут достаточно теории паёв. Это не аргумент.
-
Так я об этом и кричу на всех углах! Оставьте валентность школьникам! Не тащите её как чемодан без ручки, не натягивайте эту сову на всякий глобус, не пытайтесь выдавить из неё то чего в ней никогда не было! А то - начинается, "какая валентность у азота в закиси?" Да никакая, блять! Да плевать мне на вашу личную позицию! Я с валентностью воевал всегда, и никогда не оставлю эту священную борьбу! Если бы мы срались на форуме в Риме - я бы вам морду набил, уважаемый! Тогда нравы проще были...
-
Вот - сразу видно химика, воспитанного на классическом механистическом детерминизме. "Абстрактный" - недостаточно сильный термин, абстракция должна быть "чистой", иначе - это просто игра скрытых параметров, не доступная пониманию, но проявляющая себя в натуре. Механизм - ничто, измерение - всё!
-
Ащ-щна! Вы так внаглую смешиваете абстрактное и конкретное, что этот суп даже в платоновском смысле - иррационален! "Валентность", если дойти до истоков термина, это синоним "возможности". Возможности в широком смысле слова - от физической возможности до онтологической. Изначально ограниченный чистыми отношениями чисел, он начал приобретать свойства физического описания реальности, но всегда оставался костылём, используемым для подпорки сиюминутной хромой гипотезы. Этому термину уже нельзя придать физический смысл - он полностью исчерпан. Его нельзя переформулировать - сама концепция не позволяет. З.Ы. "Абстрактная" химическая связь - это мощно, ящитаю! Два гения на один форум - это слишком, да...
-
Ваша личность меня категорически не устраивает!
-
А тут константы нужно использовать действующие, или для диссоциирующих форм? Особенно это актуально для угольной кислоты. У неё действующая и реальная константы отличаются на два порядка.
-
Ну, так и (NH4)2CO3 существует. Означает ли это, что надо поменять местами в ряду с уже поменянными местами и Na2CO3 с NH3?
-
Никак нельзя! Это магическая завеса, отделяющая неофитов от адептов и посвящённых в высшие тайны. Адептам доступна концепция координации, посвящённые оперируют Уравнением Шредингера.
-
Да, это вопрос. Хлор с хлористым аммонием реагирует. Ещё один вопрос - бромат аммония. Он в воде довольно мало растворим (11 г на 100 г). И весьма взрывчат. Если бромид-ион успеет первым, тогда возвращаемся к первому вопросу.
-
Бром кипит при 60C. Ничего не получится - улетит и то, и другое. Разделить такую смесь даже на хорошей колонке - проблема, а уж так... Попытка с негодными средствами Зачем тут вообще дихлорметан? Растворы можно взять не столь концентрированные, бром всё равно осядет слоем.
-
Ага, щаз! Я с тобой на одном гектаре срать не сяду, не то что - беседовать. Шулер ты, тебе канделябром по бакенбардам - в самый раз.
-
Кстати - ещё один пример шулерства. Шизума, а что ж ты привёл только начало статьи в энциклопедии? Дальше неудобные вещи всплывают? Гондон ты штопанный...
-
Для учеников школы - это значит для тебя, недоросль Ты сначала читать научись.
-
А ты поищи, долбайоб
-
Обратите внимание - это шулер, ляпнув очевидную чушь будет биться фейсом об тейбл, но не признает, что просто ляпнул чушь. С ним невозможно вести никакую беседу, никакую дискуссию, это действительно - что-то психиатрическое. Я тебе про определение "стехиометрической валентности" толковал, которой коллега chemister2010 пытался хоть как-то объяснить этот твой пердимонокль. Но ты же - тетерев. Читать не умеешь.
-
Да, там слово "стехиометрическОЙ" Придурок.