-
Постов
660 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Nimicus
-
-
-
У меня получилось 122.6 г
Приведите свое решение, чтобы можно было сказать, правильно или нет. И правильный ответ, на всякий случай -
1 час назад, Ксения13 сказал:
Потому что по условию в полученной смеси соотношение органических веществ 2:3 по молям (в порядке увеличения молярных масс). Молярная масса фенола меньше молярной массы фенолята натрия, поэтому фенол в меньшем количестве и количество фенолята в полученной смеси = 0.2 моль x 3/2 = 0.3 моль
-
Также можно порешать архив заданий Санкт-Петербургской олимпиады по химии (https://olimpiada.ru/activity/247/tasks)
-
Здравствуйте!
Ищу книгу Ненайденко В.Г., Гладилин А.К., Беклемишев М.К. "Менделеевская олимпиада. Задания теоретических туров 2002-2019" (под ред. академика РАН В.В. Лунина). Может быть, кто-то знает, ее можно достать? -
Конкретные сборники не посоветую, но считаю, что полезным будет обратить внимание на архив заданий Всероссийской олимпиады по химии различных этапов (https://olimpiada.ru/activity/76/tasks), Московской городской олимпиады и олимпиады "Ломоносов" (http://www.chem.msu.ru/rus/olimp/), а также на этот сайт, где собраны относительно давние задания самых разных олимпиад, в том числе уровня региона (http://tasks.ceemat.desc.ru/dir/124/?catalog_depth=-1)
-
31.01.2021 в 11:30, KSENIA99 сказал:
спасибо большое)
а с реакцииями отличающие соединения верно указала?
Первые две реакции правильные, а третья (с реактивом Гриньяра) - нет. Вместо нее нужно написать йодоформную пробу (качественная реакция на метилкетоны и метилкарбинолы). Метилбутанон будет давать положительную пробу (реагировать с образованием йодоформа), а 3-метилбутаналь - нет
-
В заданиях 1 и 2 у меня такие же ответы. В реакции магния с азотной кислотой образуется нитрат магния, азот (простое вещество) и вода:
Mg + HNO3 ---t---> Mg(NO3)2 + N2 + H2O
Уравнивая методом электронного баланса, получаем:
5Mg + 12HNO3 ---t---> 5Mg(NO3)2 + N2 + 6H2O-
 1
1
-
-
-
Масса смеси увеличивается за счет поглощения CO2, т.е. его масса = 8.8 г (0.2 моль). Из уравнения реакции видно, при этом образовалось 0.2 моль фенола, тогда в растворе осталось 0.3 моль фенолята и исходного количество его = 0.2 моль + 0.3 моль = 0.5 моль. Отсюда находим массу соли в исходном растворе и ее массовую долю.
-
12 минут назад, chemister2010 сказал:
Реакция Гофмана не пойдет с замещенным амидом. Там промежуточно должен образоваться изоцианат по механизму.
Согласен, я не прав

-
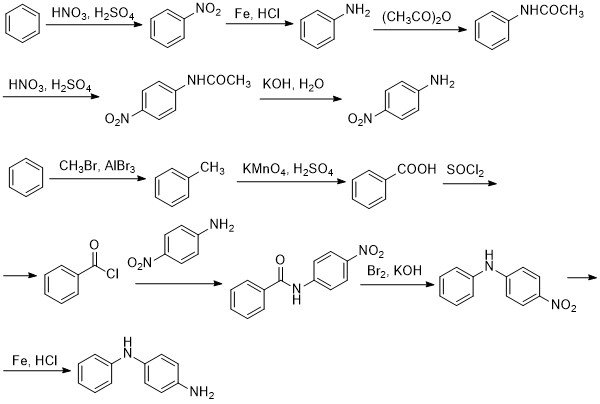
Могу еще предложить вот такую схему синтеза:

-
41 минуту назад, chemister2010 сказал:
Обычно идут проще: нитруют бензол, восстанавливают в дифенилгидразин и перегруппировывают в 4-аминодифениламин.
А как так будет дифенилгидразин перегруппироваться в 4-аминодифениламин, если должен получаться бензидин? Или там какие-то особые условия, чтобы направить реакцию в нужное русло?
-
-
1 час назад, AlexS1r сказал:
Прошу прощения, но эта схема синтеза не подойдет, т.к. известно, что из-за сильного электроноакцепторного влияния NO2-группы нитробензол не вступает в ряд реакций электрофильного замещения, характерных для бензола - например, в реакцию Фриделя-Крафтса. -
4 минуты назад, yatcheh сказал:
Ладно, вы меня убедили. У меня не осталось аргументов.

Рано Вы сдались, я почти уверовал в ущербность методической основы данной задачи

-
10 минут назад, yatcheh сказал:
Кстати, в задаче ничего не сказано и о типе дегидратации. Если уж внутримолекулярная дегидратация невозможна (ну, ладно - затруднена), то что мешает протекать реакции межмолекулярной дегидратации? С образованием простого эфира?
NO2-C(CH3)2-CH(-C2H5)-O-CH(-C2H5)-C(CH3)2-NO2
Само по себе это одно задание не может и не должно откладывать в сознании тот факт, что 1,2-нитроспирты легко дегидратируются - на это должны быть
другие задания, я уверен. И в ней нет вещей, противоречащих здравому смыслу, так что не вижу смысла придираться)
Почему же оно не переживет дегидратацию, интересно? Ну или почему внутримолекулярная дегидратация затруднена? Вторичные спирты дегидратируются под действием 60-70%-ной серной кислоты при 90-100 градусах, и межмолекулярная дегидратация для них не характерна.
-
4 минуты назад, yatcheh сказал:
Такая дегидратация должна проходить в весьма жёстких условиях, как дегидратация обычного спирта. Поскольку водород, удалённый от нитро-группы ни чем не активирован. Сомнительно, что нитросоединение переживёт такие условия.
Ну, карбкатионов как таковых в моей схеме не предполагается, но - соглашусь с тем, что она страдает определённым гнутием ствола, и я на ней не настаиваю

Суть-то в том, что невнимательный ассистент придумал задачку, которая не имеет решения. Дегидратация продуктов реакции Анри (Генри) в алкены связана как раз с высокой кислотностью водорода возле нитро-группы. А тут его (водорода) просто нету

Почему же она не имеет решения? В задаче ничего не сказано про лёгкость или тяжесть дегидратации, и вообще. Да, если б это был какой-нибудь 1-нитропропан, то образующийся нитроспирт должен был бы легко подвергаться дегидратации с образованием нитроалкена даже в присутствии щелочи. А в данном случае у нас другой нитроспирт, но дегидратироваться он будет, в кислой среде)
Мне кажется, абсолютно нормальная задача)
-
2 минуты назад, yatcheh сказал:
(CH3)2C(-NO2)-CH(OH)-CH2-CH3
Тут для нормальной дегидратации нет никакой возможности, ввиду отсутствия водорода возле нитро-группы.
Теоретически тут может сигматропная перегруппировка иметь место, с образованием изоструктурного алкена.
Но насколько это реально - ХЗ

Почему же невозможна обычная дегидратация?

Такая дегидратация, как Вы нарисовали, маловероятна, т.к. при этом должен образовываться карбокатион, в котором катионный центр связан с NO2-группой, т.е. дестабилизированный. -
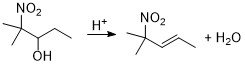
2-Нитропропан будет вступать в реакцию нитроальдольной конденсации с пропаналем в основной среде (в присутствии щелочи) при охлаждении. Полученный нитроспирт - 2-метил-2-нитро-3-пентанол - будет подвергаться дегидратации в кислой среде с образованием 4-метил-4-нитро-2-пентена
-
Первая реакция - образование метилгликозида по полуацетальной ОН-группе
вторая - метилирование всех остальных OH-групп
третья - гидролиз гликозида в кислой среде
четвертая - реакция серебряного зеркала, окисление альдегидной группы до карбоксильной
пятая - образование хлорангидрида кислоты
шестая - образование N-метиламида кислоты-
 1
1
-
-
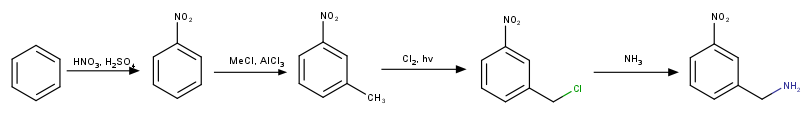
У меня получается вот так:

-
9 минут назад, AlexS1r сказал:
А если парциальное восстановление по Берчу?
Нет, думаю здесь такое совсем не к месту)
-
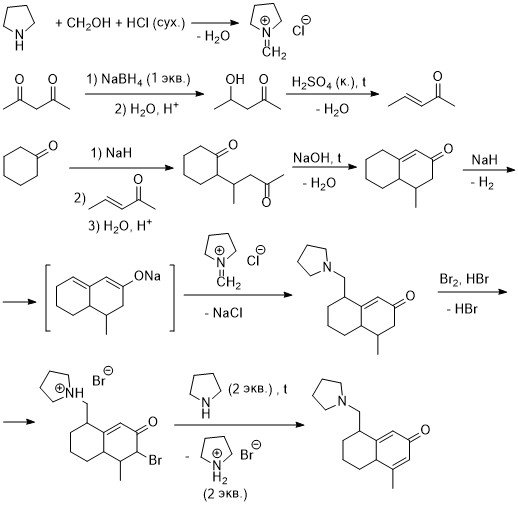
1 час назад, AlexS1r сказал:
Через Робинсона не получится?
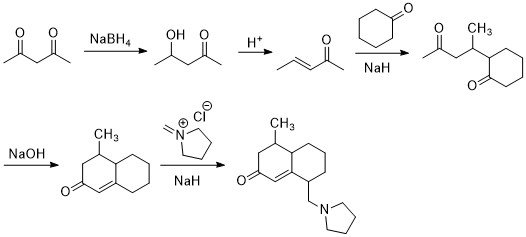
Вот думаю как-то через Робинсона, но все равно пока не могу сообразить. Получается пока вот такое, а как к целевому продукту перейти - не знаю


.thumb.jpg.57673d9b078af8ea6b76813bd85797f0.jpg)

sp-гибридизация
в Решение заданий
Опубликовано
Нет