-
Постов
660 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Весь контент Nimicus
-
Бромоформ можно получить из ацетона в одну стадию, с помощью галоформной реакции - обработка бромом в щелочной среде (при этом также образуется соль уксусной кислоты). Пропионовую кислоту можно получить, восстановив ацетон до изопропанола (водородом на Ni), потом дегидратируем до пропена (конц. H2SO4 при нагревании), вводим его в реакцию с B2H6 с последующей обработкой H2O2 в щелочной среде - образуется 1-пропанол (гидроборирование-окисление). 1-Пропанол окисляем хромовой смесью до пропионовой кислоты
-
Сульфироваться до 1,3,5-бензолтрисульфокислоты не должно, т.к. введение третьей сульфо-группы протекает значительно медленне, чем второй, т.е. легко поймать момент, когда получится именно 1,3-бензолсульфокислота, а 1,3,5-бензолтрисульфокислоты еще не будет (если взяли большой избыток H2SO4 для сульфирования)
-
Нужно использовать оснОвные свойства о-толуидина и обработать смесь водным раствором сильной кислоты (например, HCl) - о-толуидин образует водорастворимую соль, тогда как о-нитротолуол останется в органической фазе. Отделить его от водной фазы, а саму водную фазу обработать щелочью - образуется о-толуидин, который отделить от водной фазы.
-
Можно обработать каждое из соединений азотистой кислотой (NaNO2 + HCl): в случае аминопропина будет протекать дезаминирование с выделением пузырьков газа (N2), в случае пропионитрила никаких визуальных изменений не будет (не реагирует)
-
Можно получить из 2-бромпропана уксусный альдегид (в несколько стадий), затем изопропилмагнийбромид (реактив Гриньяра) и ввести его в реакция с уксусным альдегидом. Полученный 2-гидрокси-2-метилбутан дегидратировать до 2-метил-2-бутена и ввести его в реакцию с бромом
-
Можно обработать обе соли раствором щелочи - в случае сульфата анилина образуется анилин, который ограниченно растворим в воде (т.е. будут два слоя жидкости: водный раствор неорганики и органический слой анилина), в случае сульфаниловой кислоты образуется растворимая в воде соль (т.е. будет только водный раствор)
-
б) диазотируем, затем замещаем диазо-группу на CN-группу, потом гидролизуем в кислой среде
-
Можно подействовать на окись этилена аммиаком - образуется 2-аминоэтанол. Затем ввести это вещество в конденсацию с фталевым ангидридом - получится N-(2-гидроксиэтил)фталимид, окислить его хромовой смесью до N-(2-карбоксиэтил)фталимида, после этого гидролизовать в щелочной среде (с последующим подкислением) - образуется глицин. Фталевый ангидрид в данном случае нужен для защиты амино-группы перед стадией окисления хромой смесью
-
При обработке азотистой кислотой этого первичного алифатического амина интермедиатом является первичный карбокатион, который претерпевает перегруппировку (1,2-сдвиг CH3- ) во вторичный карбокатион. Этот карбокатион теряет протон, превращаясь в кетон.
-
А - циангидрин бутанона-2, Б - 1-амино-2-метил-2-бутанол
-
-
Соединение будет С6H5-С☰С-CH2OH
-
В первом задании нужно определить, какие электронные эффекты оказывают заместители на бензольное кольцо и вспомнить, что диазотирование - это SE-реакция по аминогруппе. Электронодонорные заместители будут облегчать диазотирование, электроноакцепторные - наоборот, замедлять.
-
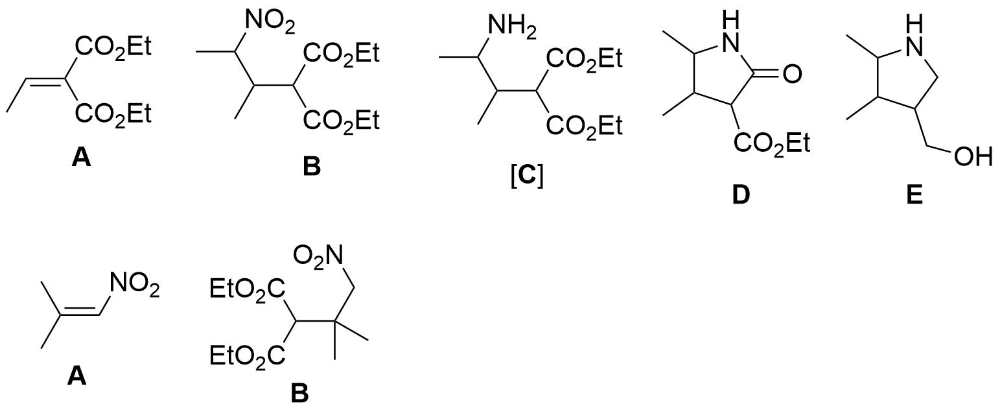
Первая реакция - это азосочетание по положению 3 индола (пиррольный цикл более активен в реакциях электрофильного замещения SE, и подобно другим SE-реакциям индола, оно протекает по положению 3). Вторая реакция - ацилирование алкена, SE-реакция. Образуется (CH3)2C=CH-CO-CH3 + HCl. Образование именно этого продукта, а не изомерного (CH3)2C(=СН)-CO-CH3, объясняется механизмом реакции (электрофил присоединяется по С=С связи с образованием третичного карбокатиона) Третья реакция - реакция Михаэля, сопряженное присоединение амина по тройной связи (1,4-присоединение по атому углерода, связанному с бензольным кольцом). С избытком азиридина дальше может протекать еще одна реакция Михаэля (присоединение по С=С связи) и образование амида.
-
- 1 ответ
-
- 1
-

-
Надо воспользоваться правилом Хюккеля - в плоской замкнутой системе должно быть 4n + 2 (n = 0, 1, 2...) электронов, т.е. 2, 6, 10... электронов, чтобы она была ароматической. В соответствии с этими критериями ароматическим будет соединение е), остальные - нет.
-
1) кротоновая конденсация с образованием 3-(4-хлорбензилиден)пентан-2,4-диона 2) замещение брома на ОН, т.е. получается 1-(2-хлорфенил)этанол 3) замещение брома на (C2H5)2N - образуется смесь изомерных N,N-диэтил-2-метоксианилина и N,N-диэтил-3-метоксианилина (ариновый механизм)

.thumb.jpg.57673d9b078af8ea6b76813bd85797f0.jpg)