Поиск
Показаны результаты для тегов 'задачи'.
Найдено 126 результатов
-
Соединение Х1 состава оптически активно, хорошо растворимо в воде (раствор окрашивает лакмус в красный цвет) и при сильном нагревании переходит в соединение Х2, которое не обладает оптической активностью, умеренно растворимо в воде (раствор имеет кислую реакцию) и намного активнее вступает во взаимодействие с перманганатом калия, чем Х1. При окислении разбавленным раствором хромовой кислоты Х1 превращается в Х3, которое не взаимодействует с перманганатом калия, а при действии йода в растворе щелочи дает желтый осадок. Определите молекулярные и структурные формулы веществ Х1 – Х3, если известно, что Х1 содержит 42.15% углерода и 7.7% водорода по массе. Запишите уравнения всех указанных реакций.
-
Объясните, пожалуйста, МАКСИМАЛЬНО подробно, почему n(H)=2n(H2O).
-
Який об'єм 0 ,1 н розчину KMnO4 піде на титруванняа)0,15 г Na2C2O4б) наважки руди, що містить по масі 43% заліза
-
- задача аналитика
- задача
- (и ещё 21 )
-
При прохождении тока последовательно через электролизёры, содержащие цианиды серебра и золота, в первом электролизёре на катоде выделилось 0,1079 г Ag, во втором – 0,0657 г Au. Вычислите: а) эквивалент золота; б) его валентность в соединении, подвергнутом электролизу.
-
- кулонометрия задачи
- кулонометрия
- (и ещё 4 )
-
-
2. Смесь нитрата меди(II) и карбоната натрия массой 51,48 г прокалили, при этом образовалось 13,44 л(н.у.) газа. Твёрдый остаток растворили в 200 г 15%-ногораствора соляной кислоты. Вычислите массовую долю хлороводорода в полученном растворе. 4. 18,4 г смеси оксида меди(II) и оксида меди(I) полностью растворены в 147 г 10%-ного раствора серной кислоты. Определите состав смеси оксидов в исходной смеси. 5. Смесь хлорида и иодида натрия общей массой 5,01 г растворили в воде и к полученному раствору добавили 200 г 8,5 %-го раствора нитрата серебра. После отделения осадка в фильтрат поместили медную пластинку, при этом 0,96 г меди растворилось. Определите состав исходной смеси солей (в % помассе).
-
Здравствуйте! При решении задачи столкнулась с неточностью в ответе. В решении, указанном составителями сборника, в ответе не учитывается концентрация HNO3, хотя при расчёте массы раствора массу азотной кислоты не вычли. То есть в растворе она есть, но её массовую долю не находят. Можете ли объяснить, почему? Или же это просто неточность или опечатка? Заранее благодарю за помощь. Прикрепляю условия задачи и решение:
- 1 ответ
-
- егэ
- егэ по химии
- (и ещё 7 )
-
Доброго времени суток, господа форумчане! Может кто поможет мне с задачками по аналитической химии, а? Хоть что нибудь, а то категорически не успеваю(((( 1. На титрование 25,00 см3 раствора KCl c TКCl/Ag = 0.01000 г/см3 расходуется 23,20 см3 раствора нитрата серебра неизвестной концентрации. Какова молярная концентрация нитрата серебра? 2. Вычислить потери РbSО4 (в г и %) за счёт растворимости осадка, полученного при добавлении к 20 см3 раствора Рb(NО3)2 молярной концентрацией 0,1 моль/дм3 и полуторного избытка раствора серной кислоты молярной концентрацией 0,1 моль/дм3. 3. Рассчитайте массовую долю Н2SО4 в. навеске 1,0215 г, если на титрование ее идет 20.00 см3 NаОН, молярная концентрация эквивалента которого 0, 1013 моль/дм3. 4. Навеска иодида калия массой 4,3080 г растворена в мерной колбе на 200см3 на титрование 20.00 см3 этого раствора, после обработки окисли¬телем расходуется 23,16 см3 раствора тиосульфата (Т(Na2S2O3/К2Сг2О7 = 0,005348 г/см3). Рассчитать массовую долю КI в образце.
-
- аналитическая химия
- задачи
-
(и ещё 1 )
C тегом:
-
Бензол и хлорбензол неограниченно растворимы друг в друге, их смесь подчиняется законам идеальных растворов. Построить диаграммы Рбензол, Рхлорбензол, Робщ=f(состав), tкип=f(состав) последующим данным: t кип 132 120 100 80,4 Рхлорб 1013 724,4 390,24 - Рбенз - 2983,4 1787,7 1013 рассчитать парциальные давления и общее давление пара при 100 градусах и молярной доле бензола, равной 0,8. Каков состав смеси, закипающей при 110 градусах под атмосферным давлением. чему равна при этом молярная доля бензола в парах? Помогите пожалуйста, разобраться какие нужно диаграммы рисовать а то диаграммы кипения вроде рисуются при постоянном давлении и наоборот - не могу понять как их в зависимости объединить.
-
Добрый вечер. Вот моя задача: К навеске химически чистого карбоната кальция массой 0,1011 г добавили 25 мл раствора серной кислоты. На титрование избытка кислоты затрачено 9,25 мл гидроксида натрия. Найдите концентрации растворов серной кислоты и гидроксида натрия, если соотношение эквивалентных объёмов V(NaOH):V(H2SO4) = 0,995. Решаю: (1) CaCO3 + H2SO4(избыток) —> CaSO4↓ + CO2↑ + H2O (2) H2SO4(остаток) + 2NaOH —> Na2SO4 + 2H2O Количество серной кислоты, которое прореагировало с карбонатом кальция, известно — оно будет равно количеству самого карбоната кальция. Чтобы найти её концентрацию, помимо количества нужно знать и объём. Очевидно, что объём раствора серной кислоты, вступившей в реакцию (1), будет равен всему объёму серной кислоты (25 мл) за вычетом объёма раствора, пошедшего на взаимодействие со щелочью в реакции (2). Последний в условии не дан. Дано некое соотношение эквивалентных объёмов. Собственно, вся загвоздка в том, что мне не вполне понятно, что такое "эквивалентные объёмы", как с ними распоряжаться. Надеюсь, вы мне поможете разобраться)
-
- 1 ответ
-
- задачи по биохимии.
- биохимия
-
(и ещё 2 )
C тегом:
-
Помогите решить первую и по возможности 3ю задачу
-
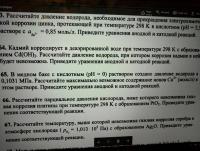
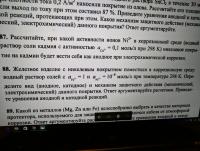
Прошу помочь решить 4 задачи по химии на тему "Коррозия". Надо решить номера: 64,88,65,85. Фотографии заданий в приложенных файлах. Буду КРАЙНЕ признателен вам)))
-
- коррозия химия
- химия
-
(и ещё 2 )
C тегом:
-
ПОМОГИТЕ ПОЖАЛУЙСТА! Я НЕ ХИМИК, НО ДЛЯ ЗАЧЕТА НАДО(
nonstopnonstop опубликовал тема в Решение заданий
ПОМОГИТЕ ПОЖАЛУЙСТА, ВООБЩЕ ХИМИЮ НЕ ПОНИМАЮ, НО ДЛЯ ЗАЧЕТА НЕОБХОДИМО РЕШИТЬ ЭТИ ЗАДАЧИ((( 1. В продуктах реакции хлора с йодистым водородом обнаружено 35,5 г хлора, а теплота процесса составила 15,86 ккал. Какое количество йодистого водорода вступило в реакцию? 2. Возможно ли горение кальция в атмосфере оксида углерода по реакции Са(к) + СО(г) = СаО(к) + С(к) ?-
- неорганика
- химия
-
(и ещё 3 )
C тегом:
-
Как приготовить 20 % раствор NaCl в объеме 300 мл? 0,1 нормальный раствор H3PO4 в объеме 200 мл? 0,15 М раствор HCl в объеме 150 мл? Как решать эти и подобные им задачи? Пожалуйста, помогите мне. Заранее спасибо.
- 1 ответ
-
- растворы
- аналитическая химия
- (и ещё 3 )
-
1)В радиатор автомобиля залили смесь, состоящую из 9 л воды и 0,16 кг метилового спирта CH3OH. При какой температуре будет замерзать раствор? 2)какие процессы пойдут на электродах гальванического элемента, работающего при коррозии сплава железа при нарушении цинкового покрытия? 3)Рассчитать ЭДС гальванического элемента составленного из железного и медного электродов с концентрацией ионов [Fe^2+]=0,01 моль/л, [Cu^2+]=0,001 моль/л. 4)в ПРОМЫШЛЕННОСТИ МЕДЬ ПОЛУЧАЮТ ПО РЕАКЦИИ Cu2O(кр) +Cu2S(кр) =4Cu(кр) +1/2SO2(г). Рассчитать дельта H реакции. 5)Рассчитайте ΔG фазовых переходов: SO3(г) ->SO3(ж) SO3(ж) -> SO3(кр) Какой процесс самопроизволен? 6)В промышленности медь получают по реакции: Cu2O(кр) + Cu2S(кр) = 4Cu(кр) + 1/2SO2(г) SO2(г) Рассчитайте ΔH реакции. 7)к 150г 10% раствора сахара прилили 100г 5% раствора. определить массовую долю растворенного вещества в полученном растворе. 8) Рассчитать потенциал кобальтового электрода в 2М растворе соли CoCl2 9) Составить электронную формулу железа. Определить валентность и степень окисления. На основании валентности бериллия написать формулы оксидов и указать их кислотно-основные свойства.
-
Здравствуйте! Прошу вашей помощи. Я в химии полный ноль (как уже ясно по моему нику ). Не могу решить эту работу. Единственная проблема в учебе - с химией. Вариант 13. 1) Сколько атомов кислорода содержится в газообразном веществе при следующих условиях: газ – NО2, объем 20 мл, температура 25оС, давление 790 мм рт. ст. 2) Как изменится скорость обратной реакции в равновесной системе: 4NH3(г)+5O2(г) D 4NО2(г) + H2O(г) при увеличении объема в 2 раза? 3) 10 см3 2н раствора HCl довели дистиллированной водой до 50см3. Молярная концентрация эквивалента приготовленного раствора стала равной ? (моль/дм3). 4) Смешали 200 см3 10%-ного (ρ=1,11 г/см3) и 100 см3 40%-ного (ρ=1,43 г/см3) растворов NaOH. Какова масса вещества в приготовленном растворе? 5) Что образуется при гидролизе соли MgCl2? Благодарю вас за помощь!
-
Вопрос к химикам:существуют ли какие-нибудь довольно малоизвестные,но эффективные приемы решения задач по растворам.Ну,вот существует так называемый конверт Пирсона (правило креста). Есть ли что-то подобное еще?
-
1) Рассчитать тепловой эффект реакции нейтрализации данной слабой кислоты сильными основанием СH3COOH(p) 2)Сопоставьте основные свойства оксидов MgО и BaO сравнив их стандартное химическое сродство в кислоте по реакции: MeO(кр)+2H(р)=Me(2+)(р)+H2O(ж)3) Определить как изменится скорость прямой реакции(при условии, что порядок реакции равен ее молекулярности), если увеличить объем реакционного сосуда в 2 раза ля процесса: N2(г)+3H2(г)---2NH3(г) 4) На сколько градусов следует повысить температуру системы, что бы скорость протекающей в ней реакции возросла в n раз если температурный коэффициент скорости y=3? : n=45,8 5) Энергия активации реакции Eа=120кДж/моль. Как изменится скорость реакции при повышении температуры от 298К до 328К? 6)Для реакции CO2(г)+H2(г)=CO( г)+H2O(г), протекающей в закрытом сосуде, константа равновесия Kc=1 Начальные концентрации исходных веществ (CO2 и H2) составили соответственно 0,2 и 0,8 моль/л. определите, при какиъ концентрациях всех веществ установится равновесие
-
Оксид неметалла в низшей степени окисления содержит 36,36% кислорода по массе,а в высшей степени окисления -74,07% кислорода по массе.Установите формулы этих оксидов.
-
Как решить задачи по химии (начиная с расчёта pH раствора)?
Хардкор опубликовал тема в Решение заданий
Помогите решить 5 нижних задач, после остальных уже качан не варит Начиная с "чему равен Ph раствора.." и до самого низа -
Добрый вечер, дорогие химики! Помогите, пожалуйста, решить эти задачи на полимеры. Очень срочно надо( Механические свойства полимеров: 1. Нарисовать термомеханические кривые для слабо сшитого полибутадиена и статистического сополимера этилена с пропиленом (состава 1:1). Указать и назвать точки температурных переходов. 2. В одних координатах нарисовать термомеханические кривые для кристаллического полипропилена (ПП) и аморфизованного образца того же ПП. Указать и назвать точки температурных переходов. 3. В одних координатах НАПРЯЖЕНИЕ-ДЕФОРМАЦИЯ нарисовать кривые для кристаллического полиэтилена (Тплавл = 137 град. Ц.) при температурах 25, 50 и 75 град. Ц. Ответ пояснить. 4. В чем существенные различия и сходства деформации полимера в стеклообразном и высокоэластическом состояниях? 5. Полиэтилентерефталат (ПЭТФ) имеет Тстекл 80 град. Ц. и Тплавл 260 град. Ц. В какой области температур надо проводить кристаллизацию ПЭТФ, чтобы получить образец с наибольшей степенью кристалличности? Реакции полимеров: 6. Какие из инициаторов - серная кислота, перекись бензоила, бутиллитий, раствор хлористого железа в перекиси водорода, амид натрия, перекись водорода, металлический натрий, четыреххлористое олово - могут вызывать радикальную полимеризацию стирола? Напишите реакцию инициирования с одним из подходящих инициаторов. 7. Напишите уравнение для степени полимеризации полимера из кинетических данных для радикальной полимеризации. Как можно снизить молекулярную массу полимера, получаемого на начальной стадии радикальной полимеризации, не снижая скорости реакции? Приведите примеры. 8. Как изменится скорость радикальной полимеризации метилметакрилата до неглубоких степеней превращения при увеличении исходных концентраций мономера в 3 раза, а инициатора в 9 раз? Напишите уравнение для скорости полимеризации. 9. какой продукт образуется и как изменяются свойства при пиролизе полиакрилонитрила? Напишите уравнения реакций и поясните ответ.