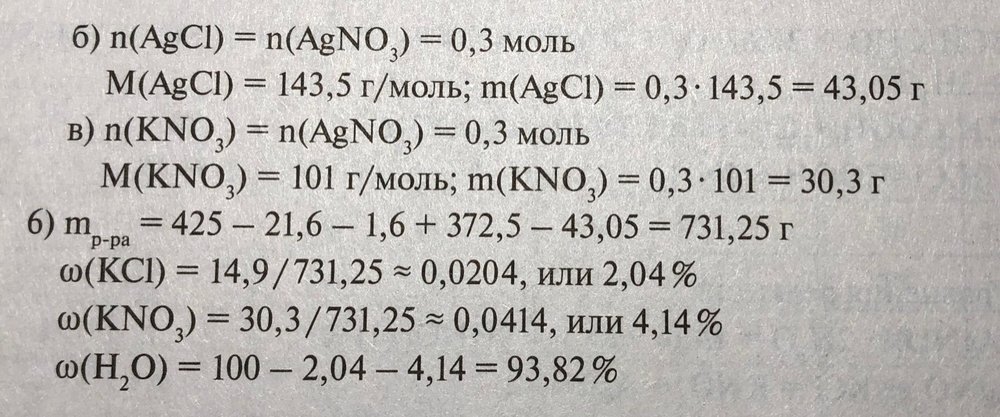Поиск
Показаны результаты для тегов 'концентрация'.
Найдено 81 результат
-
Який об'єм 0 ,1 н розчину KMnO4 піде на титруванняа)0,15 г Na2C2O4б) наважки руди, що містить по масі 43% заліза
-
- задача аналитика
- задача
- (и ещё 21 )
-
Чему равна концентрация простого(твёрдого) Bi⁰? 1 моль/л или 0? И почему?
- 2 ответа
-
- bi
- концентрация
-
(и ещё 1 )
C тегом:
-
Подскажите пожалуйста, как из 3% перекиси водорода приготовить раствор с концентрацией 100мкМ.
- 10 ответов
-
- неорган
- концентрация
-
(и ещё 1 )
C тегом:
-
Здравствуйте! При решении задачи столкнулась с неточностью в ответе. В решении, указанном составителями сборника, в ответе не учитывается концентрация HNO3, хотя при расчёте массы раствора массу азотной кислоты не вычли. То есть в растворе она есть, но её массовую долю не находят. Можете ли объяснить, почему? Или же это просто неточность или опечатка? Заранее благодарю за помощь. Прикрепляю условия задачи и решение:
- 1 ответ
-
- егэ
- егэ по химии
- (и ещё 7 )
-
Какие бывают методы? Применение?
-
Концентрация азотной кислоты для нитрования бензола.
Dmitriy1990 опубликовал тема в Органическая химия
Всем доброго времени суток. Возник такой вопрос: какая минимальная концентрация должна быть у азотной кислоты, чтобы в смеси с концентрированной серной кислотой пронитровать бензол до нитробензола? В каком избытке от теории ее необходимо брать, чтобы получить более или менее достойный выход? Буду рад любому дельному совету.- 6 ответов
-
- бензол
- нитробензол
-
(и ещё 3 )
C тегом:
-
Какими способами в домашних условиях можно повысить концентрацию этилового спирта из 70% в ну хотя-бы 95% раствор ?
-
Даны три вещества одинакового объёма и одинаковой концентрации. Если их смешать, то какова будет их концентрация. Например, даны три вещества с концентрацией 0,4 мг/см^3. Если взять по одному мл. каждого и смешать, то какая будет их концентрация в смеси?
-
Здравствуйте. Вопрос уровня школьной химии за 7 класс, но давно это было. Сам не химик по образованию. Требуется приготовить раствор для травления меди согласно описанию. Цитирую: 85г/л хлорида меди (II), 125г/л хлорида аммония, 25г/л карбоната аммония, 450 мл/л 25% раствора аммиака. Получить требуется активное соединение Cu(NH3)4Сl2. В каких именно пропорциях необходимо готовить реактивы? Без лишних колебаний взял бы каждый реактив отдельно растворил в 1 литре дист. воды и затем смешал бы. Но вот товарищ сбил с толку, говорит, что к единому объему отнесены пропорции. Теперь вот и не знаю... Концентрация ведь в 4 раза может отличаться в крайних случаях.
-
нашли два поточных влагомера (в нефти). один импортного производства (США OW-302), другой - наш (Модкон). И вроде оба хороши, однако мнения разошлись: кто-то поддержал зарубежный влагомер, однако я больше склоняюсь к отечественному аналогу. Что Вы думаете по этому поводу? Действительно ли влагомер местного производства ни чем не хуже зарубежного, или все же...?
-
Здравствуйте. Подскажите, где можно взять кривую зависимости электропроводности соляной кислоты от ее концентрации?
- 2 ответа
-
- кондуктометрия
- концентрация
-
(и ещё 1 )
C тегом:
-
Есть комплексное соединение K4[Fe(CN6)] в растворе, концентрация Cисх = 0.1 моль/л, константа нестойкости = 10-37. Этот раствор содержит избыток лиганд(ов) в виде в-ва KCN с молярной концентрацией Cизб = 1 моль/л. Нужно найти концентрацию комплексообразователя и лиганда. Решал так: [Fe(CN6)] = Fe + 6CN x = концентрация комплексообразователя (Fe) По формуле Kнестойкости= x * ( Cизб + 6x )^6 ) / (Cисх - x) нашёл x. Вопрос: концентрация лиганда будет равна Cизб, Сизб + 6x или 6x?
-
Как найти исходную концентрацию вещества А в реакции A+B=C+D?
Karina_b опубликовал тема в Решение заданий
Химическое равновесие реакции A+B=C+D (газы) установилось при следующих концентрациях : [A]=6 моль/л, [В]=2моль/л, [С]=4 моль/л, [D]=3 моль/л. Рассчитайте константу равновесия и исходную концентрацию вещества А. Константу то рассчитали, а вот как найти исходную концентрацию? -
Вычислите массовую долю раствора Na2SO4, полученного при растворении 10 г (кристаллогидрата) Na2SO4х10H2O в 150 г 5%-ного раствора Na2SO4.
- 1 ответ
-
- кристаллогидрат
- концентрация
-
(и ещё 2 )
C тегом:
-
Определите константу и степень гидролиза соли в растворе и константу диссоциации амоний гидроксида, если pH 0,1М раствора амоний хлорида равно 5,1. Помогите решить, пожалуйста.
-
- концентрация
- ph
-
(и ещё 1 )
C тегом:
-
Рассчитайте pH раствора HCl, молярная концентрация эквивалентов которого Cэ=0,005моль/л. Как изменится pH этого раствора при добавлении в него 0,08моль/л KClO4. Что делать? ПОМОГИТЕ Правильно ли я понимаю, что нужно через ионную силу найти gH+. После чего по формуле pH=-logah+ найти кислотность. А как быть с KClO4?
-
Который день ломаю голову над этим заданием. Нужно рассчитать изменение скорости прямой реакции при одновременном изменении условий реакции. Даны уравнение реакции (2А + 2В ---> C + 2D) и изменение условий ( Концентрация вещества A равна половине начальной концентрации С(А)=0.5*С0(А), концентрация вещества В равна трем начальным концентрациям С(В)=3*С0(В); изменение температуры равно 20 градусов, температурный коэффициент равен 1.5; вещества являются газами. Желательно хоть и не с подробными, но объяснениями. Заранее спасибо за помощь.
- 1 ответ
-
- кинетика
- скорость реакции
- (и ещё 6 )
-
Не получается найти концентрации. Подскажите пожалуйста, как это сделать? После того как в реакционном сосуде смешали 125 мл 2 М раствора HClO4, 135 мл 0,1 М раствора KMnO4и 270 мл 0,35 М раствораFeSO4 произошла реакция. Напишите уравнение этой реакции и определите концентрацию ионов Fe3+и Мn2+в полученном растворе. Может выразить Mn2+ и Fe3+ через исх. конц. вещ-в? В общем, не получается(..
-
Здравствуйте! Помогите с решением. При 508°С константа скорости рекции H2(г)+I2(г)=2HI(г) равна 0,16 л/(моль*м). Исходные концентрации H2 и I2, соответственно равны 0,04 моль/л и 0,05моль/л. Вычислить начальную скорость и скорость в тот момент, когда концентрация стала равной 0,03моль/л. Заранее спасибо.
- 1 ответ
-
- скорость реакции
- константа скорости
- (и ещё 2 )
-
Для уравнения реакции 2А + 2В = С + 2D нужно найти равновесные концентрации , [C], и [D], а так же концентрацию прореагировавшего вещества А. Даны исходные концентрации веществ А и В, равные С0(А)=С0(В)=1 моль/л и равновесная концентрация [A]=0.4.
- 1 ответ
-
- химическое равновесие
- концентрация
- (и ещё 2 )
-
Помогите с решением задачи. Ответ я знаю надо просто объяснить принцип решения. Заранее спасибо. #1 Сколько г 10-водного сульфата натрия и воды потребуется для приготовления 1 кг 5%-го раствора, рассчитаного на безводную соль? #2 Какой объем 92%-го раствора серной кислоты плотностью 1,83 г/мл нужно взять для приготовления 3л 0,5 Н раствора
-
К 1 литру 0,1 М раствора слабой кислоты НА (Ка=10-5) добавили некоторое количество твердого КОН, при этом рН раствора стал =4. Определите концентрации [К+], [НА] и [А-] в полученном растворе. Подскажите, пожалуйста, схему решения этой задачи. Особенно вгоняет в ступор тот факт, что не дана [КОН].
- 3 ответа
-
- физическая химия
- растворы
-
(и ещё 3 )
C тегом:
-
- 1 ответ
-
- неорганическая химия
- растворы
-
(и ещё 1 )
C тегом:
-
- 1 ответ
-
- растворы
- концентрация
-
(и ещё 1 )
C тегом: