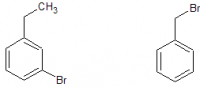-
Постов
33677 -
Зарегистрирован
-
Победитель дней
1115
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
Смотря на что. Обычно осаждают химически на носитель с развитой поверхностью - типа силикагеля или асбеста. Впрочем, к катализаторам дожигания требования могут быть и другими - в плане механической/химической стойкости. Тут уже инженерное материаловедение рулит.
-
ЛАГ, боргидрид и еже с ними. Каталитически он тоже гидрируется, тем же никелем Ренея. Просто никто в растворе этого не делает, ввиду полнейшей бессмысленности процесса.
-
Никакого отношения к муравьиной кислоте эта шняга не имеет. Это производное угольной кислоты - гидразид. И никакого восстановления тут нет. При гидролизе снова получится CO2 и гидразин: NH2-NH-COOH + HCl = CO2 + N2H4*HCl NH2-NH-COOH + 2NaOH = Na2CO3 + N2H4 Реакция полностью аналогична взаимодействию СО2 с аммиаком: CO2 + NH3 = NH2-COOH (карбаминовая кислота - амид угольной кислоты) и с водой: CO2 + H2O = HO-COOH (угольная кислота) И разлагается она так же, как карбаминовая: 2NH2-NH-COOH ----> NH2-NH-COOH*N2H4 + CO2 2NH2-COOH ----> NH2-COOH*NH3 + CO2 С нитритом будет забавная реакция: NH2-NH-COOH + NaNO2 = NaN3 + CO2 + 2H2O CО2 прекрасно восстанавливается штатными восстановителями карбонильной группы.
-
Да прям! Нормальная колба из чешского набора посуды. "Не более 2-х литров" - это про круглодонки штоле? Я на вакуумной перегонке юзал и 10-ти литровые, и 200-литровые. Главное - чтоб не покоцанная была. Конические Эрленмейера - ну, это само собой. Не дают гарантии? Жлобы патамушта. У какого-нить рукожопа круглодонка херакнется - поди потом, доказывай, шо дело не в колбе. Инструкции по ТБ лучше сразу читать двумя глазами, чем потом - одним. А если хочется поиграть в русскую рулетку с плоскодонками - валяй, мы живём в свободной стране!
-
За такой "аппарат" студентов-первокурсников бьют по голове штативом Где воздушка??? Аллонж должен быть с отводом, иначе перегонка пойдёт под давлением. А не надо смотреть. Есть толстостенные треугольные колбы Бунзена и есть круглодонные колбы. Фсьо! Только эти колбы можно использовать для вакуума. Причём для нагревания под вакуумом - только круглодонные. Как лопается на вакууме круглая пол-литровая плоскодонка я сам наблюдал.
-
Почему "против правила Марковникова"? Совершенно по правилу. Водород присоединяется к наиболее гидрогенизованному атому углерода кратной (тройной) связи.
-
Нет такого. Есть пентен-2 (CH3-CH=CH-CH2-CH3) 1. CH3-CH2-CH2-CH2-CH3 --(Br2, hv)--> CH3-CHBr-CH2-CH2-CH3 + CH3-CH2-CHBr-CH2-CH3 Из обоих изомеров при дегидрогалогенировании получается пентен-2: CH3-CHBr-CH2-CH2-CH3 --(KOH, спирт)--> CH3-CH=CH-CH2-CH3 CH3-CH2-CHBr-CH2-CH3 --(KOH, спирт)--> CH3-CH=CH-CH2-CH3 2. CH3-CHOH-CH2-CH2-CH3 --(H2SO4, -H2O)--> CH3-CH=CH-CH2-CH3 3. Можно затейливое что-нить завернуть: CH3-CH-CO-CH2-CH3 --(PCl5, -POCl3)--> CH3-CH2-CCl2-CH2-CH3 --(2KOH, спирт)--> CH3-C≡C-CH2-CH3 --(H2, Pd/BaSO4)--> CH3-CH=CH-CH2-CH3
-
- 4 ответа
-
- 1
-

-
"Нано-частицы" - это нано-частицы глины. Мокрый размол пигментов столетиями используется в красильном деле. А реакция дегидратации действительно идёт на окиси алюминия, только при высокой температуре.
-
Ничего там не образуется. И реакций никаких нет. Будет смесь глины и спирта.
-
1. Неопентан, вестимо - С(CH3)4. Получается единственный хлорид - CH3-C(CH3)2-CH2-Cl (2,2-диметил-1-хлорпропан). Дихлоридов два будет: Cl-CH2-C(CH3)2-CH2-Cl (2,2-диметил-1,3-дихлорпропан). CH3-C(CH3)2-CHCl2 (2,2-диметил-1,1-дихлорпропан). 2. А = CH3-CHBr-CH3 (2-бромпропан) B = (CH3)2CH-Li (изопропиллитий) C = Li[Cu(CH(CH3)2)2] (литийдиизопропилкупрат) D = CH3-CH(CH3)-CH2-CH3 (2-метилбутан)
-
С качественными реакциями сложнее. Ну, разве что - реакция с водным раствором аммиака: C6H5-CH2-Br + NH3 --(H2O)--> [C6H5-CH2-NH3]+Br- Бензилбромид в нём растворяется с образованием соли - бромида бензиламмония. А м-бромэтилбензол не реагирует, и не растворяется.
-
Ясен пень - химики. С уклоном в химическую физику и гетерогенный катализ. Специализация весьма специфическая (пардон за каламбурчик). К тому же такие исследования требуют нехилого (и дорогого) аппаратурного оформления. Идея, конечно - странная
-
При высушивании парафин потащится к поверхности, и никакого равномерного распределения не получится. Всё равно перемешивать придётся.
-
О! Это же Аделька! Я там, когда в гараже Водоканала работал, так насмотрелся на этот райончик (там, гле ближе к Родине). Только улица Техническая в Кировском могла с ним соперничать в протяжённости водных просторов после дождя.
-
Ну, скажем так (есть варианты): CH3-CH=CH2 --(Br2)--> CH3-CHBr-CH2Br --(2KOH, -2KBr)--> CH3-C≡CH (пропин) CH3-CH=CH2 --(O3, Zn)--> CH3-CHO + HCHO (этаналь + метаналь) CH3-CHO --(H2, кат.)--> CH3-CH2-OH (этанол) --(SOCl2, -SO2, -HCl)--> CH3-CH2-Cl (хлорэтан) CH3-C≡CH + Na --(-H2)--> CH3-C≡C-Na (пропинид натрия) CH3-C≡C-Na + CH3-CH2-Cl --(-NaCl)--> CH3-C≡C-CH2-CH3 (пентин-2) CH3-C≡C-CH2-CH3 + H2O --(HgSO4)--> CH3-CO-CH2-CH2-CH3 + CH3-CH2-CO-CH2-CH3 (пентанон-2 + пентанон-3)
-
Их не сжигают. Пусть вас не обманывает название "жжёные квасцы". Просто квасцы из водного раствора кристаллизуются с большим количеством воды (до 12 моль воды на моль квасцов). "Жжёные квасцы" - это квасцы, обезвоженные нагреванием. При этом только водяной пар выделяется, и абсолютно никакого дыма. Обезвоживать квасцы можно на сковородке, медленно нагревая их, не допуская плавления. Уже при 120С они полностью обезвоживаются.
- 4 ответа
-
- 1
-

-
Да, вполне возможно, что он всё-таки существует (как неуловимый Джо ). Я в своей практике имел дело как-то с солями этилендиамина. Казалось бы - чего проще, двухкислотное основание, средняя соль, основная соль. Ан нет! Этилендиамин с пара-толуолсульфокислотой даёт прекрасно кристаллизующуюся основную соль (и не менее прекрасно кристаллизующуюся среднюю). А вот гидрохлорид основной не получается. Только средний. Смесь среднего гидрохлорида с избытком этилендиамина так и остаётся кашевидной смесью дигидрохлорида с этилендиамином. Загадка...