-
Постов
3834 -
Зарегистрирован
-
Посещение
-
Победитель дней
35
Тип контента
Профили
Форумы
События
Весь контент ash111
-
ГЖХ, конечно же, ну точнее GCMS. Один прогон и все понятно, где что и сколько. Правда если там лютая смесь углеводородов типа изомерных октанов, то вот с соотношением отдельных изомеров может быть проблема У нас например все абсолютированные растворители проверяются именно GCMS, офигенная удобная штука, главное чтоб вещество было летучее
-
Я его от воды перегонкой сушил, правда я тогда не знал что это называется сульфурол.. Он кипит около 60°С на 0,2 mm Hg, так что единственное что может быть - что он летит с паром (у меня то в нем воды было процентов десять, но для мицунобы это было уже критично). Только даже если так, это не проблема, просто собираешь это пар в приемнике, и оттуда экстрагируешь. А вот касторовое масло - для меня странно.. какие там коэффициенты распределения - одному богу известно. Считает для него logP около нуля, сколько раз надо экстрагировать касторовым маслом, а потом из него, короче я бы не рискнул с таким заводиться
-
упарить воду досуха, вытягивать оттуда вашим нерастворимым в воде растворителем. упаренную воду тоже проэкстрагировать можно, там уже не будет никакой черной дыры.
-
с фантазией у вас полный порядок. Сделайте документалку про рождение и развитие жизни на Земле в параллель с постепенным превращением толуола в бензиловый спирт. Довольно необычно будет.
-
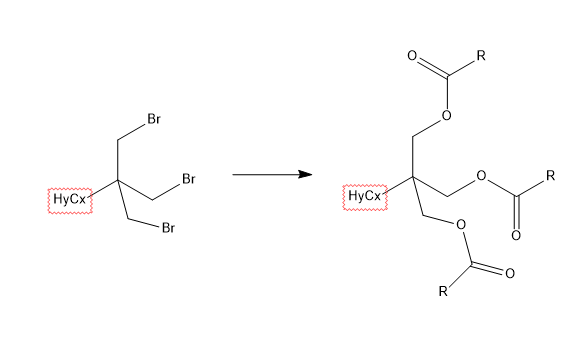
Ну потому что их нет, вообще. Я уже писал про это, ортоэфиры можно еще получить, но уже даже они дико реакционноспособные. У автора приступы безудержной фантазии. Нам на фирму заходили заказы на синтезы ортоэфиров с остатками сложнее метила и этила - кажется 75% из них так и не сделали, потому что сложно всё - заставить реагировать, выделять, чистить. А автор хочет три ацетила. Я уже молчу о том насколько токсичной была бы такая байда.
-
в ограниченной растворимости понизили температуру, часть вещества выпала. прогрейте снова до 40-50 градусов и оно опять растворится
-
нет, водороды нуклеофильно не замещаются, разве что на металлы, но не в вашем случае. без шансов. уже объяснял почему. окей, ацетатом, я оговорился, имея в виду условный конечно же ацетат. Ацетатом не заместите. Даже один галоген, не говоря уже обо всех. Херня, не получится. вот такое чтото - нормально. совершенно верно, нигде.
-
Органической химии в этой книжке - три страницы. Неорганическая - в объеме школы. Аналитической нет. Остается какая? чем вообще этот томище заполнен? не помню уже, но выбора какбы особо нет у вас она есть - зафоткайте оглавление) А, ну да, общая химия это так и называется, как книжка, но она ж по сути физическая.
-
реутов, курц,бутин, мгушное издание. там в основном все есть. Если тебя интересуют элементы вообще все типа там железа и кальция и марганца, то в целом можно сказать следующее: идет хреново, а когда идет хорошо, по получается такая гадость, что лучше бы оно шло плохо) ничего. дибром надо брать. с дибром - зависит от концентрации, что получится..) и так и так можно сделать, подбором условий, но если честно то всегда будет некая смесь. нуклеофил всегда атакует наименее стерически затрудненные позиции при прочих равных) но опять плохой пример, получается смесь нитро-соединения и алкоксинитрита имеется в виду динатрийацетилен, я так понимаю, если вопрос в том, замкнется ли он в цикл или останется линейным ой, слезы из глаз.. а нет, это кровь там описано всего по чайной ложке. абсолютно бесполезная книжка, ну может разве что физхимия там более-менее. Органика/неорганика там на школьном уровне. ужасная книга. терпеть ее не мог.
-
галогены, может быть, а не водороды? речь была про хлор если я все правильно помню какая разница какая стерика если не на что нападать))) какой эфир??) Ацетилом три галогена заместить не получится, просто забудьте об этом. даже три йода. Если замещать спиртами, это называется ортоэфир, метил- и этил-ортоэфиры известны, а все прочие - попробуй получи. И да, это реагент для получения ацеталей из кетонов, например. Берется кетон, ортоэфир чуть больше эквивалента, туда бросается кристаллик TsOH или любой кислоты и реакция происходит по щелчку пальцев. Это к разговору о том, насколько они устойчивые, инертные и вообще безопасные для человека. Это страшная гадость - ортоэфиры. Просто нарисуйте структуру которая вам примерно нужна, тогда можно посмотреть что из этого нормальное и можно сделать.
-
Сильное основание, если на втором от галогена атоме углерода есть водород, то пойдет элиминирование вместо замещения. Алкен будет. Ну и самое херовое что от этого алюминия вы потом не отобьетесь, это будет страшнейшая неразделяющаяся чача, можно ее развалить более-менее насыщенным раствором NH4Cl, но как собирать продукт в ваших условиях, я не очень понимаю. Вообще я советую перед тем как чтото химичить, представить себе в голове весь предстоящий процесс, от смешивания реагентов до получения финальной субстанции. Ознакомиться со всеми физикохимическими свойствами того, с чем предстоит работать. Потому что иначе потом нежданчики будут вылезать один за другим, и весь процесс обратится в мучение без ясных перспектив.
-
обычно эта идея провальная ибо даже с учетом наценок магазина у производителя на порядок ниже входящие цены на сырье.. Ну и потом госты же не просто так созданы, тут уже один деятель вон хотел делать искусственные жиры похожим способом, но, кажется, вовремя одумался. В гостах прописаны технические характеристики продукта, если по-простому то лицензированный продукт по идее (по идее, вы знаете где мы живем) проверен и не содержит опасных примесей, а у вас с подобными идеями эти примеси будут, с большой долей вероятности. Продукты неполного этерифицирования, с остатками галогенов, а это довольно таки гадостная вещь ибо гидрофобная и содержит галогены - прямая заявка в канцерогены. Ладно бы у вас была некая "хорошая" реакция что без анализа вы бы могли с высокой долей вероятности сказать что всё прошло и полученное может тоже гадость, но не настолько уж и злая. Но у вас-то натурально чача какая-то будет, и методами анализа вы очевидно не располагаете, чтобы результат своих действий оценить. Поэтому опасненько это все, а здоровье, как известно, дороже всего, и не только в фигуральном ключе. В общем - я предупредил)
-
это да, это да? бесспорно Пойдет, но от него очень сложно избавляться, если надо выделить продукт. Эмульсии просто чудовищные образуются. С ДМФА проще.. и его можно отогнать на роторе, ДМСО только на масляном насосе и меееедленно удачи) много галогенов вам явно задачу очень усложнят, если честно. у вас экологический чтоли какойто проект, типа взять страшную полихлорированную гадость и из нее сделать чуть меньшую гадость? Ну нееет? наоборот, эфиры серных кислот на галогены нуклеофильно меняют, мезилаты, тозилаты и так далее, чаще всего.
-
да успокойся, посмеялись - забыли. Не зафлуживай тему?
-
комплексных соединений меди туева хуча, и у вас уточняли, комплексообразование меди с чем вас интересует. Нет никакой общей характеристики, ну разве что то, что это комплексы d-металла. Координационное число может быть разным, степень окисления может быть разной, лиганды могут быть сильные и слабые, здесь необходимо уточнение, одно перечисление вышеописанного займет два урока? А вы на вопрос о лигандах уткнулись в свою медь. Это тупняк, да ? ниче, бывает
-
хлор просто очень слабополяризуемый. поэтому его заместить относительно сложно, только если он неким образом не активирован, как например в бензилхлориде или аллихлориде.. вот бром или йод - совсем другое дело. Но два галогена при одном атоме углерода это все равно плохо, какой бы галоген там ни был, вон дийодметан алкилирует пирокатехин только при долгом нагревании, а йодметан при комнатной и с разогревом. Понятно, не последнюю роль играет и стерика. Истерика это всегда плохо) явно не в этом Никак. Там вообще почти нуклеофильное замещение не идет, в промышленности этот хлор замещают при температурах выше 200 градусов и под давлением, причем это на хорошие нуклеофилы он так замещается типа первичных аминов и спиртов. И это уже SnAr, не обычное Sn1/2 Диметилацетамид можно взять, бутанол, да много вариантов.. Не скажи) нормальная тема, много раз спасала) выходы близки к количественным в случае метилйодида, бензилхлорида/бензилбромида, с первичными йодидами/бромидами можно рассчитывать на в целом хороший выход, ну, с вторичными конечно уже хуже, хотя все равно похоже по выходам с Мицунобой. Берется кислота в DMF, кидается туда поташ 1,2-1,5 эквивалента и добавляется галогенид 1,5 эквивалента, мешается ночь. Можно погреть если надо, обычно несильно) Если кислота довольно сильная как в примере ниже, можно взять гидрокарбонат натрия. Один раз надо было 2-бром-4-хлор-3-никотиновую кислоту этерифицировать, так вот только таким методом и получилось)
-
Все правильно ответил, а вот автор тупит)
-
есть, да не так чтобы вуаля, но можно нужно чтото такое, в чем и то и другое растворяется. Спирт (метанол, этанол, изопропанол), спирт/вода, ДМФА, ДМСО, чтото полярное и необязательно апротонное. А вот это плохо, даже дихлорэтан уже плохой алкилятор. Для него придется это все дело кипятить, долго и нудно более высококипящие - это плюс (можно выше греть), твердые - пофиг (главное чтобы растворялись, а растворяется хлорорганика в органике обычно хорошо, очень кстати жировую ткань любит, это так, к слову), и да, гексахлорэтан - без шансов. Сущность алкилирования состоит в том что молекула алкилятора неким образом полярная или поляризуемая хотя бы, а гексахлорэтан и неполярный, и оччень плохо поляризуемый, и все эти хлоры это чудовищная стерика. Поэтому о таком можно даже не думать.
-
Самый стабильный радикал там должен быть на изопропильном углероде, мало того что третичный, еще и бензильный. Но в целом да, такие штуки синтезируют в помощью всяких одноэлектронных окислений, типа трехвалентного железа и БИДы Тайна раскрыта)) как пить дать там образуется трехвалентный йод и окисляет это все до дифенила
-
новый, безазотный рецепт
- 21 ответ
-
- 1
-

-
Посмертно?? оо, новые идеи получения гремучей ртути, панятна
-

.thumb.jpeg.252a9b1bb4bb2764898b676b40684489.jpeg)