-
Постов
34222 -
Зарегистрирован
-
Победитель дней
1128
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
Не, не-не-не! Ерунда это всё, шо я тут наплёл. Память подводит. Что фенантролин алкилировал - это точно, там два длинных алкильных хвоста надо было посадить (какой-то жидкий кристалл получался, тогда это модно было, как сейчас - наноджигурда всякая). Вот в процессе что-то там йодом окислял, а потом от того йода долго-долго отмывал продукт (да так и не отмыл до конца). С литием какой-то литийалкил получал - эти шленки и аргон помню. Тут помню, тут не помню - развели тут ромашку . Что-то мне подсказывает, шо там шло присоединение алкиллития по кратной связи у азота, а йод нужен был для окисления/ароматизации продукта присоединения. Так что, с фениллитием может прокатить афёра. Но - хрен его знает, зря я тут вылез со своим "опытом"
- 13 ответов
-
- фенантролин
- арилирование
-
(и ещё 1 )
C тегом:
-
Сульфат свинца из сильнокислого раствора полностью не выпадет, а в присутствии нитрата свинца основной нитрат висмута не выпадет. Лучше не серную кислоту добавлять, а раствор сульфата натрия. А уж из оставшегося кислого раствора нитрата висмута и нитрата натрия вытащить висмут. При нейтрализации будет выпадать основной нитрат висмута. Его потом придётся кипятить со щёлочью, шобы в оксид перевести, или прокалить до полного разложения.
-
Было дело - альфа-алкилфенантролин получал металлированием фенантролина бутиллитием с последующим алкилированием йодалканом. Но в вашем цейтноте это вряд ли ценная информация.
- 13 ответов
-
- фенантролин
- арилирование
-
(и ещё 1 )
C тегом:
-
Исходная смесь: 30*a + (1-a)*2 = 4.5*2 a = 0.25 Состав исходной смеси: CH2O + 3H2 Пусть это будет гидрирование: CH2O + 3H2 ----> CH3OH + 2H2 плотность по водороду конечной смеси (32 + 4)/3/2 = 6 Фигня получается. Плотность возрастает. Пойдём другим путём, дегидрирование: CH2O + 3H2 ----> CO + 4H2 плотность конечной смеси: (28 + 8)/5/2 = 3.6 Опять фигня получается, даже при 100%-м выходе плотность 3 не достигается. Что-то надо в консерватории поправить
-
Нет такой кислоты (H2ZnO2). Цинкаты состава Me2ZnO2 существуют только в твёрдом виде (и получаются только "сухим" способом). В воде гидроксид цинка малорастворим, и в растворе существует в виде гидратированного комплекса [Zn(H2O)4](OH)2, который диссоциирован в очень малой степени как основание [Zn(H2O)4](OH)2 [Zn(H2O)4](OH)+ + OH- И в столь же малой степени - как кислота: [Zn(H2O)4](OH)2 H2[Zn(OH)4] H[Zn(OH)4]- + H+
-
Ну, тогда не знаю - шо там за наноджигурду намешали. Остаётся только химчистка. У вас там есть итальянские химчистки?
-
Дым-жидкость сам бодяжил, было дело. Отстирывается водой элементарно, там всё водорастворимое.
-
Да ни хрена не рванёт! Сам получал так бромистый алюминий. Фольга в колбе и бром туда подливаешь из капельницы. Греется хорошо, местами вспыхивает. Главное - никакого индукционного периода, из-за которого вся беда бывает. Горит он себе в броме - и пусть горит. Пламя не жаркое, колба не треснет.
-
Ну що вы прицепились к этому "нии"? Контору можно как угодно назвать. Активно работающая фирма часто плодит вокруг себя целый выводок фирмочек, которыми фактически руководят одни и те же боссы, а на должности назначают из своих, кого ни попадя. Я как-то тоже был директором НИИ с важным названием, но не долго - у меня подпись некрасивая, не внушает, закорючка этакая А раз на стороне ищут - стало быть нужен не аватар для босса, а просто толковый исполнитель для задач несколько выше уровня офис-менеджера (70 тыр - как раз такая зарплата).
-
Разумеется! Я - свободный художник и холодный сапожник, пардон - философ
-
Как я понял, ТС интересовало - можно ли объяснить явление чорного дыма от спички естественно-научными причинами. Уважаемые эксперты дали заключение: в области действительного такое явление невозможно. Ergo - ТС должен внимательно следить за дымом от спичек, и если он стал чорным - амба! Прокляте сработало! Надо будет искать ту цыганку, шобы снять порчу. Ну, а пока чорного дыма нет - помнить всё время про ту цыганку и её проклятие. Кстати - надо будет на сон грядущий Кинга перечитать, "Худеющий"
-
40%-я плавиковая кислота с серной будет смешиваться практически без нагревания. Всю теплоту сольватации уже "съел" HF. Безводный HF называют "лучшим растворителем белков". Но будет ли таковым смесь плавиковой и серной кислоты - хз.
-
Да! Проалкилировать опять же можно - до соли N-алкилпиридиния. Можно по Чичибабину проаминировать амидом натрия. У пиридина богатая химия, масса возможностей!
- 22 ответа
-
- тухлятина
- трупный запах
-
(и ещё 1 )
C тегом:
-
Есть такие слонобои, не спорю. Но у этого-то робингуда - какое-то "феврале без внушителя"
-
Можно. Я подберу литературку. Но - попозже. Что-то меня совсем грипп сломал. Ничего не соображаю.
-
Да ни фига! Лёгкость окисления с образованием пероксидов возрастает в ряду диметиловый эфир
-
Шо там в учебниках описано - это на совести авторов. Никаких доказательств наличия атомарного водорода in situ там нигде не приводится. Сварка атомарным водородом - это абсолютно не имеет отношения к вопросу. В таких аппаратах атомарный водород получают в электрической дуге, при высокой температуре. А ваш "знающий человек" - ошибается, мягко говоря. Водород в виде протона в водном растворе HCl покрыт весьма толстой шубой гидратной оболочки, гораздо более толстой, чем катион какого-нить свинца. Так с какого хера он будет "переносчиком", и на хрен нужен такой переносчик? Миф о водороде in situ из цинка и солянки - это действительно миф, это доказано, причём давно уже. Не ведитесь на эти сказки.
-
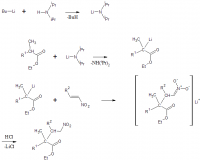
3-хлор-2-метоксифенил - это для меня просто радикал. Он может быть, может не быть. Суть в том, что диизопропиламид лития - сильное основание, с заторможенной нуклеофильностью. Роль его здесь может сводиться только к катализу конденсации сложного эфира с нитроолефином. Охлаждение до -50С предотвращает сложноэфирную самоконденсацию. Если хотите, то в общем виде это так будет: Такое моё ИМХО
-
Ну, тут всё от смеси зависит. Даже дельта температур кипения не очень-то - показатель. При равной дельте могут легко делиться, а могут в куче гнаться - хоть на термометр не смотри.
-
Данунах - шо тут близкого! Эмульсии чем только не разрушаются! Даже скрипом подшипника в реакторной мешалке. Ну ещё одно воздействие - СВЧ. А можно ультразвуком, можно деэмульгаторами, даже в радиодипазоне облучение помогает. Да у опытного аппаратчика эмульсия делится от заклинания, в нужное время и нужным образом произнесённого! Хотя, есть эмульсии, которые хоть на пупе вертись - хрен разрушишь, у меня были такие.
-
Если разгоняется смесь - однозначно есть. Другое дело, шо тут пределы выкипания фракций будут широкими, тонко её не разделишь Но если температуры кипения основного вещества и ботвы хотя бы на 30-40 градусов различаются, то лучше отследить.
-
Знаю, знаю! На Малой Арнаутской разливают. Греки его из Румынии в бензобаках шаланд возят