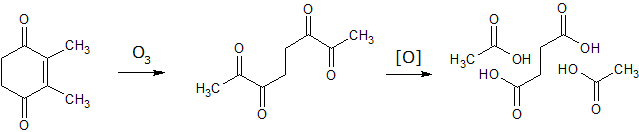-
Постов
34633 -
Зарегистрирован
-
Победитель дней
1149
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
Ну, не скажи, говорят у вьетнамок πзда поперёчная. Я не проверял, но информация заслуживает внимания.
-
Жениться бы тебе, барин, а не такой фигнёй заниматься...
-
Бро, если у тебя той платины - хоть жопой ешь, что можно такие експерименты ставить, наплюй! Есть более интересные варианты с контингентом балийских шалав. У тебя же хватит на билет до Бали?
-
Ну, так - почините! Странные разговоры - хочу посрать, но у меня палец в жопе - что делать?
-
Можно! Формиатом - халяльно, но если вы в пути, то можно...
-
Газовой горелкой сварочной. Сварщики с баллоном у вас есть в штате?
-
Множества натуральных чисел и чётных чисел - равномощные. Их количество одинаково. Каждому натуральному числу можно сопоставить чётное, и наоборот. Но к квантовой механике это не имеет отношения. А неортодоксальные специалисты пусть идуд в жеппу!
-
Ясень пень - они же постоянно дело имеют с припоями. Если мне принесли шабашку с использованием гептила - мне насрать на токсикологию, но вот если меня подряжают с гептилом работать регулярно - я, пожалуй, сольюсь. Во избежание.
-
Отталкивает электрическое. А магнитное как раз - стягивает. Как слипаются витки катушки.
- 21 ответ
-
- 1
-

-
Значит PCl3 в п/э таре хранить нельзя?
-
Брехня. Если постоянно этим заниматься - можно словить литейную лихорадку в кадмиевом варианте. Но это - если чистый кадмий лить. Я, как-то, в школе ещё, выплавлял свинец из старого аккумулятора. Получил вполне конкретный синдром - красноглазие. Это, когда не сами глаза краснеют, а кожа вокруг глаз раздражена и постоянно чешется. Это тоже - литейная лихорадка, только свинцовая. Но если сплав Вуда готовить, то там температура-то - плёвая, ничего не летит. Вот использовать его, в качестве высокотемпературной бани, надо под тягой.
-
Древние знали это знание, утерянное в веках. Потом оно возродилось в России, но цари-немцы, задушившие Петра Феодоровича - последнего Рюриковича, запродали его патерам аримофейским, езуитам и сионским мудрецам. Если катушку на хую вертеть - то будет электромагнитная индукция. Русичи всегда это знали!
-
Тут возникает законный вопрос - а что происходит между двомя електронами, летящими рядом с релятивистской скоростью? С точки зрения электронов, им надо расходиться, ибо сами они никакого магнитного поля не видят. С точки зрения стороннего наблюдателя, они должны сближаться, ибо для него они создают вполне измеримое магнитное поле.
- 21 ответ
-
- 1
-

-
Возьмём два сверхпроводящих витка, и каждый зарядим лишними электронами, а потом возбудим ток. При совпадении направления тока витки будут притягиваться, при этом ток в обоих будет уменьшаться за счёт совершения работы против внешних сил, удерживающих витки от слипания. В данном случае это будет взаимодействие зарядов. На каком-то расстоянии силы электростатические и магнитные уравновесятся. Такая модель годится?
- 21 ответ
-
- 2
-

-
Тут возникает вопрос - а что заставит заряд вращаться вокруг некоего центра? Заряд противоположного пола? В классической электродинамике эта система неустойчива. В квантовой - это атом. Тут - обширная область диполь-дипольных и поляризационных взаимодействий, но они напрямую не связаны с магнитным полем. Если это сверхпроводящее кольцо, по которому мотыляется электрон, то взаимодействие таких витков будет чисто магнитным, электрического поля там вообще не будет. Можно рассматривать движение заряженных шаров на механической тяге, на тросиках. Это об этом речь?
-
Для точечного заряда понятие "вращение" неприменимо (не может точка вращаться). Если речь идёт о магнитном моменте электрона, то он наблюдаем только в движении. Попытка представить спин электрона как результат вращения заряженной сферы конечного размера, приводят к абсурдной величине тангенциальной скорости - намного больше скорости света. Если речь идёт о заряженных телах, то тут всё может быть - и притягивание, и отталкивание - смотря какая конфигурация зарядов.
- 21 ответ
-
- 1
-

-
Гидролизуется он всё же быстрее этилацетата - из-за более высокой растворимости, лучшей стерики и кислотности метанола.
-
Во-первых - в условиях "углеводород". Во-вторых - нарисован 2,3-диметилгидрохинон, а он озоном развалится совсем не так. В-третьих - "окислительное расщепление" - это стадия озонолиза, расщепление озонида, а не отдельная реакция. Итого - вы, батенька - того... P.S. Несколько туманная формулировка. Можно двояко понимать. Правильнее было бы: или
-
А тут синилка не будет примесью? C 30%-й кислотой, она почти количественно выходит при 60С
-
Триэтиленгликоль и диэтиленгликоль, как и все полигликоли получаются из окиси этилена, на кухне их не сварганишь.
-
По Вильямсону. Триэтиленгликоль -(SOCl2)-> бис-(2-хлорэтокси)этан бис-(2-хлорэтокси)этан + диэтиленгликоль + 2NaOH -> сабж. В диэтиленгликоле растворяется щёлочь, тудой дозируется бис-(2-хлорэтокси)этан. Лучше всего NaOH работает, катион натрия координирует циклизацию.