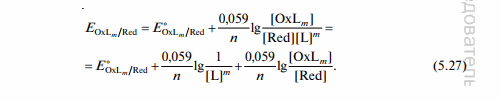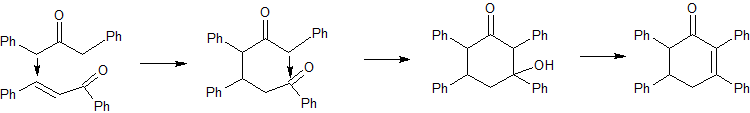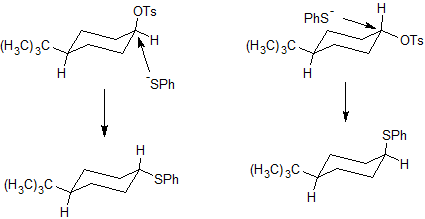-
Постов
34254 -
Зарегистрирован
-
Победитель дней
1129
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
При кипячении водного раствора малоновая кислота разлагается с выделением газа: HOOC-CH2-COOH -> CH3-COOH + CO2
-
- 2 ответа
-
- 2
-

-

-
нарисуйте нитро-группу в пара-положении к любому из гидроксилов а потом нарисуйте второй изомер, где нитро-группа располагается в орто-положении к любому из гидроксилов
-
Просто в стакане упаривать - плохая затея. По вакуумом ещё куда ни шло. Можно высадить спиртом, или ацетоном. Он в воде хило держится. На фильтре надо промыть спиртом и сушить в эксикаторе над KOH. На воздухе быстрее разложится, чем высохнет.
- 3 ответа
-
- 1
-

-
Ну как он может быть "один и тот же"? У метанола свой водород, у кислоты - свой. Другое дело, если их смешать, тогда уже не поймёшь - где чей.
-
Действительно - странно. Никаких упоминаний о конденсации глиоксаля кроме как с азотсодержащими.
-
А откуда такие сведения? Что - реально реакция останавливается на альдольной стадии, а дальше - ни-ни?
-
Дибензилкетон имеет метиленовую группу, которая активируется этилатом. Первая стадия - межмолекулярное нуклеофильное присоединение к сопряжённому кетону по активированной кратной связи [Ph-CH=CH-C(Ph)=O Ph-C+H-CH=C(Ph)-O-]. Вторая стадия - внутримолекулярная альдольная конденсация с тем же катализатором. Потом - кислотно-катализируемая дегидратация промежуточного спирта.
-
Имеется в виду 1,2,4-тиадиазол? Как продукт димеризации с участием серы? Если кипятить бензонитрил с серой (при 190С) наверное реакция будет. Но при такой температуре у ацетонитрила и алкильный хвост обсерится...
-
Поставить в пустую тягу, включить на полную мощность и подождать, пока не перестанет дымиться/гореть.
- 3 ответа
-
- 1
-

-
А чем отличаются десять электродов по 1 кв. см. от одного электрода в 10 кв. см.? Непроизводительные потери энергии определяются разностью между равновесным (теоретическим) потенциалом разложения вашего электролита и напряжением на ячейке. Увеличивая площадь электрода вы уменьшаете эти потери. Но эти потери и так не слишком велики - ну пять процентов, ну - десять. Для производства - существенно, для лаборатории - нет.
- 8 ответов
-
- электролиз
- электрод
-
(и ещё 2 )
C тегом:
-
Тионилфторид сам по себе - малореакционноспособен. Даже с водой практически не реагирует (надо отметить - при этом он ядовит жутко, хуже фосгена, и не имеет ни вкуса, ни запаха). А вот в среде HF - очень активен, той же водой гидролизуется мгновенно. В сухом виде реакция сомнительна, в среде HF - вероятна.
-
С изонитрилом будет. С нитрилом - нет.
-
Так ведь субстрат-то - славянский. Матрица готова, надо подержать в тепле подольше. Вряд ли там Чужой вылупится. А уж откуда мыши в корзине с грязным бельём - зародились, или релоцировались - постфактум уже ничего не докажешь
-
А я и не утверждал, что эти "чертежи" вариативны. Одну молекулу поменять нельзя. Можно только взять другой чертёж. Но ведь и чертёж не возникает сразу из ничего и во всех подробностях. Чем проще чертёж - тем больше вариаций он позволяет. А уж по мере усложнения вариативность, естественно - падает. Тут есть ещё один момент - наследуемость может быть множественной, т.е. разные исходные чертежи по мере усложнения могут привести к одному и тому же результату, а это ещё более расширяет "обратную" вариативность и возможную базу возникновения конкретного чертежа. Ну, это как в России - если разобрать машинку Зингера, то при попытке собрать её снова, скорее всего получится автомат Калашникова Все слабые ростки новой жизни мгновенно поедаются местными обитателями. Высокоразвитая биота - это самый оголтелый и жестокий расист.
-
Трет-бутильная группа фиксирует конформацию циклогексана - она должна быть в экваториальном положении, конформер с аксиальным трет-бутилом - сильно заслонённый, и в равновесии практически отсутствует. Соответственно, в цис-транс-изомерах тозилата создаются разные стерические условия при атаке тозилатной группы нуклеофилом. Атака идёт с тыла, и в транс-изомере это направление стерически более загружено. Другой фактор - энергия самих изомеров и продуктов. В цис-изомере тозилатная группа вынужденно находится в аксиальном положении, и энергия этого изомера выше из-за заслонений. При этом из цис-тозилата получается транс-продукт с экваториальным расположением тиофенила. А в случае транс-тозилата картина обратная - из более стабильного экваториального изомера тозилата получается менее стабильный аксиальный фенилмеркаптан. Оба фактора работают в одном направлении. А виной всему этому безобразию - толстяк трет-бутил.
-
Чисто из вежливости. Скажи это себе. Ибо невежественный болван - это ты. Но это пол-беды. Беда в том (твоя беда), что ты - тупой болван. Вот это - катастрофа
-
Пока что это ты с упорством идиота пытаешься что-то мне доказать (если это можно так назвать). Мне-то давно уже на тебя насрать, а вот ты, походу страдаешь - который раз уже ты про бордосскую жидкость и порох вопрошаешь? Не надоело эту вату жевать? Ты - идиот, могу ещё раз это повторить. И не страдай больше - прими это смиренно. Ну - идиот, ну и что теперь - стулья ломать?
-
Направленную эволюцию. Мы не наблюдаем спонтанного построения сложных молекул потому что делаем всё, чтобы этого не случилось. Если вычислить вероятность осуществления конкретного расположения молекул газа в объёме 1 литра в определённый момент времени, то получится невообразимо малое число. Тем не менее, какая-то комбинация реализуется постоянно. Так же и с биологиею - почему-то априори считается, что жизнь возможна только на основе данного, наблюдаемого, конкретного набора аминокислот, сахаров, ферментов, азотистых оснований и прочего инструментария производства строго определённой фирмы строго по одобренному комплекту чертежей. Это - произвольное допущение, не имеющее никаких доказательств. Вполне возможно, что жизнь возникает всегда и везде, когда и где для этого складываются условия. А вот конкретная реализация - уже дело как раз условий, и - возможно - случая. О числа вариантов реализации мы не имеем никакого представления, даже примерного, поэтому толковать с важным видом о "невероятности спонтанного возникновения жизни" - это толочь воду в ступе
-
Надо прохлорировать дважды, просто навесить два хлора, а не один. Полученный α,α-дихлорэтилбензол гидролизовать водной щёлочью в ацетофенон. Ацетофенон бромируется в м-положение. Потом восстановить м-бромацетофенон в спирт, и дегидратировать его.
- 1 ответ
-
- 1
-

-
Время. Как раз термодинамика не запрещает никакую реакцию. "Реакция не идёт" - это означает или "реакция идёт слишком медленно для разумного времени ожидания" или "равновесие в реакции неблагоприятное для разумного количества циклов изоляции продукта". Это всё - "кочка зрения" Скажем, для дрожжевого грибка период созревания браги - это целый ряд цивилизационных эпох, эонов, в течении которых меняются тысячи поколений, рушатся и воздвигаются царства, меняется климат, вселенная приходит к новому состоянию.
-
Почему не триллион? Сразу. Неудачники вымерли.
-
Натрием в спирту (по Буво-Блану) восстанавливаются сложные эфиры, хлорангидриды, нитрилы кислот. У многоосновных кислот селективно восстанавливаются только этерифицированные карбоксилы. Так что - да, карбоксилат-анион только ЛАГом и окучишь.