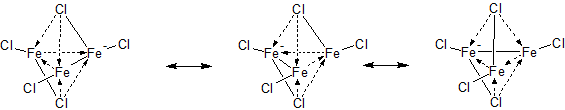-
Постов
34959 -
Зарегистрирован
-
Победитель дней
1166
Весь контент yatcheh
-
ДНК - бесполезная штука. Начинать надо с РНК, с синтеза белков. ДНК - более позднее изобретение. В восстановительной атмосфере в присутствии воды, аммиака и метана, при воздействии электрических разрядов достаточно уже просто большой лужи жидкой воды, что бы там получился бульон, проявляющий эффекты ферментативного катализа. Ферменты случайные, примитивные, но уже - ферменты.
-
А как вы представляете его конструкцию? Там должно быть железо(0) в составе, или трёхъядерный комплекс Может получаться в реакции хлористого железа с гидридом лития: 3FeCl2 + 2LiH => Li[Fe3Cl5] + LiCl + H2 Откуда дровишки?
-
Глупость какая... Жалкая, неумная отмазка.
-
Ну да, в ассортименте
- 4 ответа
-
- 1
-

-
Мнится мне, что тут будет смесь получаться всяких сер. От серы(2) до серы(6). В том числе и тионил.
- 4 ответа
-
- 1
-

-
Блин... коллега, это же - мем... Автор - Юлия Латынина, заслуженная стрелка осциллографа либершизы.
- 71 ответ
-
- 1
-

-
Да? ... Да. Я лажанулся, тут немного сложнее Нафиг, лучше я пока не буду задачки решать. Туплю.
-
"Свободная воля" - ну, вы, батенька, и загнули... Хотя, для русской души оно, может и занятно. Но сначала надо бы разобраться со "свободой" и с "волей". Волю - это мы сразу понимаем - что хочу, то и ворочу - моя воля! Вот со свободой проблема - тут начинаются градации - тут играем, тут не играем, тут рыбу заворачивали... Начинается бодяга с законоустановлениями, с законоисполнением... И вся история государства Российского сводится к боданию воли со свободой. Так что вы уж, полегче, с такими сильными средствами
-
-
Зато не надо заморачиваться на прикапываение солянки. Сидишь, такой, в халате, продвинутый - крутишь ручку и следишь за стрелкой осциллографа, а лаборант тебе пальцами показывает - "прикрути, шибко пошло", "добавь - тупить начало". И ты весь такой диджитальный, с компьютером, в халате опять же... (а, уже говорил). Научно всё, как в этом, как его, чёрта - в андронном коллайдере!
- 71 ответ
-
- 2
-

-
Да только что придумалось. Просто в вики про соли меллитовой кислоты пишут - ах, какие устойчивые, вот и подумалось - надо как-то это использовать...
-
Бро, это называется - перераспределение прибавочной стоимости. Она создаётся конструкторами, изготовителями, и службой технической поддержки роботов. Пользователь роботов может получить барыш как бонус в конкурентной борьбе, но попадает в полную зависимость к производителю роботов, и его конечная роль - роль потребителя, а не производителя. От своих роботов он получает не прибавочную стоимость, а зарплату, как любой наёмный менеджер, и уровень этой зарплаты контролируется производителем роботов. Бро, ты же - марксист, как ты не можешь не понимать таких простых вещей?
-
1,2-дибромянтарная кислота - соль - сплавление до одури с двумя эквивалентами щёлочи - натриевая соль меллитовой кислоты. Соли её (меллитовой кислоты), судя по википедии - в короне Солнца выживают, значит всё должно к ним скатываться
-
Блин блинский! А тут уже и вещество новое схимичили - полимерный фторборат, и реакцию заодно новую открыли - растворение золота в трёхфтористом боре! Вы - могильщик науки!
-
0.2 моль квасцов = 94.88 г Из 100 г насыщенного при 60С раствора при охлаждении до 10С выпадает 24.8-4=20.8 г квасцов. 94.88 г выпадет из 94.88/20.8*100 = 456.15 г насыщенного при 60С раствора. Значит надо взять 456.15*24.8/100 = 113.12 г квасцов и 456.15-113.12 = 343.03 г воды. При условии, что растворимость указана в граммах на 100 грамм раствора для додекагидрата.
-
"Крикливое большинство" - это что-то новое, доселе невиданное. Сначала веков крикливостью и борзостью отличались всякие меньшинства. С тех пор ничего не изменилось. Большинство молчит, ему некогда - надо пахать, содержать крикливое меньшинство, а то - без петухов останемся - солнышко не взойдёт
-
Лестница Пенроуза в доме Эшера. Ну, как получилось - так получилось...
-
При атаке в положение 4 в делокализации заряда сигма-комплекса участвует амино-группа. При этом область делокализации максимально удалена от обоих нитро-групп и испытывает минимальное влияние их индуктивного эффекта.
-
Нет, конечно. Непредельные реагируют на ура. Спирты тож (первичные и вторичные). С кратной связи CrO3, как кислота Льюиса, сразу сдирает пару электронов и даёт циклический эфир (уже за счёт раскисления хрома), гидролизующийся в спирт. Со спиртом - тоже получается эфир, в котором альфа-водород активирован и легко перемещается к хрому, образуя альдегид (и дальше - кислоту). За карбоновую кислоту зацепиться трудно - карбоксил уже окислен до упора, а хвост - углеводород, тоже некуда приткнуться. Для окисления карбоновой кислоты надо рвать связь С-С уже на первой стадии, а зацепиться не за что. Вот и приходится нагревать. Многие вещества с чистой CrO3 реагируют бурно - с воспламенением, так что это не метод.