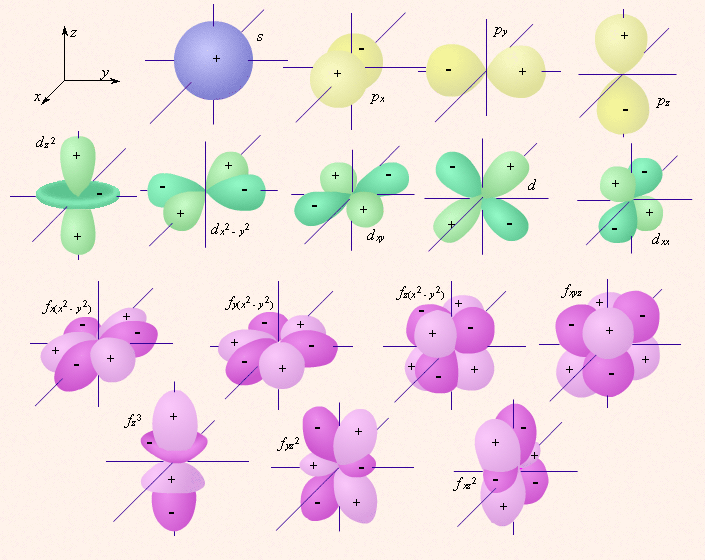-
Постов
4587 -
Зарегистрирован
-
Посещение
-
Победитель дней
19
Тип контента
Профили
Форумы
События
Весь контент Shizuma Eiku
-
Это общая реакция для всех веществ в которых есть Cl+ в нейтральной или кислой среде, Cl-+Cl+->Cl2. Она представляет главную проблему при работе с гипохлоритами т.к. удалить хлориды из них очень трудно. Сразу по нескольким направлениям, от ацетона останутся рожки и ножки, думаю что основным продуктом будет хлорпикрин т.к. он часто образуется при одновременном деструктивном хлорировании и нитровании органики. Его еще получить надо сначала как-то... По-серьезному, реакции органических веществ с такими реагентами нужно проводить в разбавленных растворах в подходящем инертном растворителе. И не факт что CCl4 не будет нитроваться ClNO3 до хлорпикрина. CF4 при температуре жидкого азота как среда был бы отличным вариантом, вот в таких условиях что-то интересное получить можно.
-
Эта реакция идет выше 100 оС, причем при щелочном рН. Если уж сравнивать SnCl2 с гидразином, то первый окисляется и при обычной температуре. Интересно, а что если хромпик использовать? Дихромат эффективное средство против коррозии стальных труб. Я бы выбрал ник связанный с котиками, но уж какой есть, такой есть. В молекуле HN3 один атом азота пятивалентный, по сравнению с гидразином, азот там куда более окисленный.
-
Учитель просто заинтересовал детей своим предметом, это не говорит что они будут знать и понимать физику школьного курса. По большому счету, дети должны учить предметы и без заинтересованности в них т.к. учеба это их работа, а харизматичных учителей меньшинство, на всех их не хватит. Я ответил про заряды - кулоновские силы слабы в масштабах атома и электронов. Вообще нет. Чтобы понять принцип неопределенности математика не нужна. Поведение электрона в пространстве атома выражается вероятностью; запрет на 100% вероятность пребывания электрона в точке следует из принципа неопределенности. Атомная орбиталь - область пространства с высокой вероятностью обнаружения электрона (90% или 95%), форму сферы она имеет далеко не всегда, в большинстве случаев форма орбитали отлична от шарообразной: В атоме у электрона нет траектории по которой он движется, есть лишь вероятность обнаружить его где-либо. А в чём проблема-то?
-
Действительно, причем тут кислород при восстановлении или окислении спиртов или фенолов, вот горе-то какое, что в реакциях вроде 2RCH2OH+2HI->2RCH3+H2O+I2 или окислении гидрохинона/восстановлении хинона, кислород не окислитель, ведь он не меняет степень окисления... На самом-же деле, степень окисления - величина формальная и может быть принята любой; при соблюдении прочих правил уравнивания, ОВР уравняется То что кислороду при расстановке степеней окисления чаще всего ставится -2, не означает, что он присоединил два электрона и образовал ионную связь с зарядом -2 на себе, вообще говоря, ион О-2 большая редкость. Соответственно, неверно считать что если кислород не поменял степень окисления то молекула не окислилась. Например, в случае восстановления спиртов, подразумевается удаление кислорода путем восстановления гидроксигруппы, что и происходит; в случае восстановления хинона наоборот - удаления кислорода из молекулы не происходит, но сама передача электронов - на вполне реальном, а не на формальном уровне - происходит через них, когда электрон присоединяется к кислороду О=С< с образованием аниона. Яцех, SnCl2 сильный восстановитель, он окисляется воздухом. Для сравнения - гидразин уж насколько сильный восстановитель, а его растворы воздухом не окисляются. Да, я тоже как-то так подумал о реакции вроде N2H4+4[H]->N2+4H2.
-
Уротропин из "сухого топлива" лучший вариант т.к. он доступен и его много. По эффективности ингибиторы растворения металла не сильно отличается друг от друга - любое средство для снятия ржавчины (хоть покупное, хоть самодельное), с любым количеством ингибитора, при нагревании довольно быстро разъедает железо. ПАВ не сильно помогают для снятия коррозии или грязи с железа. Самый лучший и самый простой вариант это лаурилсульфат натрия, который является главным моющим компонентом в любых жидких моющих средствах (жидкости для мытья посуды, гелях для душа, шампунях, жидкости для мытья пола и т.п. - всё это на самом деле очень близкие по составу смеси). К готовому составу с кислотой и уротропином добавить примерно четверть неразбавленного жидкого моющего средства, в кислой среде лаурилсульфат натрия пенности и моющих свойств не теряет. Сомневаюсь т.к. нитритная соль это почти чистая поваренная соль, а NaCl будет лишь способствовать коррозии. Также сомневаюсь что нитрит в разбавленном растворе всерьез защитит железо от коррозии. С нитритом натрия действительно есть составы для создания черных оксидных пленок на железе, но он там не главный компонент, основной компонент - NaOH, к которому (в зависимости от конкретного состава) в разных пропорциях добавлены нитрит натрия и нитрат натрия, но эта смесь работает не в разбавленном растворе, а выше 100 оС, в очень концентрированном растворе или в расплаве. Нет, у них у всех будут свои составы. Медь, бронза и латунь будут хорошо чиститься растворами содержащими аммиак (более мягкая альтернатива - смесь растворов аммиачной селитры и кальцинированной соды), а алюминий можно только заново отполировать т.к. он не корродирует, но сильно царапается. Также многое зависит от конкретного предмета и задачи - если речь идёт о чистке очень сильно прокородировавшей, но ценной медной монеты, может будет нерационально растворять продукты реакции меди с окружающей средой, а лучше будет использовать гидразин, который восстановит продукты коррозии обратно в металл. Иногда была цель почистить железо, по моему опыту, для этого нету ничего лучше, чем раствор трилона Б. Главное его преимущество - нейтральная рН среды, поэтому раствор трилона Б растворяет только ржавчину, но не металл под ней - можно надолго замочить изделие в растворе и забыть, или долго кипятить предмет в нём. После удаления ржавчины нужно взять тряпку или губку, тщательно вычистить с моющим средством (или с чистящим порошком) изделие от сажи, быстро (желательно до получаса) высушить и протереть минеральным маслом или оксоль-олифой. После этого у предмета будет более-менее приличный вид, он будет равномерным, серо-черным, без коричневых пятен и не будет корродировать на воздухе. Но, т.к. поверхность была изъедена коррозией, блестеть она не будет без полировки, какое бы средство не использовалось. Поэтому иногда проще почистить железяку наждачкой.
-
Труден, т.к. выход будет ничтожным. Даже карбамид+гипохлорит куда проще.
-
Оксиды многовалентных металлов наверняка будут разлагать - MnO2, PbO2 и т.п. Однако, откуда смесь хлора с его закисью и почему хлор нужно очистить от неё? Во-первых, обычно стоит обратная задача, во-вторых, в присутствии воды Cl2O это то-же самое что и HClO, а последняя образуется в т.ч. и при гидролизе хлора т.е. разница весьма условна.
-
С методической точки зрения это невозможная ситуация; разве что группы будут в несколько человек и предмет ну очень простым. Поскольку волновые свойства электрона выражены явно, то рассматривать электрон как шарик нельзя заранее. Вероятность нахождения электрона в некоторой точке пространства никак не противоречит тому, что полностью находиться в этой точке он не может по принципу неопределенности Гайзенберга. Если бы электрон находился бесконечно точно в определенных координатах, то имел бы бесконечно большой импульс; в реальности электрон "размазан" по пространству, просто в разных точках, вероятность обнаружить его разная. Почему именно так происходит можно без особого труда обосновать математически (да и просто рассуждая; на самом деле, принцип неопределенности можно вывести умозрительно, не используя не единого символа или числа), но истинные причины таких свойств у объектов микромира пока неизвестны. Однако, то что непонятны фундаментальные причины свойств, вовсе не означает что неизвестны сами свойства, именно обсуждаемые свойства электрона изучены и объяснены давным давно, эти объяснения связаны с математикой, отсюда и рекомендации от участников форума изучить их, используя математический аппарат.
-
Это преувеличение. Если в воздухе есть стирол, то это невозможно не почувствовать, стирол вонючий, это не говоря уже что изделие из полистирола сначала бы потеряло свою форму, а лишь потом начало бы разлагаться на мономер.
-
1 Нет. Если железо на аноде (подключен +) и электролит хлорид натрия, то оно будет растворяться и будет образовываться грязно-зеленая смесь гидроксидов двух и трехвалентного железа. Если на катоде, то на нем будет выделяться водород. Черный, липнущий осадок при растворении железа это сажа, она остается при растворении чугуна или металла инструмента, который был подвергнут науглероживанию (цементации), там получается очень явная граница - черная там где науглерожено и светлый металл где нет. 2 Счистить щеткой/ тряпкой с ПАВ - мылом или жидким моющим средством.
-
Это оксидная пленка удалилась с поверхности, плюс следы электролита, способствующие коррозии. Надо железяку хорошо вымыть, высушить, и протереть маслом.
-
Нет, это глупость. Чтобы происходил электролиз обычно достаточно очень небольшого напряжения порядка нескольких вольт, но скорость электролиза зависит от силы тока, а та через закон Ома от напряжения. Поэтому напряжение на ячейке регулируется из соображений получить нужную силу тока, оно всегда выше минимального.
-
В большинстве случаев примеси в электролите убивают кислотный аккумулятор. Если они могут окисляться и восстанавливаться, то приводят к быстрому разряду. Органика окисляется на аноде т.к. PbO2 сильный окислитель, хлориды, нитраты и т.п. минеральные ионы вызовут разрушение анода. Вроде, сульфат магния применялся в каком-то рецепте для восстановления аккумулятора, кроме того, для снятия сульфатации предлагалась смесь каких-то полифенолов (уже не помню о чём конкретно шла речь).
-
Если нужна концентрация как в книжке, то на 1 объем электролита надо добавить 2.5 объема дистиллированной воды, будет примерно 12% серная кислота (р=1.08). Но вообще, электролит не нужно разбавлять как таковой, он уже разбавлен до нужной концентрации. Концентрация кислоты связана с циклом разрядки/зарядки аккумулятора, если электролит не выливался из аккумулятора, то доливать новую серную кислоту в него не нужно т.к. сульфат-анион никуда из аккумулятора не делся. При зарядке аккумулятора концентрация кислоты повысится до нужной сама по себе. Напряжение на клеммах аккумулятора ни о чем не говорит. Если взять убитый аккумулятор и залить в него свежий электролит, то напряжение повысится почти до нормального и аккумулятор даже будет немного заряжаться с повышением напряжения (13.5В как минимум для 6 ячеек). Это происходит потому что ЭДС ячейки зависит от концентрации серной кислоты. Однако, ёмкость (т.е. сколько А*час может выдать аккумулятор) какой была ничтожной, такой и останется, аккумулятор будет очень быстро разряжаться, запитать с него можно будет разве что несколько светодиодов. Для зарядки аккумулятора подходит любое зарядное устройство, выдающее напряжение минимум 14-15В постоянного тока. Кислотные аккумуляторы, вообще говоря, можно заряжать даже сетевыми 230В, выпрямленными через диод или диодный мостик, главное ограничение силы тока (в случае 230В оно достигается подключением последовательно лампочки накаливания). Вроде даже считается что большие напряжения (или большие значения силы тока) полезны для снятия сульфатации, но на практике, сульфатацию так просто не снять. Проще сдать умерший аккумулятор и купить новый. Анод там еще интереснее, он состоит из смеси оксидов свинца, при прокаливании можно PbO получить, а при обработке щелочью ярко-красный свинцовый сурик получается.
-
Увы, углерод максимум четырехвалентный.
-
Там проблема скорее в том что нужно очень много хлора и его трудно полностью использовать. Именно по ароматическим карбоновым кислотам трудно сказать, но вроде ацетат алюминия, либо безводная смесь ацетата натрия с сульфатом алюминия, при сухой перегонке дают уксусный ангидрид. Для других карбоновых кислот должны быть соли, разлагающиеся с выделением ангидридов. Теоретически, можно попробовать заменить сульфат алюминия на хлорид, может будет хлорангидрид, хотя при наличии ароматического ядра, в присутствии алюминия, наверняка пойдет реакция Фриделя-Крафтса.
-
По-моему, главные свойства CCl4 это его инертность к хлорирующим агентам, его растворяющая способность и низкая температура кипения. Он растворяет NCl3, давно хотел попробовать как такой раствор будет взаимодействовать со склонной к реакциям присоединения органикой. NH2Cl тоже интересно, по идее, он может растворяться в CCl4.
-
Можно взять избыток диметилсульфоксида, а серы гораздо меньше чем нужно по уравнению; продукты реакции можно разделить перегонкой.
-
Электростатические силы слабы относительно других взаимодействий в атомах. Вероятно, сильное взаимодействие, и получило своё имя поэтому. Просто есть физика макромира, базирующаяся на теории относительности, а есть квантовая теория, несовместимая с теорией относительности, но хорошо описывающая микромир, которая и используется в химии. Хе, а с моей точки зрения пространство теории относительности, которое просто существует и по которому просто распространяются электромагнитные волны, наивно и неадекватно. Учёные давно над этим бьются, но из всевозможных теорий всего пока можно сделать можно лишь два противоположных предположения: 1 Либо мироздание чрезвычайно сложно для нашего восприятия и мы имеем дело с очень сложным и многомерным мирозданием (как минимум около десятка или больше измерений). 2 Либо мироздание в реальности более простое, но мы (в силу самого человеческого, бытового, мышления) что-то упускаем.
-
Это просто рисунок; можно считать что находиться электрон в ядре практически не может, вероятность обнаружить его там ничтожна. Скорее, было наоборот - сначала в результате большого числа физических и химических наблюдений пришли к выводу что существует электрон, его заряд оказался -1, соответственно у ядра заряд положительный. Обычно используется выражение вроде "падение электрона на ядро". Тут нужно помнить, что электрон не является шариком, вращающимся вокруг ядра и имеющим точное положение в пространстве. Вместо этого, в квантовой теории используется вероятность обнаружения электрона в той или иной части пространства. Вероятность обнаружить электрон в ядре очень мала, само ядро имеет чрезвычайно высокую плотность и мало по сравнению с условными размерами атома и теми областями пространства, в которых вероятность обнаружить электрон высока. Электростатического взаимодействия ядра и электрона/ов недостаточно, чтобы повлиять на вероятность нахождения электрона настолько, чтобы он оказался в ядре. Тем не менее, в случае радиоактивного распада атомов, есть определенная вероятность что электрон из ближнего к ядру уровня будет им захвачен; это явление называется электронным захватом - протон ядра захватывает электрон атома, превращаясь в нейтрон и нейтрино, образуется новое ядро и новый элемент. Именно потому что используются вероятностные характеристики, некорректно утверждать что электрон пребывал в ядре или не пребывал там.
-
Это сложная техническая задача т.к. гибкими в основном являются металлы или органические полимеры, вторые имеют низкую электропроводность, их механические свойства являются приемлемыми лишь в узком интервале температур. Среди сплавов есть такие которые становятся более пластичными при охлаждении, хотя речь идет о достаточно сильном охлаждении (например жидким азотом), вроде никонель к таким относится. Т.е. можно сделать нужную деталь, поместить ее в охлаждающую среду и для уменьшения пластичности греть током, поскольку пластичность в данном случае будет зависеть от температуры, то путем регулирования температуры, можно регулировать и пластичность. Второй вариант не столько химический - можно попытаться использовать обратный пьезо-эффект. Если вещество (там скорее будет не индивидуальное вещество, а какой-то материал) известно, например, из патентов, то синтезировать его будет относительно просто.
-
Может, очень небольшие количества ртути, если цинковый стаканчик был амальгамирован. Сам цинк солевых батареек может содержать немного кадмия (0.05%) и свинца (0.5%). Фотографии интересны тем, что на них действительно попали два разных типа батареек. Те что панасоник щелочные, а минамото солевые (вероятно); с химической стороны они близки, у обоих катодом является MnO2, анодом цинк, разница в электролите, в щелочных батарейках это КОН, в марганцево-цинковых элементах это NH4Cl. На физическом уровне, цинковые и солевые элементы очень разные, плюс, сами солевые батарейки могут отличаться в исполнении. Тип указан на этикетке, обычно на щелочных батарейках специально пишется что они щелочные, если ничего не написано то это наверняка солевая батарейка. Токсичность у них чрезвычайно низкая, теоретически, они не должны быть опасны и при проглатывании т.к. цинковый стаканчик не успеет раствориться. Явно ядовитых веществ в них нет.
-
Это общая проблема всех резин - при хранении на открытом воздухе они медленно "сохнут", становятся более твердыми, ломкими и теряют эластичность, при хранении в масле пропитываются им, увеличиваются в размерах, в обеих случаях происходит потеря прочности. Поэтому в идеале резину нужно хранить как она хранится от производителя - поверхность изделий должна быть пересыпана тальком, они не должны соприкасается, масла быть не должно, а сама резина должна быть закрыта в пакете. Я смазывал резину и силиконовым и минеральным маслом, в общем, чистое силиконовое масло гораздо слабее просачивается в резину чем минеральное, но просачивается и оно. Химическая стойкость резины особой роли не играет, например, я делал круглые клапаны для насоса из резины маски противогаза и его клапана, потом подумал, а почему бы для лучших механических свойств не оставить прокладки в ДТ на сутки, так на следующий день они почти вдвое увеличились по диаметру и стали мягкими. А это химически стойкий сорт резины. Полипропиленовую тару ДТ тоже так пропитывает, что пластик становится очень гибким. Из этого всего следует совет что нужно индивидуально подходить к каждой резиновой детали и те которые не старые, смазывать нельзя.