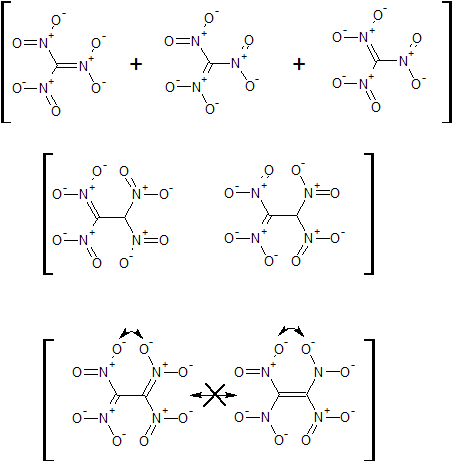-
Постов
33176 -
Зарегистрирован
-
Победитель дней
1100
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
В тринитрометане заряд аниона делокализуется тремя нитро-группами, а в тетранитроэтане - только двумя. Группировка -CH(NO2)2 действует только индуктивно, а это куда более слабый эффект. Дианион из-за аномерных зарядовых эффектов не может быть плоским и сопряжённым, а это - дополнительный фактор дестабилизации.
-
Ну, если с динитрометаном сравнивать (pKa=3.6) и тринитрометаном (pKa = 0.25), то по первой ступени будет где-то 1.5, а по второй - существенно меньше (5-6). Но соли с тяжёлыми металлами будут. Скажем - PbC2N4O8
-
5% HF спасёт отца русской демократии...
-
Да какой тут бомбизм с такой экзотикой. К статье 205-й через 223-ю есть куда более простые пути. Ну да, есть интерес у юного химика к дьявольским веществам. А у кого его не было?
-
Да, это какая-то бессмыслица получается. Видимо, тут не всё так просто. Раствор нитрата магния подвержен гидролизу, и растворение оставшегося гидроксида будет идти по реакции образования основного нитрата. Т.е. в растворе будут присутствовать ионы Mg2+, Mg(OH)+ и NO3-. В осадке - избыток Mg(OH)2. Вопрос - какова будет равновесная концентрация ионов Mg(OH)+ Тогда можно вычислить общую концентрацию магния в растворе, и его избыток, перешедший из гидроксида. Как тут обойтись величиной ПР я чего-то не могу сообразить.
-
Вещество А во всех трёх реакциях одинаково. При гидролизе трихлорметилбензола получается бензойная кислота. Кумол окисляется в гидроперекись только непосредственно кислородом и его расщепление до фенола - уже другая реакция, требующая других условий. Перманганат, бихромат окисляют его до бензойной кислоты. А - бензойная кислота B - бензоат кальция. C6H5-COOH + 3KCl + H2O
-
Последняя стадия - реакция Трофимова. Получается 2-метилпиррол. Странно, что условия не указаны, в этой реакции это важно.
- 2 ответа
-
- 1
-

-
Если бы в первой реакции было 4KOH а не не 3KOH, то получился бы бензоат калия. Во второй реакции окислителем может быть, Скажем, KMnO4 + H2SO4 Третья реакция - обычная реакция нейтрализации с образованием соли.
-
Половина из 0.1 моль Mg(OH)2 прореагировала с HNO3 с образованием раствора нитрата магния. Значит надо определить сколько растворится (из оставшегося) Mg(OH)2 в присутствии 0.1 моль/л ионов магния.
-
Давно предлагали. Только назвать его "Халява". Для размещения темы в этом разделе установить особую форму регистрации - надо открыть форточку, бросить в неё монету в пять рублей, и трижды прокричать - "Халява, приди!". Видосик с процессом регистрации отправить Одмину. Приход халявы администрация не гарантирует.
- 4 ответа
-
- 1
-

-
По уравнению Стокса: g = 9/2*VS*μ/r^2/(Pp - Pf), где g - ускорение свободного падения (м/с^2) VS - установившаяся скорость падения шарика в жидкости (м/с) r - радиус шарика (м) Pp - плотность шарика (кг/м^3) Pf - плотность жидкости (кг/м^3) μ - динамическая вязкость жидкости (Па*с) Или речь идёт об истечении из капилляра? Тогда закон Пуазейля для стационарного истечения, но там надо будет разность давлений выразить через плотность жидкости, высоту столба и ускорение свободного падения, после чего обратную задачу решить. Пустая формальность, но мне чёт лениво этим заниматься. -
-
Ломаешь капилляр выше отметки 25С, подогреваешь шарик - получаешь нужное количество. Капилляр можно заткнуть каплей герметика.
-
CH3-Cl + OH- => [HOδ-→CH3→Clδ-] => HO-CH3 + Cl- А к чему у вас там протон болтается с каким-то карбкатионом, неизвестно откуда взявшимся? В переходном состоянии углерод пентакоординирован, и связь С-О образуется одновременно с разрывом связи C-Cl. Кроме OH- и Cl- никакие другие ионы там не участвуют.
-
Да мы подумали, что вы любите жевать вату. Не сахарную.
-
Эта "история" из трёхтомника "Вредные вещества в промышленности". Книжка ещё советская, авторитетная, по каждому чиху - ссылка на литературу. У нас при подобной аварии аппаратчику начальник цеха оперативно выделил 200 кубов спирту. Аппаратчик ушёл домой весёлый и довольный. Да - и не умер
-
Нет такого механизьму. Есть SN1, но это не тот случай.
-
Правильно.
-
Тут две проблемы - относительно невысокая нуклеофильность нитрит-иона и его бидентатность (получается не только нитросоединение, но и эфир - алкилнитрит). Плюс ко всему этому полигалоидалкилы тем менее активны при замещении, чем больше атомов галогена. Поэтому практически в реакции с тетрахлорэтаном и NaNO2 вряд ли вообще что-то получится. Тут надо брать нитрит серебра, тогда может что-то выйдет.
-
Что значит "уже"? pH=3 потому что кислота слабая. Была бы сильная - был бы меньше.
-
Мы не левые, мы не правые, мы - валенки...