-
Постов
33401 -
Зарегистрирован
-
Победитель дней
1107
Тип контента
Профили
Форумы
События
Весь контент yatcheh
-
Зачем? Всему своё время. Я против дутых сенсаций, всего лишь.
-
Ещё один чудотворец нарисовался. Свидетель Церкви Неполживого Ютуба
-
С паром можно основную массу нитробензола убрать, а примесь так не уберёшь. Давление паров у них довольно близки (14 мм рт. ст. при 167C для ДНБ и 30 мм.рт.ст. при 108С для НБ). Тем более, что под паром ДНБ расплавится, будет слабый раствор НБ в ДНБ, из которого НБ не выгонишь - они совместно полетят). Лучше всё-таки перекристаллизовать из спирта.
-
Синтез описан в книге: Карякин "Чистые химические вещества" стр. 345. В сети доступен, но если что - могу скинуть. Собственно, есть два способа - в первом камфору используют как катализатор, во втором - гранулированный активный уголь (можно аптечные таблетки использовать). С углём реакция идёт при 30С. Смесь SO2 и хлора пропускают через боковой отвод в колбу, снабженную колонкой, заполненной углём. Колонку надо слегка подогревать. Образующийся сульфурил капает обратно в колбу. Уголь надо брать в крупных гранулах, шоб не захлебнулось всё нахрен.
-
За такой отчёт о проделанном эксперименте мой научрук меня бы задушил вакуумным шлангом. И правильно бы сделал! Элементарно - вода выпаривалась, а потом началась кристаллизация. При этом, как показывает опыт, испарение растворителя сильно ускоряется, а кристаллизующееся вещество может вспучится и затвердеть в виде пены. Микроволновка - она такая. Рассол греет, а твёрдую соль может перестать греть. Впрочем, я микроволновку только по телевизору видел - не знаю, что там, да как. Вы бы грели на сковородке, как люди - было бы всё проще.
-
Отрицательный индуктивный эффект карбонильной группы увеличивает положительный заряд на атоме углерода в альфа-положении к ней, и облегчает атаку нуклеофила по SN2 механизму. Этот же эффект, с другой стороны, препятствует образованию карбкатиона (акцептор дестабилизирует карбкатион) и тормозит реакцию по SN1 механизму.
-
Ну, тут только одну ещё побочную реакцию можно нарисовать, с образованием ди-н-бутилового эфира: C4H9-OH + OH- C4H9-O- + H2O (равновесная реакция, сильно сдвинутая влево) C4H9-O- + C4H9Cl ----> C4H9-O-C4H9 + Cl-
-
В пробирке? Ну-ну. Никогда такого не было - и вот, опять! Пробирки лечить - здесь вам не тут.
-
Странный способ создавать щелочную среду при помощи кислоты и её соли Добавка ацетата натрия к раствору уксусной кислоты повысит pH ближе к нейтральному. Это, безусловно - негатив. С другой стороны, слабая кислота и её соль - это буфер, что, несомненно - позитив. Повышение ионной силы раствора так же благоприятствует всяким разделениям зарядов, это - тоже позитив. Но в целом, ИМХО - ацетат натрия толи ускорит реакцию, толи замедлит... Греть надо, а не заморачиваться тонкостями теории растворов! Все проблемы химии решаются киловаттной плиткой и синей изолентой (если где-то коротнёт).
-
Дык - понятно... Среда... Третий день работать неохота. Одно утешение - День Народного Единства! Выше нос, гардемарин! Нонче пятница - в четверг!
-
С чего бы? Гидролиз ускоряется кислотами и щелочами. Какую роль сыграет ацетат натрия?
-
И микробы тоже. Но если гидролиз мочевины необратим (а он необратим) - то до равновесной смести карбоната и карбамата всё равно дойдёт, даже в стерильных условиях. Во благовремении...
-
Скоростьлимитирующая стадия в реакции SN1 - диссоциация с образованием карбкатиона. Отсюда и всё вытекает: а) Реакция SN1 приводит к рацемизации, так как карбкатион - плоский. Обращение - признак SN2 б) Увеличение объёма заместителя ускоряет SN1-реакцию из-за стерического "выталкивания" уходящей частицы. Кроме, того, в плоском карбкатионе стерическое напряжение в некоторой степени снимается из-за увеличения углов связей. в) Так как в SN1 реакции нуклеофил в скоростьлимитирующей стадии не участвует, то и на скорость реакции его свойства не влияют. г) Карбкатион в SN1-реакции может претерпевать перегруппировки. д) Реакция SN1 ускоряется электронодонорами, реакционный центр переходного состояния несёт положительный заряд, и значение р* для неё отрицательно.
-
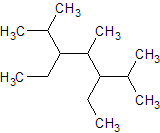
4,5,5-триметилгексанол-2 Получится CH3-CH=CH-CH(CH3)-C(CH3)2-CH3 4,5,5-триметилгексен-2 и вода
-
Не пойдёт.
-
Без нагрева реакция будет долго идти. Но, в конце концов, мочевина и водой рано или поздно разваливается - только погодить надо.
-
Сульфурилхлорид по-крайней мере - жидкий, слегка дымит и сильно воняет. Им отравится куда сложнее. Я с ним работал под тягой, разумеется, но без специальных мер защиты. У него нет фосгеноподобного эффекта, поскольку он относительно быстро гидролизуется, в ткани легких и в кровь не проникает, вызывая только поверхностный химический ожог, что, согласитесь - безусловный позитив
-
CH3-CH2-CH(CH3)-COOH --(Br2, Pкрасн, -HBr)--> CH3-CH2-C(Br)(CH3)-COOH --(NH3 изб)--> CH3-CH2-C(NH2)(CH3)-COOH + NH4Br
-
a) б) 3,3-диметилпропен-1 - неверное название, такого вещества не существует. (CH3)2CH-CH=CH2 правильно называется 3-метилбутен-1
-
Если только в водной кислоте. В безводной кислоте - нет. Какой гидролиз без воды?