-
Постов
5612 -
Зарегистрирован
-
Посещение
-
Победитель дней
28
Тип контента
Профили
Форумы
События
Весь контент Paul_S
-
Нитрование собственно пиридина, особенно нитрующей смесью, когда гетероцикл нацело протонирован, протекает чрезвычайно трудно и практического значения не имеет.
-
Думаю, помогут книги, соответствующие предмету экзамена. А лучше всего - конспекты лекций
-
Это и не нужно. Просто сжигается на блюдечке неколько грамм серы. И самоудалиться нужно на полчаса максимум.
-
Если пиридин действительно сравнит-но дегко бромируется в положение 3, то 3-бромпиридин должен вступать в реакции вполне аналогично бромбензолу. Т.е., можно заменить бром на цианогруппу нагреванием с CuCN и дальше гидролизнуть нитрил в кислоту. Рекомендуют делать это еще и в присутствии тетрафенилпалладия, но в схеме это рисовать необязательно.
-
Почему в клавиатуру? Они там живут? По-моему, тараканам там неинтерено, а у Вас руки постоянно будут в борной к-те, что неполезно. Я как-то избавился от тараканов на кухне через окуривание сернистым газом.
-
1. Делаем из циклогексанона енолят действием, например, диизопропиламида лития, реагируем его с 2,3-дибромпропеном. Получаем вот это: которое в серной кислоте циклизуется в искомый продукт с отщеплением HBr. 2. Фторпиридины можно получить через аминопиридины. 2-аминопиридин получается по Чичибабину действием амида натрия на пиридин, 4-аминопиридин получаетя нитрованием пиридин-N-оксида (получается из пиридина и перекиси водорода в уксусе) с последующим восстановлением 4-нитропиридин-N-оксида гидрированием на платине или цинком в кислоте. 3-аминопиридин можно сделать нитрованием 4-аминопиридина с последующим удалением аминогруппы через диазотированием и действием H3PO2 (сомневаюсь, правда, что здесь будет хороший выход). Получившийся 3-нитропиридин восстанавливаем в амин. Из 3-аминопиридина фторпроизводное получается диазотированием и разложением борфторида диазония аналогично обычной ароматике. С 2- и 4-производными тоже можно нарисовать такую реакцию, но в реальности они диазотруются плохо, особенно 2-амино. Лучше сделать диазотирование гидролизом до пиридонов, а на них подейтвовать SF4. Успехов!
- 4 ответа
-
- 1
-

-
Можно через нитронафталин. Нафталин нитруется без нагревания, получается 1-нитронафталин. Он сульфируется олеумом исключительно в положение 5. Потом нитрогруппа восстанавливается, амин диазотриуется при кипячении. https://ru.wikipedia.org/wiki/Нитронафталины
- 2 ответа
-
- 1
-

-
Его вообще не бывает. Тетраметилортосиликат бывает.
-
Кетон окисляется в карбоновую к-ту (в виде аниона). 5-хлортиофен-2-карбоновая к-та должна получиться.
- 2 ответа
-
- 1
-

-
Хотя, вообще, пишут, что сульфид никеля нерастворим в разбавленных кислотах, стало быть, он будет выпадать вместе с медью и свинцом. Тогда можно ко всей этой смеси катионов добавить избыткок аммиака, в растворе останутся аммиакаты Ni и Cu. К ним добавить раствор перхлората натрия и выпадет [Ni(NH3)6](ClO4)2, он нерастворим. Вот никель и отделен, и никакой диметилглиоксим не нужен
-
Медь и свинец осаждаются в кислой среде в виде сульфидов, железо затем осаждается избытком аммиака. Аммиакаты Ni остаются в растворе.
-
В общем, вот расщепление в поле лигандов по ТКП Mn4+ - это система d3, соответственно, при октаэдрическом расщеплении это будут три неспаренных электрона на нижнем уровне, при тетраэдрическом - либо один неспаренный, либо три неспаренных, из которых один будет существенно выше других по энергии. Очевидно, второй вариант по-любому невыгоднее. Магнитные измерения указывают, что марганец в MnF4 все-таки высокоспиновый. https://onlinelibrary.wiley.com/doi/full/10.1002/zaac.202000048
-
Это можно на разных уровнях объяснять. Можно сказать, что, поскольку в комплексе фтор донирует электронные пары на вакантные орбитали марганца, тем самым высокий заряд металла частично компенсируется, и высокая степень окисления стабилизируется. Если серьезнее, то требуется привлекать теорию кристаллического поля. В тетраэдрическом и октаэдрическом поле лигандов электронные уровни ионов d-металлов расщепляются по-разному, во втором случае электроны размещаются ниже по энергии. Энергия стабилизации кристаллическим полем, есть такая вещь. См. напр, здесь, стр. 559 и далее http://www2.asu.ru/departments/chemistry/site/ncd/novogenov/nc11.pdf Лекции есть на эту тему
-
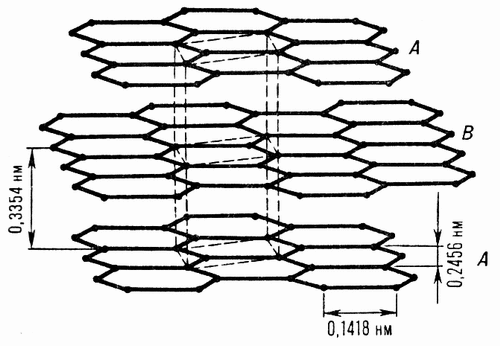
Вот параметры структуры графита, не знаю, почему пропала картинка Да, что-то вроде капиллярной конденсации там может происходить. Но по-любому, это связано с большей способностью неона к ван-дер-ваальсовым, в частности, дисперсионным взаимодействиям. А в принципе, у неона с гелием различие в температуре конденации всего 23 градуса.
-
Вообще-то в задаче рассматривается раствор CH3Cl в C2H5Cl, а не наоборот, ибо первое вещество при нуле Цельсия - газ, а второе - жидкость. Ну да ладно. В растворе - равные массовые доли веществ. При этом, с учетом мол. масс 64,5 и 55,5 мольные доли веществ будут соотноситься как 0,0155 к 0,02, т.е. 43,7 мольных % этилхлорида и 56,3 мольных % метилхлорида. Поскольку давление над раствором создается компонентами независимо, оно будет равно 0,437*0,638 = 0,2788*105 Па плюс 0,563*2,64 = 1,4863*105 Па. Первое слагаемое - парциальное давление этилхлорида, второе - метилхлорида. Массовые доли веществ в газовой фазе пропорциональны их парциальным давлениям. Складывем парциальные давления, находим процентное соотношение. У меня получилось 15,8 и 84,2, примерно как в ответе.
- 2 ответа
-
- 1
-

-
Кстати, говоря серьезно, вот параметры структуры графита При этом диаметры атомов гения и неона примерно 60 и 80 пикометров, т.е., всего 0,06 и 0,08 нм. Т.е., дело не в размере атомов, а в большей инертности неона (в смысле массы атома), а также в том, что он, как и углерод, элемент второго периода, так что его существенно более богатая электронами оболочка легче поляризуема и гораздо более способна к дисперсионным взаимодействиям.
- 4 ответа
-
- 1
-

-
4. CH3-CH(COOMgBr)-CH2-CH3
-
Бутанон гидрируется на платине во втор-бутиловый спирт, который дает с HBr втор-бутилбромид, далее образующий реактив Гриньяра, образующий с СО2 соль карбоновой килоты (2-метилмасляной).
-
Крахмал гидролизуем, глюкозу сбраживаем в этанол, его окисляем в ацетальдегид, из него с аммиаком и HCN после гидролиза получаем аланин (р-ция Штреккера). См здесь http://www.xumuk.ru/organika/406.html Ацетальдегид конденсируем в кротоновый альдегид в присут. щелочи, его гидрируем на платине в бутанол. Из бутанола и аланина в присут. H2SO4 получаем искомое.
-
Первая ссылка, кстати, вполне доступна https://onlinelibrary.wiley.com/doi/abs/10.1002/zaac.19502610312 Röntgenographische Untersuchungen an Einkristallen des CaSi ergaben eine rhombische Zelle mit den Gitterkonstanten Aus der Strukturdiskussion folgt die Raumgruppe