-
Постов
2427 -
Зарегистрирован
-
Посещение
-
Победитель дней
17
Весь контент pauk
-
Различные способы перевода манганата в перманганат перечислены тут
-
Очевидное - невероятное! A - Fe + H2SO4 -> FeSO4 + H2 B - FeSO4 + Ca(OH)2 -> Fe(OH)2 + CaSO4 C - 4Fe(OH)2 + 2NaNO2 + 2H2O -> 4Fe(OH)3 + Na2N2O2 D - Na2N2O2 + 2AgNO3 -> Ag2N2O2 + 2NaNO3 История такова. Недавно я рекомендовал одному любознательному форумцу старинную книгу, а потом решил сам на досуге полистать её. И нашёл этот удивительно простой способ. Даже имя его автора известно (Цорн). В принципе, проверить его несложно даже на коленке. На форуме немало энтузиастов, у которых чешутся руки - чего бы такого сделать? Вот пусть и попробуют, а потом расскажут, что получилось. Гидроксид железа(II) в щелочной среде может применяться в качестве восстановителя даже в органическом синтезе. Но на практике его используют нечасто. Вероятно, мало желающих возиться с отделением продукта реакции от довольно противозной субстанции Fe(OH)3.
-
Предлагаю размяться. Fe [+H2SO4] -> A [+Ca(OH)2] -> B [+NaNO2] -> C [+AgNO3] -> D (жёлтые кристаллы) A - ? B - ? C - ? D - ?
-
Вас какие связующие интересуют? Для строительных работ типа известь/песок/цемент/бетон? Или клеи/цементы/замазки разного назначения? Если второе, то на букву "Г" в интернете есть дореволюционная книга В. И. Губинского "1750 практических техно-химических рецептов". Книга посвящена не конкретно вашей теме, а вообще всему, что может понадобиться в хозяйстве. Вот её титульный лист: Книга не систематизирована по разделам, а все статьи просто помещены по алфавиту, как в энциклопедии. К тому же в ней нет оглавления, так что придётся вам её полистать вручную. Пока доберётесь до нужной статьи попутно огребёте массу полезной информации. В интернете есть ещё аналогичные сборники всякой всячины: Бродерсен Г. Г. - Золотая рецептура (1992) Королёв В. А. - 713 секретов производственных технологий (1992) Одноралов Н. В. - Полезные советы по прикладной химии (1967) Одноралов Н. В. - Секреты мастера (1991) Ратманский М. Н. и др. - Энциклопедия забытых рецептов (1994) Если вас интересуют конкретно фосфатные клеи, то кроме указанной выше книги Сычёва М. М. "Неорганические клеи" за 1986 год, в сети есть ещё книга Копейкина В. А. и др. "Материалы на основе металлофосфатов" (1976).
-
Тут-то я и спалился как резидент британской разведки МИ-6. По ихнему алфавиту это будет 4-ethyl-5-isopropyloctan-3-one.
- 3 ответа
-
- 2
-

-
Насчёт роли AlCl3 у меня была мысль о связывании хлористого водорода в комплексную кислоту H[AlCl4], но формулировка "в присутствии" сбило меня с пути истинного, учитывая ореол славы хлорида алюминия как катализатора. Надеялся уточнить этот вопрос позже, но до настоящего времени ничего существенного откопать не удалось. Насчёт реакции ацетилхлорида с ацетатом - дело в том, что она не вписывается в цепочку. Необходим одностадийный процесс дегидратации УК в УА, из-за чего и разгорелся весь сыр-бор.
-
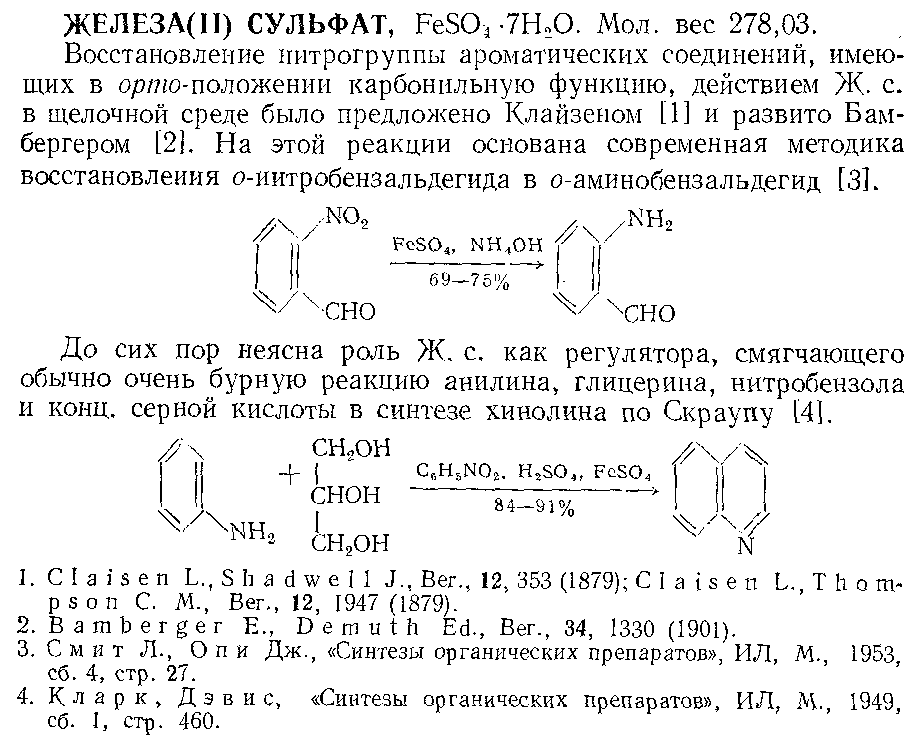
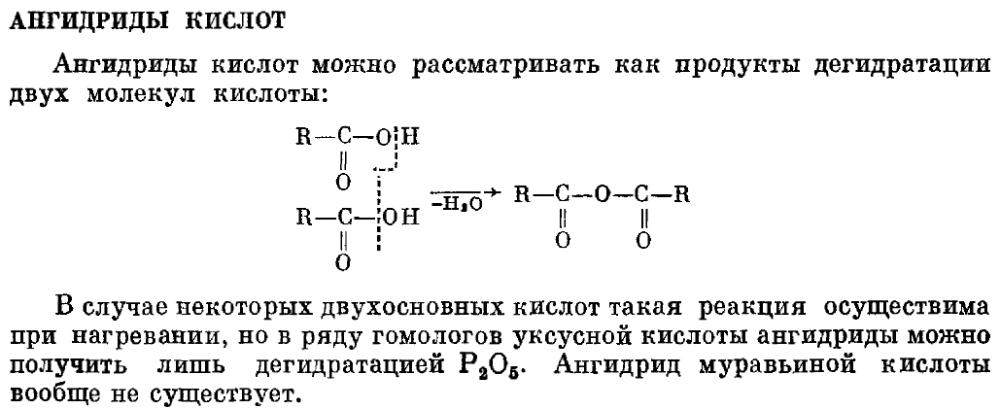
Как выяснилось, в своём сообщении выше по теме я неправильно интерпретировал цитату из ХЭ. Указанное в ней относится к современному двухстадийному промышленному методу получения уксусного ангидрида с промежуточным выделением кетена, который далее вводят в реакцию с уксусной кислотой в отдельном процессе. Дегидратация уксусной кислоты с разделением процесса на две отдельные стадии оказалась значительно рентабельнее прежнего одностадийного метода, так как позволила обойти многие проблемы, присущие процессу в одном флаконе. Но для решения цепочки это обстоятельство не имеет значения. Главное, что существует метод в одну стадию: 2CH3COOH (500°C, катализатор) -> (CH3COO)2 + H2O. Вот фактура из книги Лебедева Н. Н. "Химия и технология основного органического и нефтехимического синтеза", 1988, стр. 189-190: Что касается способов с фосгеном и др. хлорангидридами, то тут фактуры намного меньше. Всё же вероятно, что эти методы существуют, но они настолько реликтовые, что даже в книге Юкельсона И. И. "Технология основного органического синтеза" за 1958 год о них упоминается лишь вскользь, а более поздние статьи в энциклопедиях, например в ХЭ, не намного проясняют ситуацию. Понятно, что для их реализации недостаточно просто от балды смешивать ледянку с хлорангидридами, а требуются гораздо более хитропродуманные способы организации процесса. Но кажется, BritishPetroleum что-то нащупал в этом направлении. PS. Кстати, идея получать ангидриды карбоновых кислот через фосфорный ангидрид не такое уж гиблое дело: Вот бы ещё узнать шо це за гомологи...
-
Кротов тоже. У моих знакомых был кот Мартын, который охотился за кротами на приусадебном участке. Выловленных экземпляров он живыми приволакивал к окошку и показывал хозяевам, держа за шкирку.
-
Это не углеводороды, а карбонильные соединения (альдегид и кетон). Первое название правильное. Второе: 4-этил-5-изопропилоктан-3-он
- 3 ответа
-
- 1
-

-
Потому что с концентрированной серной кислотой при обычной температуре магний не реагирует вообще (пассивируется), а при нагревании протекает ОВР с выделением H2S.
- 2 ответа
-
- 1
-

-
При недостатке KCN происходит выпадение осадка: FeCl3 + 3KCN + 3H2O = Fe(OH)3↓ + 3KCl + 3HCN Или в ионом виде: Fe3+ + 3CN- + 3H2O = Fe(OH)3↓ + 3HCN (совместный гидролиз) Осадок растворяется в избытке KCN: Fe(OH)3 + 6KCN = K3[Fe(CN)6] + 3KOH Или в ионом виде: Fe(OH)3 + 6CN- = [Fe(CN)6]3- + 3OH- (комплексообразование) Суммарно: FeCl3 + 6KCN = K3[Fe(CN)6] + 3KCl Или в ионом виде: Fe3+ + 6CN- = [Fe(CN)6]3- PS. Я невнимательно прочитал ваш пост и не то написал. Избыток/недостаток с концентрацией никак не связан. Но оставлю свой ответ, вдруг он кому-то пригодится в будущем.
-
Бурдюки из слонов можно не выворачивать, у них шерсти нет.
-
Часто вегетарианцы оправдываются тем, что всё дело не в составе пищи, а в моральных принципах. Жестоко и негуманно лишать жизни божьих тварей. А чем поедание трупов убиенных растений гуманнее поедания трупов убиенных животных?
-
Это очень распространённый формат для книжных файлов. Я несу свет знаний в тёмные массы благодаря именно этому формату. В интернете имеется куча софта для его чтения - от простеньких утилит до мегапакетов. Установите его на свой комп.
-
Скачал свои вложения на комп, все три открываются. У вас что-то с ПО, не читается формат djvu.
-
Лиха беда начало! Дальше пойдут толуол и эфедрин. Так что намотайте на ус. Пригодится.
-
Эти не подходят, так как нет газовыделения.
-
Вот вам списки того, чего нельзя и того, что можно, но осторожно: Перечень наркотических средств и их прекурсоров.djvu Изменения к списку наркотических веществ и прекурсоров.djvu Перечень СДЯВ.djvu В списки время от времени вносятся изменения. Я за этим не слежу, поэтому некоторые данные из списков могут отличаться от ныне действующих правил. Но думаю, что эти списки вас устроят.
-
Аркадий промахнулся. Дипольный момент воды не высота равнобедренного треугольника, а его основание. Правило сложения векторов. Рисовать мне нечем, попробую объяснить на пальцах. Вначале имеем два исходящих из одной точки вектора длиной 1,58 и искомым углом α между ними. По биссектрисе этого угла направлен результирующий вектор 1,84. Не меняя направления, сдвигаем первый вектор из начальной точки в конец второго вектора. Получаем равнобедренный треугольник со сторонами 1,58 и основанием 1,84. Опускаем перпендикуляр из вершины треугольника на основание. Треугольник равнобедренный, поэтому высота делит основание на две равные части по 0,92. Получился прямоугольный треугольник с гипотенузой 1,58, катетом 0,92 и углом между ними φ = α/2. По определению сos φ = 0,92/1,58 = 0,5823. По таблицам или калькулятором вычисляем угол φ, а затем угол α = 2φ.
-
С этими солями не будет, а вот с сульфидом или гидросульфидом натрия обязан будет реагировать. Дигидроксокарбонат меди(II), что в переводе на человеческий язык означает малахит, хоть и нерастворим в воде, но сульфид меди ещё нерастворимее. В итоге зелёный осадок хоть и не растворится, но почернеет от горя по реакции: Cu2(OH)2CO3 (зелёный) + 2Na2S -> 2CuS (чёрный) + Na2CO3 + 2NaOH Или: Cu2(OH)2CO3 (зелёный) + 2NaHS -> 2CuS (чёрный) + Na2CO3 + 2H2O Аналогичная картина будет при действии раствора щёлочи (для ускорения реакции раствор желательно подогреть): Cu2(OH)2CO3 (зелёный) + 2NaOH -> 2Cu(OH)2 (голубой) + Na2CO3 -> 2CuO (чёрный) + Na2CO3 + 2H2O А если, к примеру, взять раствор сульфата железа(III), то осадок забуреет, а малахит с перепугу превратится в купорос: 3Cu2(OH)2CO3 (зелёный) + 2Fe2(SO4)3 + 3H2O -> 4Fe(OH)3 (бурый) + 6CuSO4 + 3CO2↑ И т. д. Отчего случаются столь странные вещи, вы можете узнать, проштудировав раздел учебника по аналитической химии, касающийся обменных реакций между ионами в растворе и в осадке.
- 4 ответа
-
- 2
-

-
Этой книги Чибисова на Либгене я не нашёл, но там есть парочка других: Чибисов К. В. - Очерки по истории фотографии (1987) Чибисов К. В. и соавт. - Фотография в прошлом, настоящем и будущем (1988) Если интересуют, то вот ссылки на страницы, откуда их можно скачать: https://libgen.gs/index.php?req=Чибисов&columns[]=t&columns[]=a&columns[]=s&columns[]=y&columns[]=p&columns[]=i&objects[]=f&objects[]=e&objects[]=s&objects[]=a&objects[]=p&objects[]=w&topics[]=l&topics[]=c&topics[]=f&topics[]=a&topics[]=m&topics[]=r&topics[]=s&res=25&filesuns=all&curtab=f&order=&ordermode=desc&filesuns=all&page=5 https://libgen.gs/index.php?req=Чибисов&columns[]=t&columns[]=a&columns[]=s&columns[]=y&columns[]=p&columns[]=i&objects[]=f&objects[]=e&objects[]=s&objects[]=a&objects[]=p&objects[]=w&topics[]=l&topics[]=c&topics[]=f&topics[]=a&topics[]=m&topics[]=r&topics[]=s&res=25&filesuns=all&order=&filesuns=all&curtab=f&order=&ordermode=desc&filesuns=all&page=6 PS. Я тоже вспомнил молодость и полез в шкап с многолетними залежами книг. Нарыл там около десятка книг по фотографии. Список книг в спойлере, но сейчас эта тематика уже неактуальна, я думаю. На досуге полистаю, но не уверен, что в них есть что-либо кардинальное по вашей проблеме. В каждой книге ещё по полтора-два десятка библиографических ссылок, но я искать по ним не буду, не моя тема. Если откопаю что-нибудь заслуживающее внимания, то тисну сюда сообщение.
- 21 ответ
-
- 3
-