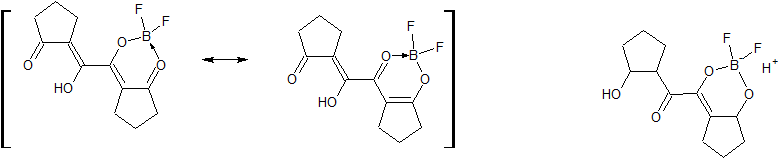-
Постов
34924 -
Зарегистрирован
-
Победитель дней
1163
Весь контент yatcheh
-
Оксимируются альдегиды и кетоны. Амиды напрямую прооксимировать не удастся - слишком жёсткие условия нужны, оксим их просто не выдержит. O=C=C(NH2)2 не существует по причине абсолютной несовместимости аминогруппы с кетеновым фрагментом.
-
В принципе, любой подходит, кроме йодистого метила. Но есть нюансы. Ph-CH=CH-C(CH3)=O [Ph-CH=CH-C+CH3-O-] [Ph-C+H-CH=C(CH3)-O-] Из этих мезомерных форм самая стабильная - вторая, но первая тоже даёт свой вклад. Электрофильный центр при карбонильного углероде - жёсткий (слабо поляризующийся), у β-углерода - мягкий. Поэтому в условиях кинетического контроля для 1,4-присоединения лучше использовать мягкий нуклеофил. Из представленных реагентов самый мягкий - (CH3)2CuLi
-
Br-CH2-CO-O-X, где X - металл, или органический радикал. А это - ацетат брома (ацетилгипобромит).
- 3 ответа
-
- 1
-

-
Тут кроме бромфенола ничего не катит. А этот забор - всякие протонированные/депротонированные ионы.
-
Фосфорной кислотой. Или я уже писал об этом?
-
Это не важно. Если реакция пройдёт (хоть какая-нибудь) смесь пожелтеет. Это основная качественная реакция органической химии на всё
-
В присутствии избытка карбоната - не потеряет.
-
Хлорформиат в отработку добавлять - пусть там гидролизуется, и меняет воду на спирт. Дэтилкарбонат - туда же. Кроме как гидролизоваться, ему деваться некуда, а, учитывая улетание СО2 из раствора - гидролиз будет необратимым. 57С - нормально. Влил, да перемешал. Только от осадка кремнезёма будет трудно избавиться. Бред тут - сама постановка вопроса. Если жалко цинк сливать в канализацию - извлекать его, но это другая задача...
-
Добавить этилхлорформиата. Эквивалент воды заместится эквивалентом спирта и эквивалентом HCl ClCOOEt + H2O => HCl + EtOH + CO2↑ Можно диэтилкарбонат добавить, но тогда спирт будет размножаться OC(OEt)2 + H2O => 2EtOH + CO2↑ Или четырёххлористый кремний, но тогда будет размножаться HCl, и фильтровать придётся SiCl4 + 2H2O => SiO2 + 4HCl Из такой злой смеси селективно воду вытащить - это надо гороху наесться.
-
Ваш "один человек", как говорится "слышал звон, да не знает где он". Во-первых, не "диаминосульфат меди (Сu(NH2)2)SO4", а "сульфат тетраамминмеди [Cu(NH3)4]SO4". Во-вторых, этот комплекс образуется из аммиака и медного купороса, с мочевиной это не пройдёт. Возможно, какое-то комплексообразование с мочевиной и будет, но это - нестойкая ерунда, это никак не изменит сущности ни купороса, ни мочевины. Ну, и в-третьих, этот комплекс отнюдь не теряет своих "медных" свойств в плане микоцидности и прочего. Смесь мочевины с купоросом - это смесь мочевины с купоросом, никаких иных сущностей там не зарождается. С железом - та же фигня.
-
Нда-а-а, батенька... Вы - явно не коллекционер
-
Могут. Никаких теоретических препятствий тут не наблюдается.
- 4 ответа
-
- 1
-

-
А давление? На самом деле там будет равновесная смесь продуктов, CO + CO2. Температура 5800 - это очень много, для этого образования только СО никак не хватит. Мощность ВВ в координатах кислородного баланса, очевидно проходит через максимум, располагающийся выше идеального баланса (БТФ C6N6O6) и ближе к нулевому теоретическому КБ (ОНК C8N8O16). Если отвлечься от привходящих (хотя и важных) обстоятельств - плотности, скорости детонации...
-
Уточните структуру, без этих размазанных связей. Или пририсуйте водороды. Если исходная структура - кетоенол, то получится незаряженная молекула (с разделением зарядов - в цикле плюс, у бора - минус), а если кетоспирт или диол - то несопряжённая:
-
Не годится щёлочь для осушки хлорэтана. Нужен нейтральный осушитель.
-
Нелетучая - оценочная характеристика. Давление пара H2SO4 при н.у. вполне измеримо, и её микроколичества улетают за вполне измеримое время. Но это не главное. Её микроколичества успешно нейтрализуются в присутствии человеков, которые есть - ходячие химические фабрики, производящие в том числе и всякие летучие основания. А есть ещё пыль, всякая микрофлора, которая тоже принимает участие в утилизации химически активной грязи. В результате всё быстро устаканивается, усредняется, нивелируется, в общем - приходит в равновесие.
-
Хлор с озоном на свету вроде реагируют. Правда пишут об этом кто во что горазд. Там и Cl2O получается, и ClO2, и Cl2O6. Но к молибдену это, получается, не имеет никакого отношения. Так, побочка...
-
Может. CH3-C☰CH -(KMnO4)-> [CH3-CH(OH)=CHOH] [CH3-CH(OH)=CHOH] -> CH3-CHOH-CHO -(KMnO4)-> CH3-CHOH-COOH Но это один из возможных продуктов. Практически там будет смесь: CH3-CHOH-COOH + CH3-CO-COOH + CH3-CO-CH2OH + CH3-COOH + CH3-CHOH-CHO + HCHO + HO-CO-CO-OH + CO2 состав которой будет зависеть от соотношения реагентов и условий реакции. Ну, наверное можно, если осторожно