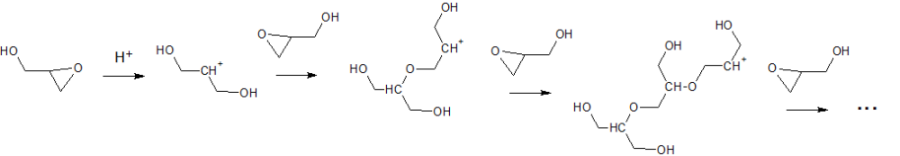-
Постов
34901 -
Зарегистрирован
-
Победитель дней
1162
Весь контент yatcheh
-
В концентрированной - прекрасно!
-
Ничего не изменится. У терефталефой кислоты только один изомер монозамещения. Хоть как её крути - она же плоская
-
1) По привесу. 2) Если по методике отгоняют под вакуумом - это отгонка "в насос". Метанол идёт на выброс. Если вам жалко метанола, и не жалко продукта - попробуйте сэкономить. 3) Димеркаптопропанол - кислота, по силе сравнимая с H2S.
-
Отмывочный раствор должен максимально эффективно пачкаться отмываемой грязью. Это же логично?
-
Я же вам толкую - никакой общей теории не существует. Нет такой книги, которая объясняет всё и вся. Есть главы в букварях, посвящённые этой теме самом общем виде, есть оригинальные статьи, или монографии, затрагивающие конкретные классы веществ. Эта тема - громадная, как та алмазная скала в тысячу ли высотой, куда раз в тысячу лет прилетает орёл, что бы поточить клюв.
-
На самом деле это совершенно не важно. В любом случае будет идти защелачивание анодного пространства в равной степени. Аммиак будет держаться в растворе, проникать в катодную область, где будет гасить кислоту... Какая-то часть будет улетать при нагревании... В целом - это будет толчение воды в ступе.
-
От физических свойств вещества и свойств растворителя. Можно предположить качественную характеристику растворимости - очень хорошо, хорошо, плохо, совсем плохо. Тут - рассуждения "по аналогии". Качественно - на основе геометрии молекулы и свойств элементов, её составляющих. В частности - электроотрицательности и поляризуемости. Количественно - экспериментом. На уже состоявшийся раствор - никак. Перемешивание ускоряет растворение и достижение точки равновесия. Но на интегральную растворимость никак не влияет. На основе предположений, базирующихся на статистических данных о растворимости того-сего в том-сём.
-
Это один из реакционных путей. Естественно, он может обрываться реакциею с гидроксилом и выбросом протона. Тогда - на колу мочало, начинай сначала. В результате получаются совершенно нерегулярная структура с невысокой степенью полимеризации.
-
Всё это прекрасно! Но это - вопрос условий нитрования. Априори нитроизофталевая кислота способна существовать в виде трёх изомеров. Для терефталевой - даже теоретически более одного изомера не нарисуешь.
- 21 ответ
-
- 1
-

-
Обычный механизм - кислотно-катализируемое раскрытие оксиранового цикла. У меня и такой вариант был. Но при повышенной температуре это или обратимо будет, или перекрёстное алкилирование пойдёт. И всё свалится в полиглицерин. Мне так имховалось
-
Тартрат и цитрат - хорошие комплексоны. Свинец выводится в раствор и удаляется вместе с ним. Рис просто промывают вымачиванием в растворе цитрата/тартрата. Естественно, в промывной воде определение свинца будет затруднено, но не более того - всё прекрасно определяется даже на фоне этих комплексонов. А вот в рисе свинец не останется, если уж он перешёл в раствор.
-
А индикатор у вас живой? Холостой опыт не пробовали?
-
полиглицерин
-
Оно самое. Только окись там не получится: 2CaF2 + 2SiO2 => 2CaSiO3 + SiF4↑ С P2O5 получается POF3 с примесью PF5, с борным ангидридом - BF3 с примесью BOF.
-
Так это терефталевая. Исходник ваш - 4-этилтолуол. Схерали тут мета-изомер? У изофталевой кислоты три мононитро-производных.
-
Что значит "не соответствует"? Вместо жёлтый-зелёный получается красный-серобуромалиновый?
-
Нет. Йодирование ароматики - не радикальная реакция. Это электрофильное замещение. Скоростьлимитирующая стадия - присоединение с образованием сигма-комплекса. Водород уходит в виде протона. Поляризация идёт за счёт катализатора - кислоты Льюиса. Проблема именно в энергии активации, суммарный процесс термодинамически разрешён, но первичный акт >C-H + I* => >C* + HI Настолько энергозатратен, что делает реакцию практически невозможной.
-
Никакие это не аргентаты, а смешанные оксиды. По типу магниевых шпинелей, которые можно, конечно, считать солями несуществующей магниевой кислоты, но это такие же смешанные оксиды.